题目内容
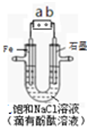 如图是模拟工业电解饱和食盐水的装置图,下列叙述正确的是( )
如图是模拟工业电解饱和食盐水的装置图,下列叙述正确的是( )| A、a为电源的正极 |
| B、通电一段时间后,石墨电极附近溶液先变红 |
| C、Fe电极的电极反应是4OH--4e-═2H2O+O2↑ |
| D、电解饱和食盐水的总反应是:2NaCl+2H2O═2NaOH+H2↑+Cl2↑ |
考点:电解原理
专题:电化学专题
分析:A、工业电解饱和食盐水石墨做电解池的阳极,与电源正极向相连,铁做阴极,与电源负极相连;
B、电解原理为溶液中氯离子在阳极失电子生成氯气,溶液中氢离子在阴极得到电子生成氢气;
C、铁做阴极,溶液中氢离子得到电子生成氢气;
D、电解饱和食盐水氯化钠和水反应是你氢氧化钠、氢气、氯气;
B、电解原理为溶液中氯离子在阳极失电子生成氯气,溶液中氢离子在阴极得到电子生成氢气;
C、铁做阴极,溶液中氢离子得到电子生成氢气;
D、电解饱和食盐水氯化钠和水反应是你氢氧化钠、氢气、氯气;
解答:
解:A、工业电解饱和食盐水石墨做电解池的阳极,与电源正极向相连,铁做阴极,与电源负极相连,a为电源负极,故A错误;
B、电解原理为溶液中氯离子在阳极失电子生成氯气,溶液中氢离子在阴极得到电子生成氢气,铁电极为阴极,附近氢氧根离子浓度增大,酚酞变红色,故B错误;
C、铁做阴极,溶液中氢离子得到电子生成氢气,2H++2e-=H2↑,故C错误;
D、电解饱和食盐水氯化钠和水反应生成氢氧化钠、氢气、氯气,反应的化学方程式2NaCl+2H2O
2NaOH+H2↑+Cl2↑,故D正确;
故选D.
B、电解原理为溶液中氯离子在阳极失电子生成氯气,溶液中氢离子在阴极得到电子生成氢气,铁电极为阴极,附近氢氧根离子浓度增大,酚酞变红色,故B错误;
C、铁做阴极,溶液中氢离子得到电子生成氢气,2H++2e-=H2↑,故C错误;
D、电解饱和食盐水氯化钠和水反应生成氢氧化钠、氢气、氯气,反应的化学方程式2NaCl+2H2O
| ||
故选D.
点评:本题考查了电解原理的分析应用,追要是电极判断,电极反应的分析计算,掌握基础是解题关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列离子方程式正确的是( )
| A、钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| B、硅酸钠溶液与醋酸溶液反应:SiO32-+2H+=H2SiO3↓ |
| C、硫酸铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ |
| D、浓硝酸中加入烧碱溶液:OH-+H+=H2O |
pH相同的等体积H2SO4、HF和CH3COOH三种溶液,分别滴加等浓度的NaOH溶液至恰好中和,消耗NaOH溶液的体积为V1、V2、V3,则三者的大小关系正确的是(已知Ka(HF)=6.8×10-4mol?L-1、Ka(CH3COOH)=1.7×10-5mol?L-1)( )
| A、V3>V2>V1 |
| B、V3=V2=V1 |
| C、V3>V2=V1 |
| D、V1=V2>V3 |
在酸性溶液中,能大量共存的离子组是( )
| A、K+、OH-、S042- |
| B、Cl-、N03-、Cu2+ |
| C、Al3+、C032-、Na+ |
| D、Ca2+、HC03-、NH4+ |
 碳族元素是形成化合物种类最多的元素.
碳族元素是形成化合物种类最多的元素.