题目内容
(1)请回答下列问题:
①已知:①CO(g)+
O2(g)=CO2(g)△H=-283.0kJ?mol-1
②CH3OH(l)+
O2(g)=CO2(g)+2H2O(l)△H=-726.5kJ?mol-1
请写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: ;
②已知拆开1molH-H键、1molCl-Cl键、1molH-Cl键分别需要的能量是436kJ、243kJ、432kJ,则反应则反应:H2(g)+Cl2(g)=2HCl(g)的△H= .
(2)已知25℃、101kPa下,稀的强酸与稀的强碱溶液反应的中和热为-57.3kJ/mol.
①则表示稀硫酸与稀烧碱溶液中和反应的热化学方程式为: .
②测定中和热实验时所需的玻璃仪器有烧杯、量筒、 、 .
①已知:①CO(g)+
| 1 |
| 2 |
②CH3OH(l)+
| 3 |
| 2 |
请写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
②已知拆开1molH-H键、1molCl-Cl键、1molH-Cl键分别需要的能量是436kJ、243kJ、432kJ,则反应则反应:H2(g)+Cl2(g)=2HCl(g)的△H=
(2)已知25℃、101kPa下,稀的强酸与稀的强碱溶液反应的中和热为-57.3kJ/mol.
①则表示稀硫酸与稀烧碱溶液中和反应的热化学方程式为:
②测定中和热实验时所需的玻璃仪器有烧杯、量筒、
考点:热化学方程式,反应热和焓变
专题:化学反应中的能量变化
分析:(1)①依据热化学方程式和盖斯定律计算得到甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式;
②依据焓变△H=反应物拆化学键吸收的能量-生成物形成化学键放出的能量计算得到;
(2)①依据中和热概念书写得到;
②依据中和热测定实验的过程和仪器分析中和热实验时所需的玻璃仪器;
②依据焓变△H=反应物拆化学键吸收的能量-生成物形成化学键放出的能量计算得到;
(2)①依据中和热概念书写得到;
②依据中和热测定实验的过程和仪器分析中和热实验时所需的玻璃仪器;
解答:
解:(1)①:①CO(g)+
O2(g)=CO2(g)△H=-283.0kJ?mol-1
②CH3OH(l)+
O2(g)=CO2(g)+2H2O(l)△H=-726.5kJ?mol-1
依据盖斯定律②-①得到甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为:CH3OH(l)+O2(g)═CO(g)+2H2O(l)△H=-443.5kJ?mol-1 ;
故答案为:CH3OH(l)+O2(g)═CO(g)+2H2O(l)△H=-443.5kJ?mol-1 ;
②已知拆开1molH-H键、1molCl-Cl键、1molH-Cl键分别需要的能量是436kJ、243kJ、432kJ,则反应:H2(g)+Cl2(g)=2HCl(g)的△H=436kJ+243kJ-2×432kJ=-185KJ/mol;
故答案为:-185kJ/mol;
(2)①依据中和热概念分析,稀硫酸与稀烧碱溶液中和反应的热化学方程式为:
H2SO4(aq)+NaOH(aq)=
Na2SO4(aq)+H2O(l)△H=-57.3 kJ/mol;
故答案为:
H2SO4(aq)+NaOH(aq)=
Na2SO4(aq)+H2O(l)△H=-57.3 kJ/mol;
②依据量热计的结果和原理分析,测定中和热实验时所需的玻璃仪器有烧杯、量筒、温度计、环形玻璃搅拌棒;
故答案为:温度计;环形玻璃搅拌棒;
| 1 |
| 2 |
②CH3OH(l)+
| 3 |
| 2 |
依据盖斯定律②-①得到甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为:CH3OH(l)+O2(g)═CO(g)+2H2O(l)△H=-443.5kJ?mol-1 ;
故答案为:CH3OH(l)+O2(g)═CO(g)+2H2O(l)△H=-443.5kJ?mol-1 ;
②已知拆开1molH-H键、1molCl-Cl键、1molH-Cl键分别需要的能量是436kJ、243kJ、432kJ,则反应:H2(g)+Cl2(g)=2HCl(g)的△H=436kJ+243kJ-2×432kJ=-185KJ/mol;
故答案为:-185kJ/mol;
(2)①依据中和热概念分析,稀硫酸与稀烧碱溶液中和反应的热化学方程式为:
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:
| 1 |
| 2 |
| 1 |
| 2 |
②依据量热计的结果和原理分析,测定中和热实验时所需的玻璃仪器有烧杯、量筒、温度计、环形玻璃搅拌棒;
故答案为:温度计;环形玻璃搅拌棒;
点评:本题考查了化学反应能量变化的分析计算,盖斯定律计算应用,键能和焓变的计算关系分析,掌握基础是解题关键,题目较简单.

练习册系列答案
相关题目
常温下有A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4C1溶液、盐酸和Na2SO4溶液中的一种.已知A、B溶液中水的电离程度相同,A、C溶液的pH相同.下列说法中不正确的是( )
| A、D溶液的PH=7 |
| B、四种溶液相比,C溶液中水的电离程度最大 |
| C、A与C等体积混合,溶液中有c(C1-)>c(NH4+)>c(H+)>c(OH-) |
| D、B与D等体积混合后,溶液中有c(OH-)=c(CH3COOH)+c(H+) |
下列化学式表示的一定是纯净物的是( )
| A、C3H8 |
| B、C12H22011 |
| C、C2H402 |
D、 |
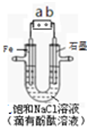 如图是模拟工业电解饱和食盐水的装置图,下列叙述正确的是( )
如图是模拟工业电解饱和食盐水的装置图,下列叙述正确的是( )| A、a为电源的正极 |
| B、通电一段时间后,石墨电极附近溶液先变红 |
| C、Fe电极的电极反应是4OH--4e-═2H2O+O2↑ |
| D、电解饱和食盐水的总反应是:2NaCl+2H2O═2NaOH+H2↑+Cl2↑ |


 原子序数之和为16的三种短周期元素的单质X、Y、Z,常温常压下均为无色气体,在适当条件下X、Y、Z之间可以发生如右图所示的变化.已知B分子组成中Z原子个数比C分子中少一个.
原子序数之和为16的三种短周期元素的单质X、Y、Z,常温常压下均为无色气体,在适当条件下X、Y、Z之间可以发生如右图所示的变化.已知B分子组成中Z原子个数比C分子中少一个.