��Ŀ����
5��2-����������һ��ҽҩ��ȡ���м��壬�㷺Ӧ����ҽҩ�����Ϻ�ũҩ�ĺϳɣ���ṹ��ʽ��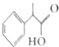 ��ʾ��
��ʾ��������ͨ�����·����ϳɣ�
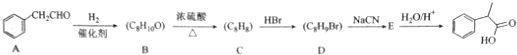
��֪��R-Br$\stackrel{NaCN}{��}$R-CN$\underset{\stackrel{{H}_{2}O/{H}^{+}}{��}}{\;}$R-COOH
�����������̻ش������й����⣺
��1����FeCl3��Һ����ɫ�ұ�����������ȡ������A��ͬ���칹����3�֣����б����Ϻ˴Ź�������Ϊ2����������Ϊ1��1��ͬ���칹��Ľṹ��ʽΪ
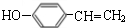 ��
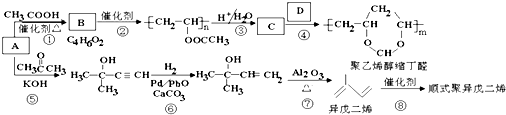
����2��B��C�Ļ�ѧ����ʽΪ
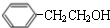 $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$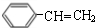 +H2O��C��D�ķ�Ӧ����Ϊ�ӳɷ�Ӧ��
+H2O��C��D�ķ�Ӧ����Ϊ�ӳɷ�Ӧ����3���л���C������Ϊ����ϩ��C��һ�������¿������ɸ߾���F��F�Ľṹ��ʽΪ
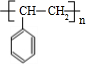 ��
����4�������й�2-�������ᣨ
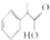 ����������ȷ����B������ĸ��ţ�
����������ȷ����B������ĸ��ţ�A����FeCl3��Һ��������ɫ
B���ɷ���������Ӧ�ͼӳɷ�Ӧ
C��������ˮ����ȡ����Ӧ
D������NaI��NaOH��Na2CO3��NaHCO3��Ӧ��
���� D��-Br��-CNȡ������E��E����ˮ�ⷴӦ�õ� ����EΪ
����EΪ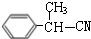 ��DΪ
��DΪ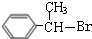 �����ƿ�֪CΪ
�����ƿ�֪CΪ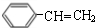 ��BΪ
��BΪ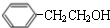 ��
��
��� �⣺D��-Br��-CNȡ������E��E����ˮ�ⷴӦ�õ� ����EΪ
����EΪ ��DΪ
��DΪ �����ƿ�֪CΪ
�����ƿ�֪CΪ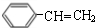 ��BΪ
��BΪ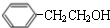 ��
��
��1����FeCl3��Һ����ɫ�ұ�����������ȡ������A��ͬ���칹�壬���з��ǻ���-CH=CH2�����ڡ��䡢��3�֣����б����Ϻ˴Ź�������Ϊ2����������Ϊ1��1��ͬ���칹��Ľṹ��ʽΪ ��
��
�ʴ�Ϊ��3�� ��
��
��2��B��C�Ļ�ѧ����ʽΪ��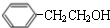 $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$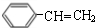 +H2O��C��D�DZ���ϩ��HBr�����ӳɷ�Ӧ��
+H2O��C��D�DZ���ϩ��HBr�����ӳɷ�Ӧ��
�ʴ�Ϊ��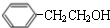 $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$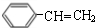 +H2O���ӳɷ�Ӧ��
+H2O���ӳɷ�Ӧ��
��3���л���CΪ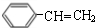 ������Ϊ����ϩ��C��һ�������¿������ɸ߾���F��F�Ľṹ��ʽΪ
������Ϊ����ϩ��C��һ�������¿������ɸ߾���F��F�Ľṹ��ʽΪ  ��
��
�ʴ�Ϊ������ϩ�� ��
��
��4��A���������ǻ�����FeCl3��Һ��������ɫ����A����
B�������Ȼ����ɷ���������Ӧ�����б��������з����ӳɷ�Ӧ����B��ȷ��
C����������ˮ����ȡ����Ӧ����C����
D�������Ȼ�������NaOH��Na2CO3��NaHCO3��Ӧ��������NaI��Ӧ����D����
��ѡ��B��
���� ���⿼���л����ƶϡ��л���Ľṹ�����ʡ�ͬ���칹����д���л���Ӧ���͵ȣ����ݷ�Ӧ���������ƶϣ��������չ����ŵ�������ת�����Ѷ��еȣ�

| A�� | HClO��NaOH��Һ��Ӧ H++OH-�TH2O | |
| B�� | CaCO3��ϡ���ᷴӦ CO32-+2H+�TCO2��+H2O | |
| C�� | Fe��ϡH2SO4��Ӧ 2Fe+6H+�T2Fe3++3H2�� | |
| D�� | �����Ba��OH��2��Һ��Ӧ H++OH-�TH2O |
| A�� | CH3COOH | B�� | 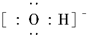 | C�� | �����¶� | D�� | NaOH |
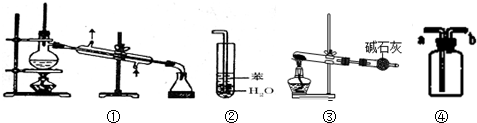
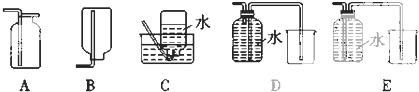
| A�� | װ�âٳ����ڷ��뻥�����ܵ�Һ������ | |
| B�� | װ�âڿ��������հ�������ֹ���� | |
| C�� | ��KClO3 Ϊԭ�ϣ�װ�âۿ������Ʊ�����O2 | |
| D�� | װ�â�a���ڿ��ռ�H2��CO ������ |
| A�� | C3O2���ӡ�COS������̼ԭ�ӿ��ܶ���ȡsp�ӻ� | |
| B�� | C3O2��CO2����̼����������ǻ�Ϊͬ���칹�� | |
| C�� | COS���ɼ��Լ����ɵķǼ��Է��ӣ�����������ԭ�Ӷ�����8�����ȶ��ṹ | |
| D�� | COS����������ȫȼ�գ���������CO2��SO3 |
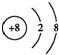 ��A��F��Ԫ����ɵĻ��������ʽΪNa+[��H]-��
��A��F��Ԫ����ɵĻ��������ʽΪNa+[��H]-��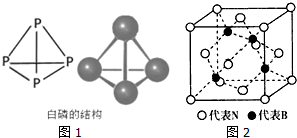 �������ڱ���ͬ��Ԫ�ص������ԣ���Ԥ��Ԫ�ص����ʣ�
�������ڱ���ͬ��Ԫ�ص������ԣ���Ԥ��Ԫ�ص����ʣ�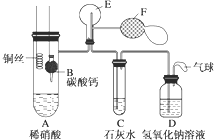
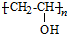 ��CH3CH2CH2CHO��
��CH3CH2CH2CHO��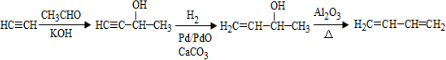 ��
��