题目内容
5.在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应N2(g)+3H2(g)?2NH3(g)△H<0,其化学平衡常数K与温度t的关系如表:| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
②400℃时,其逆反应2NH3(g)?N2(g)+3H2(g)的化学平衡常数的值为:2.
分析 ①由△H<0可知,该反应为放热反应,升高温度,平衡逆向移动,K减小;
②互为逆反应时,K互为倒数关系,以此来计算.
解答 解:①由△H<0可知,该反应为放热反应,升高温度,平衡逆向移动,K减小,则K1>K2,
故答案为:>;
②由表格数据可知,400℃时N2(g)+3H2(g)?2NH3(g)K=0.5,则400℃时,其逆反应2NH3(g)?N2(g)+3H2(g)的化学平衡常数的值为$\frac{1}{0.5}$=2,
故答案为:2.
点评 本题考查化学平衡的计算,为高频考点,把握温度与K的关系、正逆反应K的关系为解答的关键,侧重分析与计算能力的考查,注意表格数据的应用,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1;反应Fe(s)+H2O(g)?FeO(s)+H2(g)△H2,平衡常数为K2
在不同温度时K1、K2的值如表:
反应CO2(g)+H2(g)?CO(g)+H2O(g)△H,平衡常数为K,则△H=△H1-△H2(用△H1和△H2表示),K=$\frac{{K}_{1}}{{K}_{2}}$(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g)?CO(g)+H2O(g)是吸热反应(填“吸热”或“放热”).
在不同温度时K1、K2的值如表:
| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
17.维生素C是一种水溶性维生素(其水溶液呈酸性),它的化学式是C6H8O6,人体缺乏这样的维生素能得坏血症,所以维生素C又称抗坏血酸.在新鲜的水果、蔬菜、乳制品中都富含维生素C,例如新鲜橙汁中维生素C的含量在500mg/L左右.十二中某研究性学习小组测定了某品牌软包装橙汁中维生素C的含量,下面是他们的实验分析报告.
(一)测定目的:测定×××牌软包装橙汁中维生素C的含量.
(二)测定原理:C6H8O6+I2→C6H6O6+2H++2I-
(三)实验用品及试剂
(1)仪器和用品(自选,略)
(2)试剂:指示剂淀粉溶液(填名称),浓度为8.00×10-3mol•L-1的I2标准溶液、蒸馏水等.
(四)实验过程
(3)洗涤仪器,检查滴定管是否漏液,润洗相关仪器后,装好标准碘溶液待用.
(4)用酸式滴定管(填仪器名称)向锥形瓶中移入20.00mL待测橙汁,滴入2滴指示剂.
(5)用左手控制滴定管的活塞(填部位),右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化,直到滴定终点.滴定至终点时的现象是最后一滴标准液滴入时,溶液由无色变为蓝色,且半分钟内不褪色.
(五)数据记录与处理
(6)若经数据处理,则此橙汁中维生素C的含量是1056.00mg/L.
(六)问题讨论
(7)从分析数据看,此软包装橙汁是否是纯天然橙汁?不是(填“是”或“不是”或“可能是”,1分).生产商最可能采取的做法是B(填编号):
A.加水稀释天然橙汁 B.将维生素C作为添加剂 C.橙汁已被浓缩.
(一)测定目的:测定×××牌软包装橙汁中维生素C的含量.
(二)测定原理:C6H8O6+I2→C6H6O6+2H++2I-
(三)实验用品及试剂
(1)仪器和用品(自选,略)
(2)试剂:指示剂淀粉溶液(填名称),浓度为8.00×10-3mol•L-1的I2标准溶液、蒸馏水等.
(四)实验过程
(3)洗涤仪器,检查滴定管是否漏液,润洗相关仪器后,装好标准碘溶液待用.
(4)用酸式滴定管(填仪器名称)向锥形瓶中移入20.00mL待测橙汁,滴入2滴指示剂.
(5)用左手控制滴定管的活塞(填部位),右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化,直到滴定终点.滴定至终点时的现象是最后一滴标准液滴入时,溶液由无色变为蓝色,且半分钟内不褪色.
(五)数据记录与处理
| 起始(mL) | 终点(mL) | |
| 1 | 5.00 | 20.02 |
| 2 | 3.00 | 18.00 |
| 3 | 4.00 | 18.98 |
(六)问题讨论
(7)从分析数据看,此软包装橙汁是否是纯天然橙汁?不是(填“是”或“不是”或“可能是”,1分).生产商最可能采取的做法是B(填编号):
A.加水稀释天然橙汁 B.将维生素C作为添加剂 C.橙汁已被浓缩.
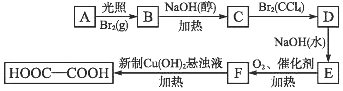

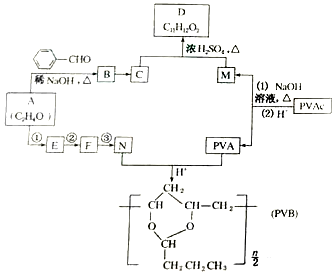
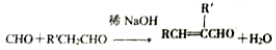 (R、R′表示烃基或氢)
(R、R′表示烃基或氢)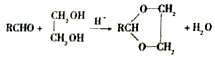
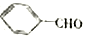 合成B的化学方程式是
合成B的化学方程式是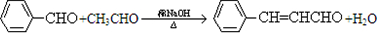 .
.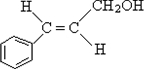 .
.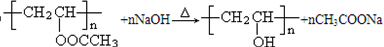 .
.
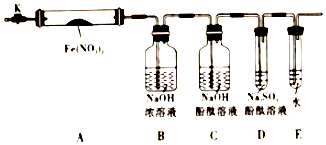 固体硝酸盐加热易分解且产物较复杂,某学习小组以Fe(NO3)2为研究对象,通过实验探究其热分解的产物,查阅资料,根据硝酸盐受热分解的规律,提出如下4种猜想:
固体硝酸盐加热易分解且产物较复杂,某学习小组以Fe(NO3)2为研究对象,通过实验探究其热分解的产物,查阅资料,根据硝酸盐受热分解的规律,提出如下4种猜想: