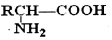题目内容
10.某实验小组把CO2通入饱和Na2CO3溶液制取NaHCO3,装置如图1所示(气密性已检验,部分夹持装置略):
(1)C中反应的化学方程式是Na2CO3+CO2+H2O═2NaHCO3.
(2)请结合化学平衡移动原理解释B中溶液的作用CO2在水中存在平衡:CO2+H2O?H2CO3?HCO3-+H+,有H2SO4存在时,可使上述平衡向左移动,从而减少CO2在水中的溶解,同时吸收挥发出来的HCl气体.
(3)当C中有大量白色固体析出时,停止实验,将固体过滤、洗涤、干燥备用.为确定固体的成分,实验步骤如下:
第一步:准确称取一定质量的固体,配成1000mL溶液作为样液,其余固体备用.配制溶液时肯定不需要如图2所示仪器中的AC(填字母),配制上述溶液还需用到的玻璃仪器是烧杯、玻璃棒(填仪器名称).
第二步:设计方案如下.
①方案1:取样液与澄清的Ca(OH)2溶液混合,出现白色沉淀.
实验小组对现象产生的原理进行分析,认为该方案不合理,理由是Na2CO3和NaHCO3都能跟Ca(OH)2溶液发生反应生成白色沉淀,无法确定固体的成分中是否含有NaHCO3.
②方案2:取样液与BaCl2溶液混合,出现白色沉淀并有气体产生.
实验小组认为固体中存在NaHCO3,其离子方程式是2HCO3-+Ba2+=BaCO3↓+CO2↑+H2O.
该小组认为不能确定是否存在Na2CO3,你认为该结论是否合理?合理.
③方案3:实验小组中甲、乙同学利用NaHCO3的不稳定性进行如下实验:
甲同学:取样液400mL,用pH计测溶液pH,再水浴加热蒸发至200mL,接下来的操作是冷却到室温,
加水至溶液体积为400mL,再次测定pH,结果表明白色固体中存在NaHCO3.为进一步证明白色固体是否为纯净的NaHCO3,结合甲同学实验,还应补充的实验是取相同质量的纯净的NaHCO3配成1000mL溶液,取400mL,重复甲的实验,进行对照.
乙同学:利用仪器测定了固体残留率随温度变化的曲线,如图3所示.
已知:残留率=$\frac{剩余固体的质量}{原始固体的质量}$×100%
根据A点坐标得到的结论是白色固体为NaHCO3.
分析 (1)由图可知,A中生成二氧化碳,在C中二氧化碳与碳酸钠、水反应生成碳酸氢钠;
(2)B中酸可抑制二氧化碳的溶解;
(3)配制溶液是计算固体质量,称量、溶解、转移、洗涤转移、定容、摇匀得到溶液,据此选择仪器;
①Na2CO3和NaHCO3都能跟Ca(OH)2溶液发生反应生成白色沉淀;
②样液与BaCl2溶液混合,现白色沉淀并有气体产生,沉淀为碳酸钡、气体为二氧化碳;Na2CO3和BaCl2溶液混合也能生成沉淀;
③甲同学:蒸发后冷却,测定pH,可确定固体存在碳酸氢钠,补充实验为对比性实验;
乙同学:A点说明碳酸氢钠分解,残留率为63.09%.
解答 解:(1)由图可知,A中生成二氧化碳,在C中二氧化碳与碳酸钠、水反应生成碳酸氢钠,该反应为Na2CO3+CO2+H2O═2NaHCO3,
故答案为:Na2CO3+CO2+H2O═2NaHCO3;
(2)B中酸可抑制二氧化碳的溶解,则B中溶液的作用为CO2在水中存在平衡:CO2+H2O?H2CO3?HCO3-+H+,有H2SO4存在时,可使上述平衡向左移动,从而减少CO2在水中的溶解,同时吸收挥发出来的HCl气体,
故答案为:CO2在水中存在平衡:CO2+H2O?H2CO3?HCO3-+H+,有H2SO4存在时,可使上述平衡向左移动,从而减少CO2在水中的溶解,同时吸收挥发出来的HCl气体;
(3)准确称取一定质量的固体,配成1000mL溶液作为样液,其余固体备用,结合步骤分析可知,配制溶液时肯定不需要如图2所示仪器中的A、C,配制上述溶液还需用到的玻璃仪器是搅拌所用玻璃棒,溶解用的烧杯,
故答案为:AC;烧杯、玻璃棒;
①Na2CO3和NaHCO3都能跟Ca(OH)2溶液发生反应生成白色沉淀,所以无法确定固体的成分中是否含有NaHCO3,
故答案为:Na2CO3和NaHCO3都能跟Ca(OH)2溶液发生反应生成白色沉淀,无法确定固体的成分中是否含有NaHCO3;
②样液与BaCl2溶液混合,现白色沉淀并有气体产生,沉淀为碳酸钡、气体为二氧化碳,离子反应为2HCO3-+Ba2+=BaCO3↓+CO2↑+H2O;Na2CO3和BaCl2溶液混合也能生成沉淀,则不能确定是否存在Na2CO3,结论合理,
故答案为:2HCO3-+Ba2+=BaCO3↓+CO2↑+H2O;合理;
③甲同学:取样液400mL,用pH计测溶液pH,再水浴加热蒸发至200mL,接下来的操作是冷却到室温,加水至溶液体积为400mL,再次测定pH,可确定固体存在碳酸氢钠,补充实验为取相同质量的纯净的NaHCO3配成1000mL溶液,取400mL,重复甲的实验,进行对照,
故答案为:冷却到室温,加水至溶液体积为400mL,再次测定pH;取相同质量的纯净的NaHCO3配成1000mL溶液,取400mL,重复甲的实验,进行对照;
乙同学:A点说明碳酸氢钠分解,残留率为63.09%,可知白色固体为碳酸氢钠,
故答案为:白色固体为NaHCO3.
点评 本题考查化学实验方案的评价,涉及物质的性质,盐类水解、化学平衡、差量法计算、图象分析较等,综合性较强,差量的计算方法为解答的难点,题目难度较大.

I.测定牙膏中摩擦剂碳酸钙的含量:利用如图所示装置进行实验,充分反应后,通过测定C中生成沉淀的质量来确定样品中碳酸钙的质量分数.图中夹持仪器略去.
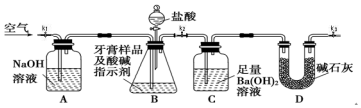
依据实验过程回答下列问题:
(1)以下检查整套装置气密性的操作正确的是a(填字母代号).
a.组装好仪器后,关闭K1和K3、打开K2,分液漏斗中装水.打开分液漏斗的两个活塞,若漏斗中水下滴一会后停止,且液面不再降低,则整套装置不漏气.
b.裝好药品后,关闭K1和K3、打开K2.打开分液漏斗的两个活塞,若漏斗中盐酸下滴一会后停止,且液面不再降低,则整套装置不漏气.
c.短时间轻微加热B,若A中溶液进入长导管,C中长导管冒气泡,则整套装置不漏气.
(2)实验过程中需持续缓慢通入空气,其作用除了可搅拌B、C中的反应物外,还有把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收.
(3)盐酸有一定程度的挥发性,为什么实验时不在B、C之间增添盛有饱和碳酸氢钠溶液的洗气装置?碳酸氢钠虽能吸收盐酸,但也产生CO2,HCl即使进入装置C中,由于Ba(OH)2是足量的,就会被Ba(OH)2中和,不会溶解BaCO3.
(4)实验中准确称取20.00g样品三份,进行三次测定,测得BaCO3平均质量为7.88g.则样品中碳酸钙的质量分数为20.0%.
II.为确定该牙膏摩擦剂中氢氧化铝的存在,请设计实验.
| 实验步骤 | 预期现象与结论 |
| 取适量牙膏样品于试管中,加入足量的NaOH溶液,过滤,向滤液中滴加盐酸. | 滤液中先出现白色沉淀,随后沉淀溶解,说明该牙膏摩擦剂中含氢氧化铝. |
实验Ⅰ:

(1)无色气体为NH3.
(2)该固体混合物的成分为NH4I、MgBr2、AlCl3.
实验Ⅱ:取一定量的该固体混合物溶于水配成1L溶液,并向该混合溶液中通入一定量的Cl2,测得溶液中几种阴离子(分别用A-、B-、C-表示)的物质的量与通入Cl2体积的关系如表所示.
| Cl2的体积 (标准状况下)/L | 2.8 | 5.6 | 11.2 |
| n(A-)/mol | 1.25 | 1.5 | 2 |
| n(B-)/mol | 1.5 | 1.4 | 0.9 |
| n(C-)/mol | a | 0 | 0 |
(4)原固体混合物中各组成成分的物质的量之比为.
| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
②400℃时,其逆反应2NH3(g)?N2(g)+3H2(g)的化学平衡常数的值为:2.
| A | B | C | D | E | F | G | H | I | J | |
| 原子半径 (10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 | 1.02 | 0.037 |
| 最高或最低 化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | +6 | +1 | |
| -2 | -3 | -1 | -3 | -2 |
(1)D在元素周期表中的位置第三周期第VA族,若H的一种同位素中子数为5,则其原子符号是510B,B元素的原子结构示意图是
 ,G与F分别形成的简单离子半径大小关系为N3->Na+.
,G与F分别形成的简单离子半径大小关系为N3->Na+.(2)F与A形成的化合物电子式是:
 、
、 .
.(3)用电子式表示F2I的形成过程:
 ;
;(4)F与J形成的化合物电子式为
 ,该化合物与水反应放出气体的化学方程式为NaH+H2O=NaOH+H2↑..
,该化合物与水反应放出气体的化学方程式为NaH+H2O=NaOH+H2↑.. 
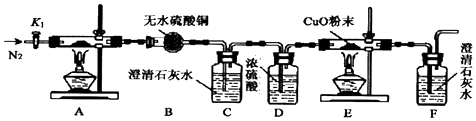
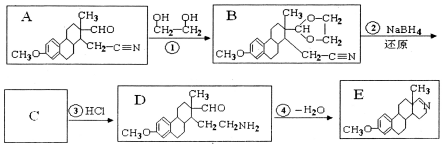
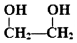 的名称为乙二醇;写出其与对苯二甲酸反应生成高聚物的化学方程式
的名称为乙二醇;写出其与对苯二甲酸反应生成高聚物的化学方程式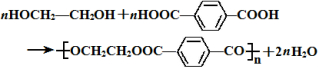 ;
;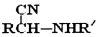 $\stackrel{H+}{→}$
$\stackrel{H+}{→}$