题目内容
14.NH3是重要的化工原料.(1)实验室常用NH4Cl和Ca(OH)2制备NH3,该反应的方程式为2NH4Cl(固体)+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.反应发生装置、气体收集装置和尾气处理装置依次为A、C、G.

(2)按图2装置(A、B两容器体积相等,温度相等)进行NH3性质实验.
①先打开旋塞1,B瓶中的现象是产生白烟,原因是NH3+HCl═NH4Cl(用化学方程式表示),稳定后,关闭旋塞1.
②再打开旋塞2,B瓶中的现象是烧杯中的石蕊溶液会流入B瓶,且溶液有紫色变为红色.
分析 (1)实验室用加热氯化铵与氢氧化钙的方法制取氯气,依据反应物状态与反应条件选择发生装置,依据氨气密度小于空气密度,易溶于水,选择收集方法,氨气为碱性气体,易溶于水,尾气处理可以用水吸收,注意防止倒吸的发生;
(2)①根据A、B容器压强以及A、B混合后压强相等以及氨气和氯化氢反应生成氯化铵分析;
②氨气、氯化氢为气体反应生成的氯化铵为固体,压强减小,氯化铵为强酸弱碱盐,溶液呈酸性,据此分析.
解答 解:(1)实验室用加热氯化铵与氢氧化钙的方法制取氯气,方程式:2NH4Cl(固体)+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,反应物状态为固体+液体,反应条件为加热,所以应选择A做发生装置,氨气密度小于空气密度,易溶于水,应选择向下排空气法收集,所以应选择装置C为收集装置,氨气为碱性气体,易溶于水,尾气处理可以用水吸收,容易发生倒吸,为防止倒吸应选择装置G为尾气处理装置;
故答案为:2NH4Cl(固体)+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;ACG;
(2)①A容器压强为150KPa,B容器压强100KPa,A容器压强大于B容器,先打开旋塞1,A容器中的氯化氢进入B容器,氨气和氯化氢反应,NH3+HCl=NH4Cl,生成氯化铵固体小颗粒,所以B瓶中的现象是出现白烟,
故答案为:产生白烟;NH3+HCl=NH4Cl;
②氨气、氯化氢为气体反应生成的氯化铵为固体,压强减小,再打开旋塞2,紫色的石蕊试液倒吸入B瓶中,氯化铵为强酸弱碱盐,溶液中铵根离子水解生成一水合氨和氢离子,水解方程式为:NH4++H2O?NH3•H2O+H+,溶液呈酸性,所以紫色石蕊试液变红,
故答案为:烧瓶中的液体倒吸入B瓶,且紫色石蕊试液变红.
点评 本题考查了氨气的实验室制备及氨气性质的检验,掌握实验室制取氨气的制备原理和性质是解题关键,题目难度不大.

 如图,p、q为直流电源两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D产生气泡.试回答:
如图,p、q为直流电源两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D产生气泡.试回答:(1)p为正极,A极发生了氧化(填反应类型)反应.
(2)D为阴极,试管里收集到H2.
(3)C极的电极方程式是4OH--4e-=O2↑+2H2O.
(4)在电解过程中,测得C、D两极上产生的气体的实验数据如下:
| 时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 阴极生成 气体体积(cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 | 79 | 89 |
| 阳极生成 气体体积(cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
(5)当电路中通过0.004mol电子时,B电极上沉积金属X的质量为0.128g,则此金属的摩尔质量为64g•mol-1.
(6)当反应进行一段时间后,A、B电极附近溶液的pH不变(填“增大”、“减小”或“不变”).
| A. | d元素最高价氧化物对应的水化物酸性比c最高价氧化物对应的水化物酸性强 | |
| B. | e与氢气化合比b与氢气化合更容易 | |
| C. | a元素的氢化物是离子化合物 | |
| D. | c在空气中点燃可生成其最高价氧化物 |
| A. | 根据金属失去电子的多少来判断,失去电子较多的金属性较强 | |
| B. | 用钠置换MgCl2溶液中的Mg2+,来验证钠的金属性强于Mg | |
| C. | Mg不与NaOH溶液反应而Al能与NaOH溶液反应,可说明金属性:Al>Mg | |
| D. | 碱性:NaOH>Mg(OH)2>Al(OH)3,可说明钠、镁、铝金属性依次减弱 |
| A. | 乙酸钾 | B. | 甲醇 | C. | 乙醛 | D. | 乙酸 |

 .
.
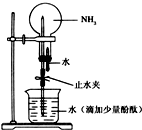 有关氨的实验室制取和性质实验如下:
有关氨的实验室制取和性质实验如下: