题目内容
19.电子式(1)甲烷

(2)羟基
 .
.
分析 (1)甲烷分子为共价化合物,分子中含有4个碳氢键,碳原子最外层满足8电子稳定结构,据此写出甲烷的电子式;
(2)羟基为中性原子团,碳原子最外层电子数为7,据此写出羟基的电子式.
解答 解:(1)1个甲烷分子中含1个C、4个H原子,分子式为CH4,碳原子的最外层有4个电子,氢原子最外层1个电子,一个碳原子形成4对共用电子对,一个氢原子形成一对共用电子对,所以电子式为 ,
,
故答案为: ;
;
(2)氧原子与氢原子通过一对共用电子对连接,羟基中的氧原子含有一个未成对电子,其电子式为 ,
,
故答案为: .
.
点评 本题考查了电子式的书写,题目难度不大,明确电子式的概念及书写原则为解答关键,注意掌握羟基与氢氧根离子、甲基与甲烷的电子式的区别,试题有利于提高学生的灵活应用基础知识的能力.

练习册系列答案
相关题目
9.下列叙述正确的是( )
| A. | 含有极性键的化合物分子内一定不含有非极性键 | |
| B. | 分子内两种非金属元素的原子之间形成的化学键是极性键 | |
| C. | 离子化合物中一定含有金属阳离子和离子键 | |
| D. | 两种元素构成的共价化合物分子中的化学键一定都是极性键 |
10.下列各组物质中互为同分异构体的是( )
| A. | 1H与2H | B. | O2与O3 | C. | 乙烯与丙烯 | D. | 正丁烷与异丁烷 |
7.能贮存在具有玻璃塞的磨口试剂瓶里的试剂是( )
| A. | HF溶液 | B. | KOH溶液 | C. | 盐酸 | D. | 水玻璃 |
11.下列表述正确的是( )
| A. | H、D、T互为同素异形体 | B. | 中子数为20的氯原子: | ||
| C. | 四氯化碳的电子式: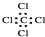 | D. | Cl-的结构示意图: |
8.下列各组中属于同位素关系的是( )
| A. | ${\;}_{19}^{40}K$与${\;}_{20}^{40}Ca$ | B. | D2O与T2O | ||
| C. | ${\;}_{19}^{40}K$与${\;}_{19}^{39}K$ | D. | 白磷与红磷 |
