题目内容
8.根据下列实验操作和现象所得到的结论正确的是( )| 选项 | 实验操作和现象 | 结论 |
| A | 室温下,向苯酚钠溶液中通入足量CO2,溶液变浑浊. | 碳酸的酸性比苯酚的强 |
| B | 室温下,向浓度均为0.1mol•L-1的BaCl2和CaCl2混合溶液中滴加Na2SO4溶液,出现白色沉淀. | Ksp(Ba2S O4)<Ksp(Ca2S O4) |
| C | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色. | Fe2+的氧化性比I2的强 |
| D | 室温下,用PH试纸测得:0.1mol•L-1 Na2SO3溶液的PH约为10;0.1mol•L-1 NaHSO3溶液的PH约为5. | HSO3-结合H+的能力比SO32-的强 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.向苯酚钠溶液中通入足量CO2,反应生成苯酚;
B.硫酸钡、硫酸钙均为白色沉淀;
C.向FeCl3溶液中滴加少量KI溶液,发生氧化还原反应生成碘、亚铁离子;
C.NaHSO3溶液电离大于其水解,Na2SO3溶液水解显碱性.
解答 解:A.向苯酚钠溶液中通入足量CO2,反应生成苯酚,由强酸制取弱酸的反应原理可知,碳酸的酸性比苯酚的强,故A正确;
B.硫酸钡、硫酸钙均为白色沉淀,则不能比较Ksp,故B错误;
C.向FeCl3溶液中滴加少量KI溶液,发生氧化还原反应生成碘、亚铁离子,可知Fe3+的氧化性比I2的强,故C错误;
C.NaHSO3溶液电离大于其水解,Na2SO3溶液水解显碱性,则HSO3-结合H+的能力比SO32-的弱,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应、Ksp比较、氧化性比较、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.下列说法正确的是( )
| A. | 摩尔是国际单位制中的七个基本物理量之一 | |
| B. | 1molO2中约含有6.02×1023个O2 | |
| C. | 1mol任何物质都含有6.02×1023个原子 | |
| D. | 摩尔表示物质的量 |
13.下列说法正确的是( )
| A. | 加入过量氨水,有白色沉淀生成,则原溶液中一定有Al3+ | |
| B. | 加入盐酸酸化的BaCl2溶液,有白色沉淀生成,则原溶液一定有SO42- | |
| C. | 向某溶液中先加入氯水振荡,再加KSCN溶液后显血红色,该溶液中一定有Fe2+ | |
| D. | 向某溶液中先加入新制饱和氯水,再加CCl4,振荡,分层,下层呈橙红色,则该溶液中一定含有Br- |
17.下列分子中,所有原子都处在同一平面的是( )
| A. | 环己烯 | B. | 丙烯 | C. | 乙烷 | D. | 氯乙烯 |
18.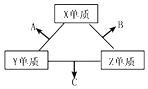 三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如图变化.一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10.下列判断正确的是( )
三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如图变化.一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10.下列判断正确的是( )
 三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如图变化.一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10.下列判断正确的是( )
三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如图变化.一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10.下列判断正确的是( )| A. | 原子半径:Z<Y<X | B. | 非金属性 Z>Y>X | ||
| C. | 化合物A易溶于水 | D. | 化合物B与C的混合物呈碱性 |

 (或
(或 ),A分子中一定共面的碳原子有8个.
),A分子中一定共面的碳原子有8个. (或
(或 )(任写一种).
)(任写一种).