题目内容
20.标准状况下,67.2L CO2的质量为13.2g,其中含有0.6mol氧原子.分析 结合n=$\frac{V}{Vm}$、m=nM及分子构成计算.
解答 解:标准状况下,67.2L CO2的质量为$\frac{6.72L}{22.4L/mol}$×44g/mol=13.2g,其中含有$\frac{6.72L}{22.4L/mol}$×2=0.6mol氧原子,
故答案为:13.2;0.6.
点评 本题考查物质的量的计算,为高频考点,把握质量、物质的量、体积的关系为解答的关键,侧重分析与计算能力的考查,注意物质的构成,题目难度不大.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
11.下列反应中,属于有机物引入官能团反应的是( )
| A. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | B. | CH2=CH2+H2$→_{△}^{催化剂}$CH3-CH3 | ||
| C. |  +3H2$→_{△}^{Ni}$ +3H2$→_{△}^{Ni}$ | D. |  +HNO3(浓)$\stackrel{浓H_{2}SO_{4}}{→}$ +HNO3(浓)$\stackrel{浓H_{2}SO_{4}}{→}$ NO2+H2O NO2+H2O |
8.根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 室温下,向苯酚钠溶液中通入足量CO2,溶液变浑浊. | 碳酸的酸性比苯酚的强 |
| B | 室温下,向浓度均为0.1mol•L-1的BaCl2和CaCl2混合溶液中滴加Na2SO4溶液,出现白色沉淀. | Ksp(Ba2S O4)<Ksp(Ca2S O4) |
| C | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色. | Fe2+的氧化性比I2的强 |
| D | 室温下,用PH试纸测得:0.1mol•L-1 Na2SO3溶液的PH约为10;0.1mol•L-1 NaHSO3溶液的PH约为5. | HSO3-结合H+的能力比SO32-的强 |
| A. | A | B. | B | C. | C | D. | D |
12. 我国利用合成气直接制烯烃获重大突破,其原理是( )
我国利用合成气直接制烯烃获重大突破,其原理是( )
反应①:C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1
反应②:C(s)+H2O(g)?CO(g)+H2(g)△H2
反应③:CO(g)+2H2(g)?CH3OH(g)△H3=-90.1kJ•mol-1
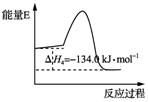
反应④:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H4,能量变化如图所示
反应⑤:3CH3OH(g)?CH3CH═CH2(g)+3H2O(g)△H5=-31.0kJ•mol-1
下列说法正确的是( )
 我国利用合成气直接制烯烃获重大突破,其原理是( )
我国利用合成气直接制烯烃获重大突破,其原理是( )反应①:C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1
反应②:C(s)+H2O(g)?CO(g)+H2(g)△H2
反应③:CO(g)+2H2(g)?CH3OH(g)△H3=-90.1kJ•mol-1
反应④:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H4,能量变化如图所示
反应⑤:3CH3OH(g)?CH3CH═CH2(g)+3H2O(g)△H5=-31.0kJ•mol-1
下列说法正确的是( )
| A. | 反应③使用催化剂,△H3减小 | |
| B. | 反应④中正反应的活化能大于逆反应的活化能 | |
| C. | △H1-△H2<0 | |
| D. | 3CO(g)+6H2(g)?CH3CH═CH2(g)+3H2O(g)△H=-121.1 kJ•mol-1 |
9.下列物质中,可溶于水的是( )
| A. | 胆固醇: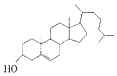 | B. | 芬必得: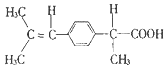 | ||
| C. | 保幼激素JH-I: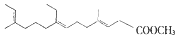 | D. | 维生素C: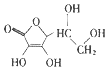 |
10. 如图是一种新型燃料电池装置示意图,该电池以溶有电解质A的稀盐酸为电解质溶液,它不仅能提供电能,还能起到固氮作用.下列对该电池的说法不正确的是( )
如图是一种新型燃料电池装置示意图,该电池以溶有电解质A的稀盐酸为电解质溶液,它不仅能提供电能,还能起到固氮作用.下列对该电池的说法不正确的是( )
 如图是一种新型燃料电池装置示意图,该电池以溶有电解质A的稀盐酸为电解质溶液,它不仅能提供电能,还能起到固氮作用.下列对该电池的说法不正确的是( )
如图是一种新型燃料电池装置示意图,该电池以溶有电解质A的稀盐酸为电解质溶液,它不仅能提供电能,还能起到固氮作用.下列对该电池的说法不正确的是( )| A. | 通入H2的电极为负极,A为NH4Cl | |
| B. | 每转移0.1mol电子,消耗1.12L H2 | |
| C. | 溶液中H+向通入N2的一极移动,Cl-向通入H2的一极移动 | |
| D. | 通入N2的电极发生的电极反应式为N2+6e-+8H+═2NH4+ |
 .
.
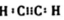 .
.