题目内容
16.设反应C+CO2?2CO△H>0,反应速率为v1;平衡常数为K1;N2+3H2?2NH3 △H<0,反应速率为v2,平衡常数为K2.对于上述反应,当温度升高时,v1、v2、K1、K2的变化情况为( )| A. | v1、v2、K1、K2同时增大 | B. | v1、v2、K1、K2同时减小 | ||
| C. | v1、v2增大,K1增大,K2减小 | D. | v2减小,v1增大,K1增大,K2减小 |
分析 化学反应无论是吸热反应还是放热反应,温度升高,化学反应速率都增大,正逆反应速率都增大,升温平衡向吸热反应方向进行,平衡常数随温度变化.
解答 解:反应C+CO2?2CO△H>0,反应速率为v1,平衡常数为K1,对此反应升温,反应速率v1增大,正反应是吸热反应,升温平衡正反应方向进行,平衡常数K1增大;
N2+3H2?2NH3 △H<0,反应速率为v2,平衡常数为K2,对于此反应,当温度升高时,反应速率v2增大,正反应为放热反应,升温平衡逆反应方向进行,平衡常数K2减小,综上所述,v1、v2增大,K1增大,K2减小,C正确,
故选C.
点评 本题考查了影响化学反应速率和化学平衡常数的因素分析,化学平衡移动原理的理解应用,注意平衡常数随温度变化,题目较简单.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
6.常温下,某溶液中由水电离的[H+]和[OH-]的乘积为1.0×10-22 mol2•L-2,则在该溶液中一定不能大量共存的离子组是( )
| A. | Al3+、Na+、NO3-、Cl- | B. | K+、Na+、Cl-、CO32- | ||
| C. | NH4+、Na+、Cl-、SO42- | D. | NH4+、K+、SiO32-、NO3- |
7.下列物质反应时,反应物用量或反应条件的改变对生成物无影响的是( )
| A. | C和O2 | B. | Na2CO3和盐酸 | C. | Na和O2 | D. | NaHCO3和NaOH |
11.下列有关物质的性质与应用不相对应的是( )
| A. | 氮气化学性质不活泼,可用作食品防腐剂 | |
| B. | 硅胶无毒、无味、无腐蚀性,可用作食品干燥剂 | |
| C. | SiO2、Al2O3、MgO都有很高的熔点,可以制耐火材料 | |
| D. | 二氧化锰具有强氧化性,可用作H2O2分解的氧化剂 |
1.某溶液中可能存在Fe3+、Fe2+、I-、HCO${\;}_{3}^{-}$、Cl-、NO${\;}_{3}^{-}$六种离子中的几种.进行下列实验:
①取少量溶液滴加KSCN溶液,溶液呈红色;
②另取少量原溶液滴加盐酸,溶液的棕黄色加深.
据此可以推断,该溶液中一定大量存在的阴离子是( )
①取少量溶液滴加KSCN溶液,溶液呈红色;
②另取少量原溶液滴加盐酸,溶液的棕黄色加深.
据此可以推断,该溶液中一定大量存在的阴离子是( )
| A. | I- | B. | HCO${\;}_{3}^{-}$ | C. | Cl- | D. | NO${\;}_{3}^{-}$ |
8.某恒容密闭容器中充入一定量SO2和O2进行反应:2SO2(g)+O2(g)?2SO3(g)△H<0,反应速率(v)与温度(T)、SO2的体积分数[V(SO2)%]与压强(p)的关系分别如图甲、图乙所示.下列说法正确的是( )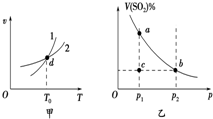

| A. | 图甲中,曲线1表示正反应速率和温度的关系,曲线2表示逆反应速率与温度的关系 | |
| B. | 图乙中,温度恒定时,a、b两点对应的反应速率:va>vb | |
| C. | 图甲中,d点表示温度为T0时,反应已经达到平衡 | |
| D. | 图乙中,温度恒定时,c点的反应正在向正反应方向进行 |
6.爱迪生电池在充电和放电时发生的反应:Fe+NiO2+2H2O?Fe(OH)2+Ni(OH)2,下列该蓄电池推断不正确的是( )
| A. | 放电时,Fe参与负极反应,NiO2参与正极反应 | |
| B. | 充电时,阴极上的电极反应式为:Fe(OH)2+2e-═Fe+2OH- | |
| C. | 蓄电池的电极必须浸入某种碱性电解质溶液中 | |
| D. | 放电时,电解质溶液中的阴离子向正极方向移动 |