题目内容
5.铝热反应是铝的一个重要性质.某校化学兴趣小组同学为了克服传统铝热反应纸漏斗易燃烧,火星四射等缺点,将实脸改成以下装置,取磁性氧化铁在如图A实验进行铝热反应,冷却后补到“铁块”混合物.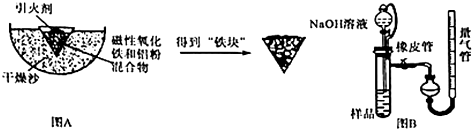
(1)实验中可以用蔗糖和浓硫酸代替镁条作引火剂,共原因是蔗糖在浓硫酸中脱水并放出大量的热.
(2)该铝热反应的化学方程式为8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe.
(3)取反应后的“铁块”研碎取样称量,加入如图B装置,滴入足量NaOH溶液充分反应,测量生成气体体积以测量样品中残留铝的百分含量.试回答下列问题:
①量气管的量具部分是一个中学实验常见量具改装而成,该仪器的名称为碱式滴定管.
②量气管在读数时必须进行的步骤是冷却至常温和调节量气管使左右液面相平.
③取1g样品进行上述实验,共收集到44.8mL气体(换算成标准状况下),则铝的百分含量为3.6%.
④装置中分液漏斗上端和烧瓶用橡胶管连通,除了可以平衡压强让液体顺利滴入试管之外,还可以起到降低实验误差的作用.如果装置没有橡胶管,测出铝的百分含量将会偏大(填“偏大”或“偏小”).
分析 (1)浓硫酸具有脱水性,并放出热;
(2)Al还原Fe3O4生成Fe和Al2O3,结合质量守恒定律分析;
(3)滴入足量NaOH溶液充分反应,测量生成气休体积以测量样品中残留铝的百分含量,由图可知,量气管测定氢气的体积,读数时调节内外液面相平,可利用滴定管代替量气管,结合2Al+2NaOH+2H2O=2NaAlO2+3H2↑计算含量,如果装置没有橡胶管,烧瓶内压强增大,造成气体读数偏大,以此来解答.
解答 解:(1)因为把浓硫酸加入到蔗糖中发生脱水并放出大量的热,可作引火剂,故答案为:蔗糖在浓硫酸中脱水并放出大量的热;
(2)Al还原Fe3O4生成Fe和Al2O3,由原子守恒可得化学方程式为8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe,故答案为:8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe;
(3)滴入足量NaOH溶液充分反应,测量生成气休体积以测量样品中残留铝的百分含量,由图可知,量气管测定氢气的体积,
①因为该仪器盛放NaOH溶液,所以由碱式滴定管改装而成,故答案为:碱式滴定管;
②因为气体的体积受温度和压强影响,所以量气管在读数时必须进行的步骤是:冷却至常温和调节量气管使左右液面相平,故答案为:冷却至常温和调节量气管使左右液面相平;
③根据Al与NaOH溶液反应的化学方程式:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,m(Al)=n(Al)×27g/mol=$\frac{2}{3}$3n(H2)×27g/mol=$\frac{2}{3}$×0.0448L÷22.4L/mol×27g/mol=0.036g,则铝的百分含量为$\frac{0.036g}{1g}$×100%=3.6%,故答案为:3.6%;
④如果装置没有橡胶管,烧瓶内压强增大,造成气体读数偏大,则铝的百分含量将会偏大,故答案为:偏大.
点评 本题以铝热反应为载体考查物质含量测定,为高频考点,把握反应原理、气体的测定装置为解答的关键,侧重分析与计算、实验能力的综合考查,题目难度不大.

| A. | 常温常压下,16 g O3中含有质子总数为8NA | |
| B. | 25℃时,1 mL纯水中含有OH-离子数目为10-10 | |
| C. | pH=2的醋酸稀释10倍后,溶液中H+数目大于0.001NA | |
| D. | 1molCl2与足量NaOH溶液反应,转移的电子数为2NA |
| A. | Fe的基态原子外围电子排布图: | |
| B. | 氯化钠的分子式:NaCl | |
| C. | N的基态原子核外电子排布式:lS22S22p3 | |
| D. | HC10的结构式:H-O-Cl |
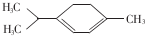 青蒿素是抗疟特效药属于萜类化合物,如图所示有机物也属于萜类化合物,该有机物的一氯取代物有(不含立体异构)( )
青蒿素是抗疟特效药属于萜类化合物,如图所示有机物也属于萜类化合物,该有机物的一氯取代物有(不含立体异构)( )| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
| A. | 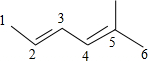 :5-甲基-2,4-己二烯 :5-甲基-2,4-己二烯 | B. |  1,2,3,4-四甲基环己烷 1,2,3,4-四甲基环己烷 | ||
| C. |  :1,3,4-三甲基苯 :1,3,4-三甲基苯 | D. | 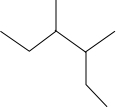 :3-甲基-2-乙基戊烷 :3-甲基-2-乙基戊烷 |
CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.0kJ•mol-1
该反应在工业上被称为“一氧化碳变换”.
(1)写出该反应的平衡常数表达式:K=$\frac{c(C{O}_{2})•c({H}_{2})}{c(CO)•c({H}_{2}O)}$.
K(200℃)>K(300℃)(填“>”、“=”或“<”).
(2)恒温恒容条件下,以下能说明该反应达到平衡状态的是a(填字母序号).
a.ν消耗(CO)=ν生成(H2O) b.c(CO2)=c(CO)
c.混合气体的总物质的量不再改变 d.混合气体的密度不再改变
(3)某温度下,在一个容积为10L的密闭容器中加入1mol CO和4mol H2O(g),反应经20min后达到平衡,测得平衡时CO2的物质的量为0.8mol,该时间范围内反应的平均速率ν (CO )=0.004mol•L-1•min-1;平衡常数K的数值为1.
(4)某工业合成氨的原料气组成为:H2 40%、N2 20%、CO 30%、CO210%(均为体积分数).现采用“一氧化碳变换”法,向上述原料气中加入水蒸气,将其中的CO除去.已知不同温度及反应物投料比($\frac{n({H}_{2}O)}{n(CO)}$)下,变换后平衡混合气体中CO的体积分数如下表所示:
| 投料比 CO的体积分数% 温度/℃ | $\frac{n({H}_{2}O)}{n(CO)}$=1 | $\frac{n({H}_{2}O)}{n(CO)}$=3 | $\frac{n({H}_{2}O)}{n(CO)}$=5 |
| 200 250 300 350 | 1.70 2.73 6.00 7.85 | 0.21 0.30 0.84 1.52 | 0.02 0.06 0.43 0.80 |
②温度是一氧化碳变换工艺中最重要的工艺条件,实际生产过程中将温度控制在300℃左右,其原因是提高温度,会提高反应速率,但平衡逆向移动,CO的转化率下降,实际生产过程中应该综合考虑速率和平衡两个方面.
| A. | 0.125 | B. | 0.10 | C. | 0.08 | D. | 0.20 |