题目内容
16.常温下,下列有关电解质溶液叙述错误的是( )| A. | 某H2S04溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1.0×l0-8,由水电离出的c(H+)=1×10-11 mol•L-1 | |
| B. | 将0.02 mol.L-1 HCI溶液与0.02 mol•L-l Ba( OH)2溶液等体积混合后,溶液pH约为12 | |
| C. | 将一定体积稀盐酸与稀氨水混合,当溶质为NH3•H20和NH4Cl时,溶液的pH≥7 | |
| D. | 向0.1 mol•L-1 Na2C03溶液中逐滴滴加0.1 mol•L-1稀盐酸,溶液中c(HCO3-)先增大后减小 |
分析 A、某H2S04溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1.0×l0-8,结合水的离子积可知,c(H+)和c(OH-),而硫酸中的氢氧根全部来自于水的电离;
B、将0.02 mol.L-1 HCI溶液与0.02 mol•L-l Ba( OH)2溶液等体积混合后,氢氧化钡过量,根据c(OH-)来计算;
C、将一定体积稀盐酸与稀氨水混合,当溶质为NH3•H20和NH4Cl时,NH3•H20和NH4Cl的量的相对多少决定溶液显什么性;
D、向0.1 mol•L-1 Na2C03溶液中逐滴滴加0.1 mol•L-1稀盐酸,盐酸先和Na2C03反应生成NaHC03,然后盐酸再和NaHC03反应生成二氧化碳.
解答 解:A、某H2S04溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1.0×l0-8,结合水的离子积c(H+)•c(OH-)=10-14,可解得c(H+)=10-3mol/L,c(OH-)=10-11mol/L,硫酸中的氢氧根全部来自于水的电离,而水电离出的氢离子浓度等于其电离出的氢氧根的浓度,故溶液中水电离出的c(H+)=1×10-11 mol•L-1,故A正确;
B、将0.02 mol.L-1 HCI溶液与0.02 mol•L-l Ba( OH)2溶液等体积混合后,氢氧化钡过量,溶液中的c(OH-)=$\frac{0.04mol/L×VL-0.02mol/L×VL}{2VL}$=0.01mol/L,则c(H+)=10-12mol/L,故pH=12,故B正确;
C、将一定体积稀盐酸与稀氨水混合,当溶质为NH3•H20和NH4Cl时,NH3•H20和NH4Cl的量的相对多少决定溶液显什么性,当NH3•H20和NH4Cl的量差不多时,溶液显碱性,当NH3•H20比NH4Cl少时,溶液可能显中性,当NH3•H20比NH4Cl少很多时,溶液可能选酸性,故C错误;
D、向0.1 mol•L-1 Na2C03溶液中逐滴滴加0.1 mol•L-1稀盐酸,盐酸先和Na2C03反应生成NaHC03,然后盐酸再和NaHC03反应生成二氧化碳,故溶液中c(HCO3-)先增大后减小,故D正确.
故选C.
点评 本题考查了酸碱混合后溶液pH的计算和盐类的水解,难度不大,应注意的是NH3•H20和NH4Cl的量的相对多少决定溶液显什么性.

| A. | 白醋中滴入石蕊溶液呈红色 | |
| B. | 白醋加入豆浆中有沉淀产生 | |
| C. | 蛋壳浸泡在白醋中有气体放出 | |
| D. | 测得白醋溶液中的c(H+)在1×10-2 mol•L-1到1×10-3 mol•L-1之间 |
| A. | +2 | B. | +3 | C. | +6 | D. | +7 |
 某溶液可能含有如表离子
某溶液可能含有如表离子| 阳离子 | H+、K+、Al3+、NH4+、Mg2+ |
| 阴离子 | SO42-、OH- |
提示:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3+H2O
请回答下列问题:
(1)产生的气体是NH3和O2.
(2)上述溶液中一定存在的离子是H+、Al3+、NH4+、Mg2+、SO42-.图中横坐标字母c=9mol.
(3)加Na2O2固体到bmol时所得沉淀的化学式Mg(OH)2和Al(OH)3.
(4)用离子方程式表示加Na2O2固体到amol前没有出现沉淀的原因2Na2O2+4H+=4Na+2H2O+O2↑.
(5)检验溶液中还可能大量含有的离子,其具体操作是用铂丝蘸蘸取溶液在无色火焰上灼烧,透过蓝色钴玻璃观察火焰颜色,若呈紫色,则证明有K+,反之,则证明没有K+.
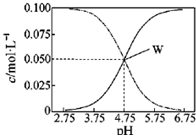 25℃,有c(CH3COOH)+c(CH3COO-)=0.l mol/L的一组醋酸和醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示.有关离子浓度关系分析正确的是( )
25℃,有c(CH3COOH)+c(CH3COO-)=0.l mol/L的一组醋酸和醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示.有关离子浓度关系分析正确的是( )| A. | pH=5.5溶液中:c(CH3COO->c(CH3COOH)>c(H+)>c(OH一) | |
| B. | W点表示溶液中:c(Na+)=c(CH3COO-) | |
| C. | pH=3.5溶液中:c(Na+)-c(OH-)+c(CH3COOH)=0.l moL/L | |
| D. | 向W点所表示溶液中通入0.05molHCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH)+c(OH-) |
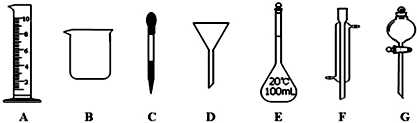
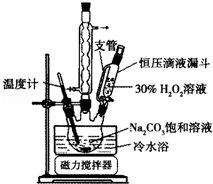 2Na2CO3•3H2O2是一种新型的氧系漂白剂.某实验兴趣小组进行了如下实验.
2Na2CO3•3H2O2是一种新型的氧系漂白剂.某实验兴趣小组进行了如下实验.