题目内容
3.体积相同的甲、乙两个容器中,分别都充有等物质的量的SO3,在相同温度下发生反应:2SO3(g)?2SO2(g)+O2(g),并达到平衡.在这个过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO3的转化率为p%,则乙容器中SO3的转化率( )| A. | 等于p% | B. | 大于p% | C. | 小于p | D. | 无法判断 |
分析 先假定甲、乙的体积都不变,达到平衡后再保持乙的压强不变,此反应是气体体积增大的反应,因此,待等体积达平衡后,欲保持乙的压强不变,就需要增大体积.增大体积则乙的压强减小,平衡向气体体积增大的方向进行,平衡正向移动.
解答 解:先假定甲、乙的体积都不变,达到平衡后再保持乙的压强不变,此反应是气体体积增大的反应,因此,待等体积达平衡后,欲保持乙的压强不变,就需要增大体积.增大体积则乙的压强减小,平衡向气体体积增大的方向进行,平衡正向移动,所以,若甲容器中SO2的转化率为P%,则乙的SO3的转化率将大于甲的,即大于P%.
故选B.
点评 本题考查了化学平衡的建立,恒温恒容容器和恒温恒压容器的应用条件,这一类问题的解决方法一般如此,先设为同等条件,平衡后再改变某一条件使之符合题设条件,分析变化.这样,问题就迎刃可解了,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.常温下,下列有关电解质溶液叙述错误的是( )
| A. | 某H2S04溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1.0×l0-8,由水电离出的c(H+)=1×10-11 mol•L-1 | |
| B. | 将0.02 mol.L-1 HCI溶液与0.02 mol•L-l Ba( OH)2溶液等体积混合后,溶液pH约为12 | |
| C. | 将一定体积稀盐酸与稀氨水混合,当溶质为NH3•H20和NH4Cl时,溶液的pH≥7 | |
| D. | 向0.1 mol•L-1 Na2C03溶液中逐滴滴加0.1 mol•L-1稀盐酸,溶液中c(HCO3-)先增大后减小 |
17.某无色混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种气体.现将此混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色.对于原混合气体成份的判断正确的是( )
| A. | 肯定含有SO2和NO | B. | 肯定含有NO和O2 | ||
| C. | 可能有Cl2 | D. | 肯定没有Cl2、NO2,可能有O2 |
14.向含等物质的量浓度的FeI2、FeBr2混合溶液中通人适量氯气,下列离子反应一定不正确的是( )
| A. | 4Fe2++2I-+3Cl2═4Fe3++I2+6Cl- | |
| B. | 2I-+Cl2═2Cl-+I2 | |
| C. | 2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- | |
| D. | 2Fe2++2I-+2Br-+3Cl2═2Fe3++I2+Br2+6Cl- |
1.下列不属于有机物的原子成键特点的是( )
| A. | 碳原子易失去最外层的电子形成离子 | |
| B. | 碳原子最外层电子易于其他原子的外层电子形成共同电子对 | |
| C. | 组成有机物的碳原子可以形成单键、双键和三键等多种成键形式 | |
| D. | 组成有机物的氧原子、氮原子、卤素原子分别形成2个、3个、1个共价键 |
12.A、B、C、D为可溶于水的四种固体,B的水溶液呈浅绿色,D为含氧酸盐,组成它们的离子有:
Ⅰ.将四种固体溶于水,分别取它们的水溶液进行实验,结果如下:
(1)A溶液的颜色反应为黄色,则A溶液中含有的金属离子是Na+(填离子序号).
(2)将A的水溶液逐滴加入C中,先生成白色沉淀,后白色沉淀逐渐溶解,请写出白色沉淀逐渐溶解的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
(3)B溶液与D溶液反应生成不溶于稀硝酸的白色沉淀,请写出该反应的离子方程式Ba2++SO42-=BaSO4↓.
Ⅱ.(4)据此推断它们是(写化学式)ANaOH;DBa(NO3
)2.
(5)A溶液与B溶液反应的现象为先生成白色絮状沉淀,然后变为灰绿色,最后变为红褐色.
| 阳离子 | Fe2+、Na+、Ba2+、Al3+ |
| 阴离子 | Cl-、SO42-、NO3-、OH- |
(1)A溶液的颜色反应为黄色,则A溶液中含有的金属离子是Na+(填离子序号).
(2)将A的水溶液逐滴加入C中,先生成白色沉淀,后白色沉淀逐渐溶解,请写出白色沉淀逐渐溶解的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
(3)B溶液与D溶液反应生成不溶于稀硝酸的白色沉淀,请写出该反应的离子方程式Ba2++SO42-=BaSO4↓.
Ⅱ.(4)据此推断它们是(写化学式)ANaOH;DBa(NO3
)2.
(5)A溶液与B溶液反应的现象为先生成白色絮状沉淀,然后变为灰绿色,最后变为红褐色.
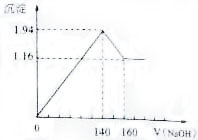 将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为0.5 mol/L的NaOH溶液,生成的沉淀质量跟加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)求:(1)合金中Mg,Al的质量;
将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为0.5 mol/L的NaOH溶液,生成的沉淀质量跟加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)求:(1)合金中Mg,Al的质量;