题目内容
6.实验是化学研究的一种重要手段,现有下图所示A~G七种仪器,请根据要求填空.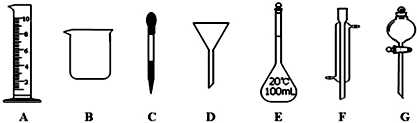
(1)写出仪器名称:C胶头滴管,G分液漏斗
(2)下列实验操作中用到仪器G的是b(选填下列选项的编号字母).
a.分离水和酒精的混合物
b.分离水和苯的混合物
c.分离水和泥砂的混合物
(3)实验室配制95mL 0.5mol/L的盐酸溶液.
①下列关于仪器E的使用方法中,正确的是d(选填下列选项的编号字母).
a.使用前不用检查是否漏液 b.使用前不必烘干
c.能用作物质反应或溶解的容器 d.热溶液不可直接转移到容量瓶中
②需要10mol/L的浓盐酸5.0mL.取用该体积盐酸时,需要用到上述仪器中的A和C(选填仪器的编号字母).
分析 (1)根据仪器的外形来分析;
(2)仪器G是分液漏斗,用于分液;
(3)①容量瓶在使用前要检查是否漏液,只能用于溶液的配制,不能用于溶解固体、稀释溶液和做反应容器;
②根据溶液稀释定律C浓V浓=C稀V稀来计算,取用一定体积的溶液用胶头滴管和量筒.
解答 解:(1)根据仪器的外形可知,C为胶头滴管,G为分液漏斗,故答案为:胶头滴管,分液漏斗;
(2)仪器G是分液漏斗,用于分液,即用于分离互不相溶的液体混合物,故选b;
(3)①a.容量瓶在使用前要检查是否漏液,故a错误;
b.使用前不必烘干,容量瓶中有水对浓度无影响,故b错误;
c.容量瓶不能受热,故不能用作物质反应或溶解的容器,故c错误;
d.容量瓶不能受热,故热溶液不可直接转移到容量瓶中,故d正确.
故选d.
②由于实验室无95mL容量瓶,故应选用100mL容量瓶,配制出100mL溶液,设需要的浓盐酸的体积为VmL,根据溶液稀释定律C浓V浓=C稀V稀可知:10mol/L×VmL=0.5mol/L×100mL,解得V=5.0mL,而取用一定体积的溶液所用的仪器为胶头滴管和量筒,故答案为:5.0,C.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和仪器的使用,属于基础型题目,难度不大.

练习册系列答案
相关题目
17.下列离子方程式正确的是( )
| A. | 向NaHSO4溶液中滴加Ba(OH)2溶液至中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| B. | 向饱和Na2CO3溶液中通入足量CO2:2Na++CO32-+CO2+H2O═2NaHCO3↓ | |
| C. | 向Ca(HCO3)2溶液中加入足量Ca(OH)2溶液:Ca2++HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| D. | 向次氯酸溶液中滴加NaOH溶液:H++OH-═H2O |
14.某混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种气体.现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色.对于原混合气体成分的判断中正确的是( )
| A. | 肯定有SO2、NO、O2 | B. | 肯定没有C12、O2和NO2 | ||
| C. | 可能有Cl2和O2 | D. | 肯定只有NO |
11.有A、B、C、D四种强电解质,它们在水中电离产生下列离子(每种物质只含一种阴离子且互不重复).
已知:①A、C溶液的pH均大于7,四种物质的溶液中只有A、B的溶液中水的电离程度均大于纯水的电离程度;②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无现象.
(1)A是CH3COONa,B是NH4Cl(填化学式).
(2)写出C和D反应的离子方程式Ba2++SO42-=BaSO4↓.
(3)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序是c(OH-)>c(Ba2+)=c(Cl-)>c(NH4+)>c(H+).
(4)在一定体积的0.005mol•L-1的C溶液中,加入一定体积的0.00125mol•L-1的盐酸,混合溶液的pH=11,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是1:4.
| 阳离子 | Na+、Ba2+、NH4+ |
| 阴离子 | CH3COO-、OH-、Cl-、SO42- |
(1)A是CH3COONa,B是NH4Cl(填化学式).
(2)写出C和D反应的离子方程式Ba2++SO42-=BaSO4↓.
(3)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序是c(OH-)>c(Ba2+)=c(Cl-)>c(NH4+)>c(H+).
(4)在一定体积的0.005mol•L-1的C溶液中,加入一定体积的0.00125mol•L-1的盐酸,混合溶液的pH=11,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是1:4.
15.不能作为判断硫、氯两种元素非金属性强弱的依据是( )
| A. | 单质氧化性的强弱 | |
| B. | 最高价氧化物对应的水化物酸性的强弱 | |
| C. | 单质沸点的高低 | |
| D. | 单质与氢气化合的难易 |
16.常温下,下列有关电解质溶液叙述错误的是( )
| A. | 某H2S04溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1.0×l0-8,由水电离出的c(H+)=1×10-11 mol•L-1 | |
| B. | 将0.02 mol.L-1 HCI溶液与0.02 mol•L-l Ba( OH)2溶液等体积混合后,溶液pH约为12 | |
| C. | 将一定体积稀盐酸与稀氨水混合,当溶质为NH3•H20和NH4Cl时,溶液的pH≥7 | |
| D. | 向0.1 mol•L-1 Na2C03溶液中逐滴滴加0.1 mol•L-1稀盐酸,溶液中c(HCO3-)先增大后减小 |