��Ŀ����
12������һ����Ҫ�ĺϽ�Ԫ�أ������ڴ��������͵�أ��Ӻ���������������SiO2��Al2O3����������������ȡ����һ���¹�����Ҫ������ͼ1��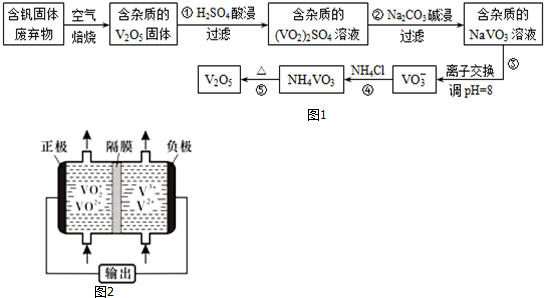
���ֺ�����������ˮ�е��ܽ������±���
| ���� | V2O5 | NH4VO3 | VOSO4 | ��VO2��2SO4 |
| �ܽ��� | ���� | ���� | ���� | ���� |
��1����Ӧ��������Һ�г�H+֮�����������VO2+��Al3+��
��2����Ӧ�ڼ�����˳��Ĺ�����Ҫ�ɷ���Al��OH��3��д��ѧʽ����
��3����Ӧ�ܵ����ӷ���ʽΪVO3-+NH4+=NH4VO3����
��4��25�桢101 kPaʱ��4Al��s��+3O2��g���T2Al2O3��s����H1=-a kJ/mol
4V��s��+5O2��g���T2V2O5��s����H2=-b kJ/mol
��V2O5�������ȷ�Ӧұ�����������Ȼ�ѧ����ʽ��10Al��s��+3V2O5��s��=5Al2O3��s��+6V��s����H=-$\frac{5a-3b}{2}$kJ/mol��
��5����Һ����أ���ͼ2��ʾ�����й�����Ӧ��������г�ǰ�����õ���и�Ĥֻ����H+ͨ������طŵ�ʱ�����ĵ缫��ӦʽΪV2+-e-=V3+����س��ʱ�����ĵ缫��Ӧʽ��VO2+-e-+H2O=VO2++2H+��
��6���������ữ��H2C2O4��Һ�ζ���VO2��2SO4��Һ���Բⶨ��Ӧ�ٺ���Һ�еĺ���������Ӧ�����ӷ���ʽΪ��2VO2++H2C2O4+2H+�T2VO2++2CO2��+2H2O��ȡ25.00mL 0.1000 mol/L
H2C2O4����Һ����ƿ�У�����ָʾ����������Һʢ���ڵζ����У��ζ����յ�ʱ���Ĵ���Һ24.0mL���ɴ˿�֪���ã�VO2��2SO4��Һ�з��ĺ���Ϊ10.6g/L��
���� ��Ӧ���������ܽ⺬��������������SiO2��Al2O3�����������������ɣ�VO2��2SO4����������SiO2�Ȳ��������ʹ��˳�ȥ����Ӧ������̼������Һ�루VO2��2SO4����������Ӧ���루VO2��2SO4��Ӧ����NaVO3��̼���������������ˮ����ٽ�����Al��OH��3��������Ӧ����NaVO3��Һ���Ȼ�立�Ӧ����NH4VO3����������NH4VO3�ֽ�ΪV2O5���ݴ˽��1����2����3����
��4������֪�Ȼ�ѧ����ʽ�ʹ����Ȼ�ѧ����ʽ�����ø�˹���ɼ��㣻
��5����Һ����طŵ�ʱ��������������Ӧ������������ԭ��Ӧ�����ʱ����������������Ӧ��
��6���Ⱦݷ�Ӧ����ʽ�͵ζ����ݼ��㣨VO2��2SO4��Һ��c��VO2+�������ʵ���Ũ�ȣ��ټ���ã�VO2��2SO4��Һ�з��ĺ�����
��� �⣺��Ӧ���������ܽ⺬��������������SiO2��Al2O3�����������������ɣ�VO2��2SO4����������SiO2�Ȳ��������ʹ��˳�ȥ����Ӧ������̼������Һ�루VO2��2SO4����������Ӧ���루VO2��2SO4��Ӧ����NaVO3��̼���������������ˮ����ٽ�����Al��OH��3��������Ӧ����NaVO3��Һ���Ȼ�立�Ӧ����NH4VO3����������NH4VO3�ֽ�ΪV2O5��
��1���������ܽ⺬��������������SiO2��Al2O3�����������������ɣ�VO2��2SO4������������Һ�е������ӳ����������VO2+��Al3+��
�ʴ�Ϊ��VO2+��Al3+��
��2�������ʵģ�VO2��2SO4��Һ��̼������Һ������ɺ����ʵ�NaVO3��Һ��Al��OH��3������������Է�Ӧ�ڼ�����˳��Ĺ�����Ҫ�ɷ���Al��OH��3��
�ʴ�Ϊ��Al��OH��3��
��3���ݹ�������ͼ��֪����Ӧ�ܵ����ӷ���ʽΪVO3-+NH4+=NH4VO3�����ʴ�Ϊ��VO3-+NH4+=NH4VO3����
��4����֪��4Al��s��+3O2��g���T2Al2O3��s����H1=-a kJ/mol
��4V��s��+5O2��g���T2V2O5��s����H2=-b kJ/mol
�ݸ�˹���ɣ����١�5-�ڡ�3����2�ã�10Al��s��+3V2O5��s��=5Al2O3��s��+6V��s����H=-$\frac{5a-3b}{2}$kJ/mol��
�ʴ�Ϊ��10Al��s��+3V2O5��s��=5Al2O3��s��+6V��s����H=-$\frac{5a-3b}{2}$kJ/mol��
��5����Һ����طŵ�ʱ��������������Ӧ����ͼ��֪���缫��ӦʽΪV2+-e-=V3+������������ԭ��Ӧ�����ʱ����������������Ӧ���缫��ӦʽΪVO2+-e-+H2O=VO2++2H+��
�ʴ�Ϊ��V2+-e-=V3+��VO2+-e-+H2O=VO2++2H+��
��6���ݵζ����ݣ�������ӷ���ʽc��VO2+��=$\frac{2��0.025L��0.100mol/L}{0.024L}$=0.2083mol/L������1L��Һ�к�V������Ϊ0.2083mol/L��1L��51g/mol=10.6g��
�ʴ�Ϊ��10.6��
���� ���⿼�����ʷ�����ᴿ��Ϊ��Ƶ���㣬�漰ԭ��غ͵���ԭ�����ζ�ʵ�鼰���㡢��˹���ɡ����ʷ�����ᴿ��֪ʶ�㣬��ȷʵ��ԭ�����������ʡ����������������ǽⱾ��ؼ����ѵ��Ƿ�������ͼ��ÿһ�����ܷ����ķ�Ӧ���������������ע���������Ϣ���������Ŀ�Ѷ��еȣ�

| ʵ����� | ʵ��Ŀ�� | |
| A | �ͱ��ӻ����Һ�еμӹ���Ũ��ˮ | ��ȥ�����Һ�еı��� |
| B | �����Һ�м��뱥��̼������Һ | �������ᡢ�����������Ҵ� |
| C | ��3mL5%CuSO4��Һ�еμ�3-4��1%����������Һ���������м���0.5mL��ȩ������ | ����ȩ�� |
| D | ��������������������Һ���ȣ���ȴ�������μ���������Һ | �����������е���Ԫ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | 4�֡�3�� | B�� | 3�֡�4�� | C�� | 6�֡�2�� | D�� | 2�֡�6�� |
| A�� | 4.4gCO2��N2O�ɵĻ�������к��е�������Ϊ2.2NA | |
| B�� | 7.8gNa2O2����������ĿΪ0.2NA | |
| C�� | 2L0.5mol•L-1��NH4��2SO4��Һ�к��е�NH4+������Ϊ2NA | |
| D�� | ��ѧ��Ӧ��ÿ����1molO2��ת�Ƶĵ�����һ����4NA |
| A�� | 1s22s22p5 | B�� | 1s22s22p2 | C�� | 1s22s22p63s1 | D�� | 1s22s22p63s2 |

