题目内容
用标准盐酸滴定未知浓度的NaOH溶液,如果测得结果偏低,则产生误差的原因可能是下列叙述中的( )
| A、滴定过程中,锥形瓶中有溶液溅出 |
| B、锥形瓶用蒸馏水洗净后,未经干燥即进行滴定 |
| C、酸式滴定管未用标准盐酸润洗 |
| D、滴定前酸式滴定管尖嘴部分有气泡,滴定终止时气泡消失 |
考点:中和滴定
专题:
分析:根据c(待测)=
分析不当操作对V(标准)的影响,以此判断浓度的误差.
| c(标准)×V(标准) |
| V(待测) |
解答:
解:A.滴定过程中,锥形瓶中有溶液溅出,待测液的物质的量偏小,造成V(标准)偏小,根据c(待测)=
分析,可知c(待测)偏小,故A正确;
B.锥形瓶用蒸馏水洗净后,未经干燥即进行滴定,待测液的物质的量不变,标准液的体积不变,根据c(待测)=
分析,可知c(待测)不变,故B错误;
C.酸式滴定管未用标准盐酸润洗,溶液被稀释,浓度偏小,造成V(标准)偏大,根据c(待测)=
分析,可知c(待测)偏大,故C错误;
D.滴定前酸式滴定管尖嘴部分有气泡,滴定终止时气泡消失,造成V(标准)偏大,根据c(待测)=
分析,可知c(待测)偏大,故D错误;
故选A.
| c(标准)×V(标准) |
| V(待测) |
B.锥形瓶用蒸馏水洗净后,未经干燥即进行滴定,待测液的物质的量不变,标准液的体积不变,根据c(待测)=
| c(标准)×V(标准) |
| V(待测) |
C.酸式滴定管未用标准盐酸润洗,溶液被稀释,浓度偏小,造成V(标准)偏大,根据c(待测)=
| c(标准)×V(标准) |
| V(待测) |
D.滴定前酸式滴定管尖嘴部分有气泡,滴定终止时气泡消失,造成V(标准)偏大,根据c(待测)=
| c(标准)×V(标准) |
| V(待测) |
故选A.
点评:本题主要考查了中和滴定操作的误差分析,根据c(待测)=
分析是解答的关键,题目难度不大.
| c(标准)×V(标准) |
| V(待测) |

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
设NA为阿伏加德罗常数,则下列说法正确的是( )
| A、1molNa2O2含有阴阳离子总数为4NA |
| B、0.1mol Fe与0.1mol Cl2充分反应,转移的电子数为0.3NA |
| C、常温常压,22.4L CO2中含有CO2分子NA个 |
| D、18 g水中含有的电子数为10NA |
下列气体属于温室效应气体的是( )
| A、CO2 |
| B、N2O |
| C、CH4 |
| D、N2 |
一定量的KClO3中加入浓盐酸发生如下反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,其中发生氧化反应的元素和发生还原反应的元素的质量之比为( )
| A、1:6 | B、6:1 |
| C、1:5 | D、5:1 |

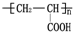 的单体,则A中所含官能团的名称是
的单体,则A中所含官能团的名称是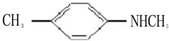 、
、