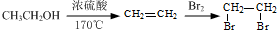题目内容
已知A为常见金属,X、Y为常见非金属,X、E、F、G常温下为气体,C为液体,B是一种盐,受热极易分解,在工农业生产中用途较广(如被用作某些干电池的电解质).现用A与石墨作电极,B的浓溶液作电解质,构成原电池.有关物质之间的转化关系如图:
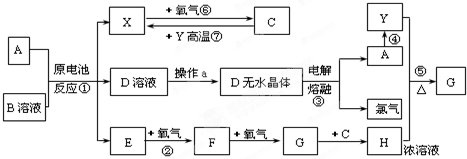
(注意:其中有些反应的条件及部分生成物被略去)请填写下列空白:
(1)反应④为A在某种气体中燃烧,生成单质Y和A的氧化物,其反应方程式为: .
(2)从D溶液制备D的无水晶体的“操作a”为 .
(3)反应②方程式 .
(4)反应③方程式 .如果以惰性电极电解D的水溶液,写出电解的总反应式
(5)反应⑤方程式 .

(注意:其中有些反应的条件及部分生成物被略去)请填写下列空白:
(1)反应④为A在某种气体中燃烧,生成单质Y和A的氧化物,其反应方程式为:
(2)从D溶液制备D的无水晶体的“操作a”为
(3)反应②方程式
(4)反应③方程式
(5)反应⑤方程式
考点:无机物的推断
专题:
分析:本题的突破口有两个:一是C为液体,由气体X(X由原电池反应得到,可能是H2)和氧气反应得到,故C应是H2O,X是H2,根据反应⑦可知Y是非金属C.二是E→F→G→H,属于常温下气体E的连续氧化得到气体G,在中学阶段可推出E为NH3、F为NO、G为NO2,则H为HNO3.再由反应⑤可验证G是NO2,由反应④进一步推出A为Mg,则D为MgCl2,结合反应①可推知B为NH4Cl,据此解答.
解答:
解:本题的突破口有两个:一是C为液体,由气体X(X由原电池反应得到,可能是H2)和氧气反应得到,故C应是H2O,X是H2,根据反应⑦可知Y是非金属C.二是E→F→G→H,属于常温下气体E的连续氧化得到气体G,在中学阶段可推出E为NH3、F为NO、G为NO2,则H为HNO3.再由反应⑤可验证G是NO2,由反应④进一步推出A为Mg,则D为MgCl2,结合反应①可推知B为NH4Cl,
(1)反应④为Mg在CO2气体中燃烧,生成单质C和Mg的氧化物,其反应方程式为:2Mg+CO2
2MgO+C,故答案为:2Mg+CO2
2MgO+C;
(2)D为MgCl2,易水解,不能直接加热,要将MgCl2溶液在HCl气流中蒸干,故答案为:将MgCl2溶液在HCl气流中蒸干;
(3)反应②为NH3与O2的反应,方程式4NH3+5O2
NO+6H2O,故答案为:4NH3+5O2
NO+6H2O;
(4)反应③为电解熔融MgCl2的反应,方程式为MgCl2(熔融)
Mg+Cl2↑,惰性电极电解MgCl2的水溶液,生成氢气和氯气,电解方程式为MgCl2+2H2O
Mg(OH)2↓+H2↑+Cl2↑,故答案为:MgCl2(熔融)
Mg+Cl2↑;MgCl2+2H2O
Mg(OH)2↓+H2↑+Cl2↑;
(5)反应⑤为Cu和浓硝酸的反应,方程式为C+4HNO3(浓)
CO2↑+4NO2↑+2H2O,故答案为:C+4HNO3(浓)
CO2↑+4NO2↑+2H2O.
(1)反应④为Mg在CO2气体中燃烧,生成单质C和Mg的氧化物,其反应方程式为:2Mg+CO2
| ||
| ||
(2)D为MgCl2,易水解,不能直接加热,要将MgCl2溶液在HCl气流中蒸干,故答案为:将MgCl2溶液在HCl气流中蒸干;
(3)反应②为NH3与O2的反应,方程式4NH3+5O2
| ||
| △ |
| ||
| △ |
(4)反应③为电解熔融MgCl2的反应,方程式为MgCl2(熔融)
| ||
| ||
| ||
| ||
(5)反应⑤为Cu和浓硝酸的反应,方程式为C+4HNO3(浓)
| ||
| ||
点评:本题考查无机物的推断,侧重于学生的分析能力和元素化合物知识的综合运用的考查,为高考常见题型,注意把握题给信息,结合转化关系进行推断,难度中等.

练习册系列答案
相关题目
用标准盐酸滴定未知浓度的NaOH溶液,如果测得结果偏低,则产生误差的原因可能是下列叙述中的( )
| A、滴定过程中,锥形瓶中有溶液溅出 |
| B、锥形瓶用蒸馏水洗净后,未经干燥即进行滴定 |
| C、酸式滴定管未用标准盐酸润洗 |
| D、滴定前酸式滴定管尖嘴部分有气泡,滴定终止时气泡消失 |
用已知浓度的NaOH溶液滴定未知浓度的盐酸溶液,下列操作会使测定结果偏低的是( )
| A、滴定前对碱式滴定管仰视读数,滴定后又俯视 |
| B、滴定前锥形瓶内含有少量水 |
| C、滴定前,碱式滴定管尖嘴部分有气泡,滴定后气泡消失 |
| D、碱式滴定管用蒸馏水洗净后,直接装入已知浓度的NaOH溶液 |
右图是用0.1000mol/L的NaOH溶液滴定20.00mL未知浓度盐酸(酚酞作指示剂)的滴定曲线.下列说法正确的是( )
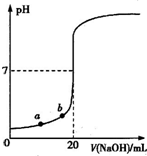

| A、水电离出的氢离子浓度:a>b |
| B、盐酸的物质的量浓度为0.0100mol?L-1 |
| C、指示剂变色时,说明盐酸与NaOH恰好完全反应 |
| D、当滴加NaOH溶液10.00mL时,该混合液的pH=1+lg3 |
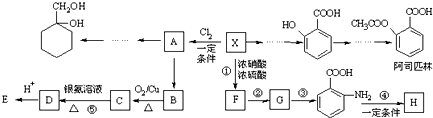
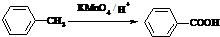
 (苯胺,易被氧化)
(苯胺,易被氧化)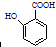 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有 和其他无机物合成
和其他无机物合成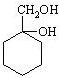 最合理的方案(不超过4步).
最合理的方案(不超过4步).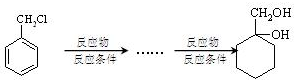
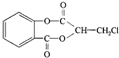 )在一定条件下可以发生如图所示的转化(其他产物和水已略去).
)在一定条件下可以发生如图所示的转化(其他产物和水已略去).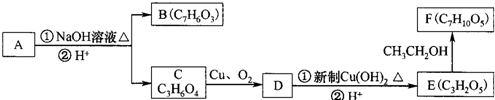
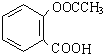 (即乙酰水杨酸,分子式 C9H8O4),满足以下条件的阿司匹林的同分异构体有
(即乙酰水杨酸,分子式 C9H8O4),满足以下条件的阿司匹林的同分异构体有 )经过几步有机反应制得,试写出以乳酸为主要原料制备有机物C的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2OH
)经过几步有机反应制得,试写出以乳酸为主要原料制备有机物C的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2OH 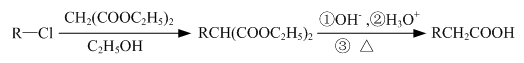
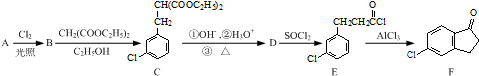
 的合成路线流程图(注明反应条件).合成路线流程图示例如下:
的合成路线流程图(注明反应条件).合成路线流程图示例如下: