题目内容
一定量的KClO3中加入浓盐酸发生如下反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,其中发生氧化反应的元素和发生还原反应的元素的质量之比为( )
| A、1:6 | B、6:1 |
| C、1:5 | D、5:1 |
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:在KClO3+6HCl=KCl+3Cl2↑+3H2O的反应中,根据化合价不交叉的原则,KClO3中+5价的氯元素降为0价,HCl中氯元素升为0价,氯化钾中的氯元素来自盐酸,所以KClO3是氧化剂、部分HCl是还原剂,氧化剂被还原、还原剂被氧化,据此分析解答.
解答:
解:根据化合价不交叉的原则,在KClO3+6HCl=KCl+3Cl2↑+3H2O的反应中,KClO3中+5价的氯元素降为0价,该氯原子为被还原的氯原子,HCl中氯元素升为0价,该氯原子为被氧化的氯原子,氯化钾中的氯元素来自盐酸,则被氧化发生氧化反应的Cl为5,
所以KClO3是氧化剂、部分HCl是还原剂,氧化剂被还原、还原剂被氧化,被氧化和被还原的元素都是Cl元素,其质量之比等于其物质的量之比=5:1,
故选D.
所以KClO3是氧化剂、部分HCl是还原剂,氧化剂被还原、还原剂被氧化,被氧化和被还原的元素都是Cl元素,其质量之比等于其物质的量之比=5:1,
故选D.
点评:本题考查了氧化还原反应的特征和有关的规律,要求学生具有分析和解决问题的能力,明确元素化合价是解本题关键,注意HCl部分作还原剂、部分起酸的作用,为易错点,题目难度不大.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
用标准盐酸滴定未知浓度的NaOH溶液,如果测得结果偏低,则产生误差的原因可能是下列叙述中的( )
| A、滴定过程中,锥形瓶中有溶液溅出 |
| B、锥形瓶用蒸馏水洗净后,未经干燥即进行滴定 |
| C、酸式滴定管未用标准盐酸润洗 |
| D、滴定前酸式滴定管尖嘴部分有气泡,滴定终止时气泡消失 |
检验小苏打粉末中是否有苏打的方法是( )
| A、溶于水,加Ca(OH)2溶液 |
| B、溶于水,加稀CaCl2溶液 |
| C、加稀盐酸 |
| D、溶于水,加入NaOH溶液 |
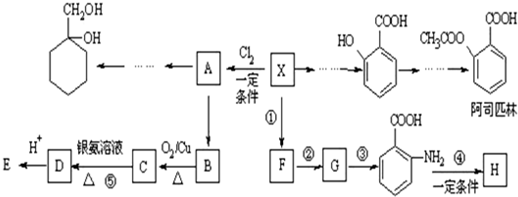
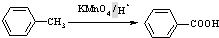
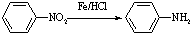 (苯胺,易被氧化)
(苯胺,易被氧化)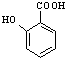 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有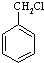 和其他无机物合成
和其他无机物合成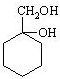 最合理的方案(不超过4步),请在答题纸的方框中表示.例:
最合理的方案(不超过4步),请在答题纸的方框中表示.例: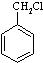
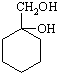
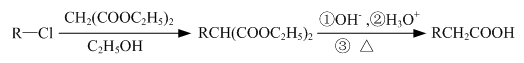
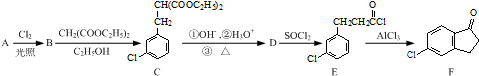
 的合成路线流程图(注明反应条件).合成路线流程图示例如下:
的合成路线流程图(注明反应条件).合成路线流程图示例如下: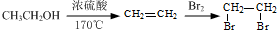
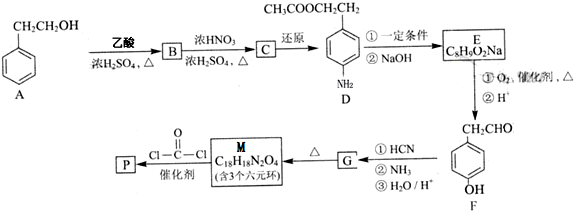
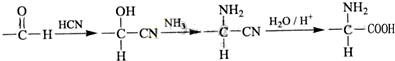
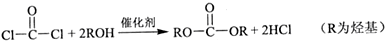

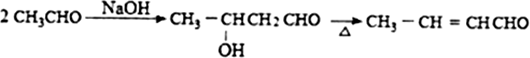
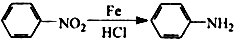 :苯胺中氨基易被氧化.
:苯胺中氨基易被氧化.