题目内容
17.下列实验中,无明显现象的是( )| A. | CO2通入CaCl2溶液中 | B. | NO2通入FeSO4溶液中 | ||
| C. | NH3通入A1C13溶液中 | D. | SO2通入Ba(NO3)2溶液中 |
分析 A.二氧化碳通入氯化钙溶液中不能发生反应;
B.二氧化氮具有氧化性,能氧化亚铁离子为铁离子;
C.氨气通入水溶液中生成一水合氨,一水合氨和铝离子结合生成氢氧化铝沉淀;
D.二氧化硫通入硝酸钡溶液中,二氧化硫和水反应生成酸,溶液中存在稀硝酸能氧化二氧化硫生成硫酸,硫酸和钡离子生成白色沉淀硫酸钡;
解答 解:A.碳酸酸性小于盐酸,二氧化碳通入氯化钙溶液中不发生反应,无明显现象,故A正确;
B.NO2通入FeSO4溶液中,二氧化氮和水反应生成硝酸和一氧化氮,硝酸具有强氧化性能氧化硫酸亚铁为硫酸铁,溶液颜色浅绿色变化为黄色,故B错误;
C.NH3通入A1C13溶液中发生反应生成氢氧化铝白色沉淀,Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故C错误;
D.SO2通入Ba(NO3)2溶液中,发生氧化还原反应生成白色的硫酸钡沉淀,故D错误;
故选A.
点评 本题考查了物质性质、反应现象、溶液中隐含离子的性质分析判断、掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
7.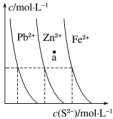 如图为某温度下,PbS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2-浓度、金属阳离子浓度变化情况.下列说法正确的是( )
如图为某温度下,PbS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2-浓度、金属阳离子浓度变化情况.下列说法正确的是( )
 如图为某温度下,PbS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2-浓度、金属阳离子浓度变化情况.下列说法正确的是( )
如图为某温度下,PbS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2-浓度、金属阳离子浓度变化情况.下列说法正确的是( )| A. | 三种难溶物的溶度积Ksp(FeS)的最小 | |
| B. | 如果向三种沉淀中加盐酸,最先溶解的是PbS | |
| C. | 向新生成的ZnS浊液中滴入足量含相同浓度的Pb2+、Fe2+的溶液,振荡后,ZnS沉淀会转化为PbS沉淀 | |
| D. | 对于三种难溶物来讲,a点对应的都是不饱和溶液 |
8.常温下,在溶液中可发生以下反应:
①H++Z-+XO42-→X2++Z2+H2O(未配平),
②2M2++R2═2M3++2R-
③2R-+Z2═R2+2Z-.
由此判断下列说法正确的是( )
①H++Z-+XO42-→X2++Z2+H2O(未配平),
②2M2++R2═2M3++2R-
③2R-+Z2═R2+2Z-.
由此判断下列说法正确的是( )
| A. | 氧化性强弱顺序为XO42->Z2>R2>M3+ | |
| B. | Z2在③中发生氧化反应 | |
| C. | R元素在反应②中被氧化,在③中被还原 | |
| D. | 常温下反应不可进行2M2++Z2═2M3++2Z- |
9.煤和煤制品(如水煤气、焦炭、甲醚等)已广泛应用于工农业生产中.
(1)已知:C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ.mol-l
CO2(g)+H2(g)=CO(g)+H2O(g)△H=+41.3kJ.mol-l
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为C(s)+2H2O(g)=CO2(g)+2H2(g)△H=+90.0kJ.mol-1,该反应在高温(填“高温”、“低温”或“任何温度”)下有利于正向自发进行.
(2)利用炭还原法可处理氮氧化物(如NO等),发生的反应为C(s)+2NO(g)?N2(g)+CO2 (g).向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得的各气体的浓度如表所示:
①10~20min内,N2的平均反应速率可v(N2)=0.009mol.L-l.min-l.
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是AD(填字母).
A.通入一定量的NO B.加入一定量的活性炭
C.加入合适的催化剂 D.遁当缩小容器的体积
(3)研究表明,反应CO(g)+H2O(g)?H2(g)+CO2(g)的平衡常数随温度的变化如表所示:
若反应在500℃时进行,设起始时CO和H2O的浓度均为0.020mol•L-l,在该条件下达到平衡时,CO的转化率为75%.
(1)已知:C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ.mol-l
CO2(g)+H2(g)=CO(g)+H2O(g)△H=+41.3kJ.mol-l
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为C(s)+2H2O(g)=CO2(g)+2H2(g)△H=+90.0kJ.mol-1,该反应在高温(填“高温”、“低温”或“任何温度”)下有利于正向自发进行.
(2)利用炭还原法可处理氮氧化物(如NO等),发生的反应为C(s)+2NO(g)?N2(g)+CO2 (g).向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得的各气体的浓度如表所示:
| 时间(min) 浓度(mol•L-1) 物质 | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是AD(填字母).
A.通入一定量的NO B.加入一定量的活性炭
C.加入合适的催化剂 D.遁当缩小容器的体积
(3)研究表明,反应CO(g)+H2O(g)?H2(g)+CO2(g)的平衡常数随温度的变化如表所示:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
6.如图是高温下某反应的微观过程.下列说法中正确的是( )


| A. | 该反应属于分解反应 | B. | 图中的两种化合物都属于氧化物 | ||
| C. | 该反应中元素的化合价没有变化 | D. | 反应前后原子的种类改变 |

 某化学兴趣小组用如图装置电解CuSO4溶液,测定铜的相对原子质量.
某化学兴趣小组用如图装置电解CuSO4溶液,测定铜的相对原子质量.