题目内容
8.常温下,在溶液中可发生以下反应:①H++Z-+XO42-→X2++Z2+H2O(未配平),
②2M2++R2═2M3++2R-
③2R-+Z2═R2+2Z-.
由此判断下列说法正确的是( )
| A. | 氧化性强弱顺序为XO42->Z2>R2>M3+ | |
| B. | Z2在③中发生氧化反应 | |
| C. | R元素在反应②中被氧化,在③中被还原 | |
| D. | 常温下反应不可进行2M2++Z2═2M3++2Z- |
分析 ①H++Z-+XO42-→X2++Z2+H2O,反应中XO4-是氧化剂,Z2是氧化产物,氧化性:XO4->Z2;
②2M2++R2═2M3++2R-,反应中R2是氧化剂,M3+是氧化产物,氧化性:R2>M3+;
③2R-+Z2═R2+2Z-,反应中Z2是氧化剂,R2是氧化产物,氧化性:Z2>R2;
所以氧化性强弱关系为:XO4->Z2>R2>M3+,以此解答该题.
解答 解:①H++Z-+XO42-→X2++Z2+H2O,反应中XO4-是氧化剂,Z2是氧化产物,氧化性:XO4->Z2;
②2M2++R2═2M3++2R-,反应中R2是氧化剂,M3+是氧化产物,氧化性:R2>M3+;
③2R-+Z2═R2+2Z-,反应中Z2是氧化剂,R2是氧化产物,氧化性:Z2>R2;
所以氧化性强弱关系为:XO4->Z2>R2>M3+,
A.所以氧化性强弱关系为:XO4->Z2>R2>M3+,故A正确;
B.③2R-+Z2═R2+2Z-,反应中Z2是氧化剂,发生还原反应,故B错误;
C.R元素在反应②中做氧化剂,被还原,在③中做还原剂,被氧化,故C错误;
D.反应2M2++Z2═2M3++2Z-中,Z2是氧化剂,M3+是氧化产物,氧化性Z2>M3+,符合题意,故D错误;
故选:A.
点评 本题考查了氧化性、还原性强弱比较,明确氧化还原反应强弱规律,准确判断氧化剂、氧化产物、还原剂、还原产物是解题关键,题目难度不大.

练习册系列答案
相关题目
18.工业上可利用煤的气化产物(CO和H2)合成二甲醚(CH3OCH3)同时生成二氧化碳,其三步反应如下:
①2H2(g)+CO(g)?CH3OH (g)△H=-90.8kJ•mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ•mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.3kJ•mol-1
(1)总合成反应的热化学方程式为3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-246.4kJ•mol.
(2)一定条件下的密闭容器中,上述总反应达到平衡时,要提高CO的转化率,可以采取的措施是CE(填字母代号).
A.高温高压 B.加入催化剂 C.减少CO2的浓度 D.增加CO的浓度 E.分离出二甲醚
(3)已知反应②2CH3OH(g)?CH3OCH3(g)+H2O(g)在某温度下的平衡常数K=400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如表格:
此时,v(正)> v(逆) 填“>”、“<”或“=”);达到平衡后,CH3OCH3的物质的量浓度是0.80mol/L.
①2H2(g)+CO(g)?CH3OH (g)△H=-90.8kJ•mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ•mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.3kJ•mol-1
(1)总合成反应的热化学方程式为3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-246.4kJ•mol.
(2)一定条件下的密闭容器中,上述总反应达到平衡时,要提高CO的转化率,可以采取的措施是CE(填字母代号).
A.高温高压 B.加入催化剂 C.减少CO2的浓度 D.增加CO的浓度 E.分离出二甲醚
(3)已知反应②2CH3OH(g)?CH3OCH3(g)+H2O(g)在某温度下的平衡常数K=400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如表格:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c/mol•L-1 | 0.44 | 0.60 | 0.60 |
16.第四届“绿发会”主题是“绿色发展让世界更美好”,下列行为不符合这一宗旨的是( )
| A. | 提高风能、太阳能等可再生清洁能源的使用比例 | |
| B. | 推广CO2再利用技术,将其合成有价值的化学品 | |
| C. | 利用工业废水灌溉农作物,提高水资源的利用率 | |
| D. | 研发煤炭的洁净、高效利用技术,保护生态环境 |
3.用标准浓度的盐酸来滴定锥形瓶中放置时间较长的氢氧化钠溶液,应选用的指示剂及滴定终点颜色变化的情况最好是( )
| A. | 石蕊,由蓝变红 | B. | 酚酞,红色褪去 | C. | 甲基橙,由黄变橙 | D. | 甲基橙,由橙变黄 |
20.向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生CuI白色沉淀,蓝色溶液变为棕色.再向反应后的溶液中通入过量的SO2气体,溶液变成无色.则下列说法正确的是( )
| A. | 通入22.4LSO2参加反应时,有2 NA个电子发生转移 | |
| B. | 上述实验条件下,物质的氧化性:Cu2+>I2>SO2 | |
| C. | 滴加KI溶液时,KI被氧化,CuI是氧化产物 | |
| D. | 通入SO2后溶液逐渐变成无色,体现了SO2的漂白性 |
17.下列实验中,无明显现象的是( )
| A. | CO2通入CaCl2溶液中 | B. | NO2通入FeSO4溶液中 | ||
| C. | NH3通入A1C13溶液中 | D. | SO2通入Ba(NO3)2溶液中 |
18.不同温度下水的离子积常数如表所示:
①请用文字解释随温度升高水的离子积增大的原因:水电离吸热,升高温度后平衡正向移动
②25℃条件下,pH=4的盐酸溶液中由水电离出来的H+的浓度为1.0×10-10mol/L
③10℃时纯水的电离平衡常数为5.3×10-17.
| t/℃ | 0 | 10 | 20 | 25 | 40 | 50 | 100 |
| KW/10-14 | 0.114 | 0.292 | 0.681 | 1.00 | 2.92 | 5.47 | 55.0 |
②25℃条件下,pH=4的盐酸溶液中由水电离出来的H+的浓度为1.0×10-10mol/L
③10℃时纯水的电离平衡常数为5.3×10-17.
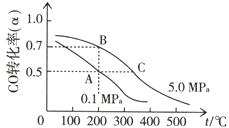 “洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了热值高达122500~16000kJ•m-3的煤炭气,其主要成分是CO和H2.CO和H2可作为能源和化工原料,应用十分广泛.
“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了热值高达122500~16000kJ•m-3的煤炭气,其主要成分是CO和H2.CO和H2可作为能源和化工原料,应用十分广泛.