题目内容
9.某溶液中大量存在NH4+、Fe2+、Br-、CO32-、AlO2-、S2-、SO32-七种离子中的几种.向该溶液中滴加足量氯水后,有气泡产生并生成橙色澄清溶液;向所得橙色溶液中加入BaCl2溶液时无沉淀生成.根据上述实验事实推断,在该溶液中能大量存在的离子组是( )| A. | NH4+、SO32-、AlO2- | B. | NH4+、Br-、CO32- | ||
| C. | Fe2+、S2-、SO32- | D. | NH4+、Br-、AlO2- |
分析 向该溶液中滴加足量氯水后,有气泡产生并生成橙色澄清溶液,则一定含CO32-、Br-,向所得橙色溶液中加入BaCl2溶液时无沉淀生成,则一定不含SO32-,结合离子的共存及电荷守恒来解答.
解答 解:向该溶液中滴加足量氯水后,有气泡产生并生成橙色澄清溶液,则一定含CO32-、Br-,一定不含S2-,由离子共存可知不含Fe2+,
向所得橙色溶液中加入BaCl2溶液时无沉淀生成,则一定不含SO32-,
由电荷守恒可知一定含阳离子为NH4+,且AlO2-、NH4+不能共存,
故选B.
点评 本题考查常见离子的检验,为高频考点,把握离子之间的反应与现象、电荷守恒为解答的关键,侧重分析与实验能力的考查,注意电荷守恒的应用,题目难度不大.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
17.化学反应 A2+B2═2AB 的能量变化如图所示,则下列说法正确的是( )
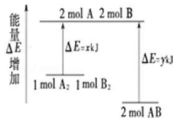

| A. | 该反应是吸热反应 | |
| B. | 断裂 1molA-A 键和 1mol B-B 键放出 xkJ 能量 | |
| C. | 断裂 2molA-B 键需要吸收 y kJ 的能量 | |
| D. | 1molA2和 1molB2 的总能量低于 2molAB 的总能量 |
19.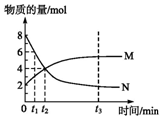 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确的是( )
 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确的是( )| A. | 化学方程式:2N?M | B. | t2时,正逆反应速率相等,达到平衡 | ||
| C. | t3时,正反应速率大于逆反应速率 | D. | t1时,M的浓度是N浓度的2倍 |
 .
. .
. .
. 、
、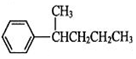 、
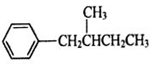
、
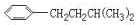 、
、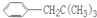 、
、 、
、 .
.