题目内容
17.化学反应 A2+B2═2AB 的能量变化如图所示,则下列说法正确的是( )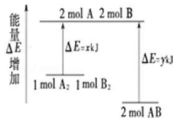
| A. | 该反应是吸热反应 | |
| B. | 断裂 1molA-A 键和 1mol B-B 键放出 xkJ 能量 | |
| C. | 断裂 2molA-B 键需要吸收 y kJ 的能量 | |
| D. | 1molA2和 1molB2 的总能量低于 2molAB 的总能量 |
分析 A.反应物的能量高于生成物的能量时,反应是放热反应;
B.旧键的断裂吸收能量,新键的形成释放能量;
C.形成2molA-B键放出的能量与断裂2mol A-B键吸收的能量相等;
D.根据图象可判断反应物与生成物的总能量.
解答 解:A.由图象可知,反应物的能量高于生成物的能量,反应是放热反应,故A错误;
B.因旧键的断裂吸收能量,而不是释放能量,所以断裂 1molA-A 键和 1mol B-B 键吸收 xkJ 能量,故B错误;
C.由图可知形成2molA-B键需要放出ykJ能量,因此断裂2mol A-B键需要吸收ykJ的能量,故C正确;
D.由图可知,1molA2和1molB2的总能量高于2molAB的总能量,故D错误;
故选C.
点评 本题考查了反应热与焓变,题目难度不大,注意把握化学键的断裂、形成与能量的关系,侧重于考查学生对基础知识的应用能力.

练习册系列答案
相关题目
17.下列离子在溶液中能大量共存的是( )
| A. | H+、AlO2-、CO32- | B. | K+、Ba2+、SO42- | C. | NH4+、OH-、NO3- | D. | Fe3+、NO3-、Cl- |
8.某固体可能含有Na+、NH4+、Fe3+、Fe2+、Cl-、I-、CO32-、SO42-中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);
(1)一份固体溶于水,加入足量BaCl2溶液,得沉淀4.46g
(2)另一份固体溶于水,与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672L(标准状况),并得到沉淀,沉淀经洗涤、灼烧,最终获得1.6g红色固体.下列说法正确的是( )
(1)一份固体溶于水,加入足量BaCl2溶液,得沉淀4.46g
(2)另一份固体溶于水,与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672L(标准状况),并得到沉淀,沉淀经洗涤、灼烧,最终获得1.6g红色固体.下列说法正确的是( )
| A. | 该固体中一定含有NH4+、Cl-、SO42-、Na+ | |
| B. | 根据以上实验,无法确定该固体中有Cl- | |
| C. | 该固体中只含有NH4+、Fe3+、SO42-、Cl- | |
| D. | 该固体中一定没有I-、CO32- |
5.已知常温下0.1mol•L-1NH4HCO3溶液的pH=7.8.溶液中含氮(或含碳)各微粒的分布分数(平衡时某种 微粒的浓度占各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( )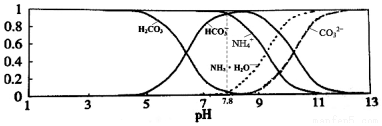

| A. | 当溶液的pH=9时,溶液中存在下列关系:c(NH4+)>c(HCO3-)>c(NH3•H2O)>c(CO32-) | |
| B. | 往该溶液中逐滴滴加氢氧化钠时NH4+和HCO3-浓度逐渐减小 | |
| C. | NH4HCO3溶液中:c(NH4+)+c(NH3•H2O)+c(H+)=c(CO32-)+c(H2CO3)+c(HCO3-)+c(OH-) | |
| D. | 通过分析可知常温下Kb(NH3•H2O)>Ka1(H2CO3) |
12.C和H2在生产、生活、科技中是重要的燃料.
①2C(s)+O2(g)═2CO(g)△H1=-220kJ/mol
②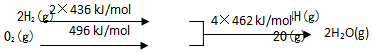
下列推断正确的是( )
①2C(s)+O2(g)═2CO(g)△H1=-220kJ/mol
②

下列推断正确的是( )
| A. | C(s)的燃烧热110 kJ/mol | |
| B. | 2H2(g)+O2(g)═2H2O(g)△H1=+480 kJ/mol | |
| C. | C(s)+H2O(g)═CO(g)+H2(g)△H1=+130 kJ/mol | |
| D. | 欲分解2 mol H2O(l),至少需要提供4×462 kJ 的热量 |
2.已知某溶液中存在NH4+、Ba2+、Fe3+三种阳离子,则其中可能大量存在的阴离子是( )
| A. | SCN- | B. | CO32- | C. | Cl- | D. | OH- |
9.某溶液中大量存在NH4+、Fe2+、Br-、CO32-、AlO2-、S2-、SO32-七种离子中的几种.向该溶液中滴加足量氯水后,有气泡产生并生成橙色澄清溶液;向所得橙色溶液中加入BaCl2溶液时无沉淀生成.根据上述实验事实推断,在该溶液中能大量存在的离子组是( )
| A. | NH4+、SO32-、AlO2- | B. | NH4+、Br-、CO32- | ||
| C. | Fe2+、S2-、SO32- | D. | NH4+、Br-、AlO2- |
6.下列反应既属于非氧化还原反应,又属于吸热反应的是( )
| A. | 高温下炭与CO2的反应 | B. | Ba(OH)2•8H2O与NH4Cl的反应 | ||
| C. | 生石灰溶于水的反应 | D. | 盐酸与烧碱溶液的中和反应 |
7.在一定温度下,下列叙述是可逆反应A(g)+3B(g)?2C(g)达平衡时的特征的是( )
(1)单位时间内生成a mol A,同时生成3a mol B;
(2)A、B、C的分子数之比为1:3:2;
(3)单位时间内消耗a mol A,同时生成3a mol B;
(4)A、B、C的浓度不再变化.
(1)单位时间内生成a mol A,同时生成3a mol B;
(2)A、B、C的分子数之比为1:3:2;
(3)单位时间内消耗a mol A,同时生成3a mol B;
(4)A、B、C的浓度不再变化.
| A. | (1)(2) | B. | (3)(4) | C. | (1)(2)(3)(4) | D. | (1)(3) |