题目内容
19.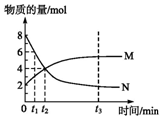 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确的是( )| A. | 化学方程式:2N?M | B. | t2时,正逆反应速率相等,达到平衡 | ||
| C. | t3时,正反应速率大于逆反应速率 | D. | t1时,M的浓度是N浓度的2倍 |
分析 在t2时,N的物质的量为4mol,变化4mol,M的物质的量为4mol,变化2mol,反应的方程式为2N?M,结合图象解答该题.
解答 解:A.在t2时,N的物质的量为4mol,变化4mol,M的物质的量为4mol,变化2mol,反应的方程式为2N?M,故A正确;
B.t2时,M、N物质的量还在变化,所以没有达到平衡状态,故B错误;
C.t3时,达到平衡状态,则正逆反应速率相等,故C错误;
D.t1时,N的物质的量为6mol,M的物质的量为3mol,则N的浓度是M浓度的2倍,故D错误;
故选A.
点评 本题考查化学平衡与图象问题的考查,侧重于学生的分析能力的考查,为高考常见题型,难度中等,注意把握图象曲线变化的趋势以及平衡状态的判断.

练习册系列答案
相关题目
9.某溶液中大量存在NH4+、Fe2+、Br-、CO32-、AlO2-、S2-、SO32-七种离子中的几种.向该溶液中滴加足量氯水后,有气泡产生并生成橙色澄清溶液;向所得橙色溶液中加入BaCl2溶液时无沉淀生成.根据上述实验事实推断,在该溶液中能大量存在的离子组是( )
| A. | NH4+、SO32-、AlO2- | B. | NH4+、Br-、CO32- | ||
| C. | Fe2+、S2-、SO32- | D. | NH4+、Br-、AlO2- |
10.化学反应速率的大小主要取决于( )
| A. | 反应物的性质 | B. | 反应物的浓度 | C. | 反应的温度 | D. | 是否使用催化剂 |
7.在一定温度下,下列叙述是可逆反应A(g)+3B(g)?2C(g)达平衡时的特征的是( )
(1)单位时间内生成a mol A,同时生成3a mol B;
(2)A、B、C的分子数之比为1:3:2;
(3)单位时间内消耗a mol A,同时生成3a mol B;
(4)A、B、C的浓度不再变化.
(1)单位时间内生成a mol A,同时生成3a mol B;
(2)A、B、C的分子数之比为1:3:2;
(3)单位时间内消耗a mol A,同时生成3a mol B;
(4)A、B、C的浓度不再变化.
| A. | (1)(2) | B. | (3)(4) | C. | (1)(2)(3)(4) | D. | (1)(3) |
14.能说明醋酸是弱电解质的是
①醋酸溶液能导电;
②醋酸能和碳酸钙反应放出CO2;
③0.1mol/L醋酸钠溶液pH=8.9;
④醋酸稀溶液中存在醋酸分子;
⑤常温下,0.2mol/L醋酸的pH比0.2mol/L盐酸的pH大;
⑥大小相同的铁片与同物质的量浓度的盐酸和醋酸反应,醋酸产生H2速率慢( )
①醋酸溶液能导电;
②醋酸能和碳酸钙反应放出CO2;
③0.1mol/L醋酸钠溶液pH=8.9;
④醋酸稀溶液中存在醋酸分子;
⑤常温下,0.2mol/L醋酸的pH比0.2mol/L盐酸的pH大;
⑥大小相同的铁片与同物质的量浓度的盐酸和醋酸反应,醋酸产生H2速率慢( )
| A. | ③⑤⑥ | B. | ①③⑤⑥ | C. | ①②③④⑤⑥ | D. | ③④⑤⑥ |
11.下列设计的实验方案与对应的现象或结论正确的是( )
| A. | 镁与水的反应实验:取一小段镁带,直接投入试管,向试管中加入2ml水并滴入2滴酚酞溶液,加热试管至沸腾,观察到溶液变红 | |
| B. | 为了确定酸碱中和是放热反应,实验中向10ml 2mol/L NaOH溶液中加入浓硫酸至恰好中和,测定出溶液温度升高 | |
| C. | 原电池能将化学能转化为电能:将锌片和铜片用导线连接(导线中间接入一个电流表),平行插入盛有稀硫酸溶液的烧杯中,观察到电流表指针偏转 | |
| D. | 探究不同催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLFeCl3溶液,向第二试管中加入2mL5%H2O2和少量MnO2粉末,不同的催化剂对化学反应速率的影响不同 |
8.手性碳原子存在于很多有机化合物中,人们将连有四个不同基团的碳原子形象地成为手性碳原子.下列化合物中含有2个手性碳原子的是( )
| A. | 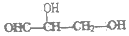 | B. | 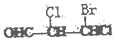 | C. | CH3CH2COOH | D. | 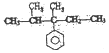 |
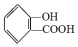 ,
,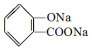 ;请写出将
;请写出将 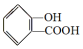 转化为
转化为 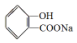 的化学方程式
的化学方程式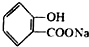 +H2O+CO2↑.
+H2O+CO2↑.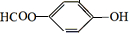
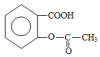 ,它与足量氢氧化钠溶液发生反应的方程式是
,它与足量氢氧化钠溶液发生反应的方程式是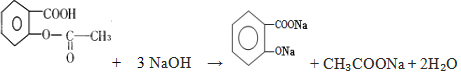 .
.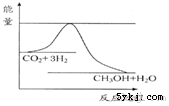 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化.
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化.