题目内容
某学习小组在研究CH4还原Fe2O3的实验中,发现生成的黑色粉末各组分均能被磁铁吸引.查阅资料得知:在温度不同、受热不均时会生成具有磁性的Fe3O4.为进一步探究黑色粉末的组成及含量,他们进行如下实验.一.定性检验
(1)往黑色粉末中滴加盐酸,观察到有气泡产生,则黑色粉末中一定有 ,产生气泡的离子方程式为 .
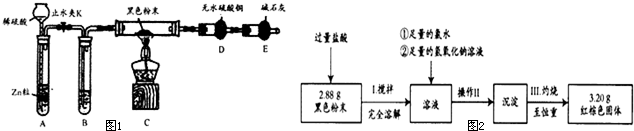
(2)热还原法检验:按图1装置连接好仪器(图中夹持设备已略去),检查装置的气密性.往装置中添加药品.打开止水夹K通人氢气,持续一段时间后再点燃C处的酒精灯.
请回答下列问题:
①检查装置A气密性的方法是 .
②B中试剂的名称是 .
③若加热一段时间后,装置D中白色粉末变蓝色,对黑色粉末的组成得出的结论是 .
(3)为证明黑色粉末是否含Fe3O4,某同学设计实验方案如下:取少量黑色粉末于试管,加足量盐酸,充分振荡使黑色粉末完全溶解,滴入KSCN溶液,观察现象.请分析此方案是否可行,并解释原因.答: .
二.沉淀法定量测定
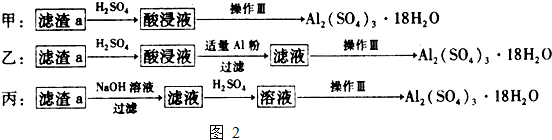
按如图2实验流程进行测定.
(4)操作II的名称是 、 、转移固体.
(5)通过以上数据,计算黑色粉末中各组分的质量分别为 .
(1)往黑色粉末中滴加盐酸,观察到有气泡产生,则黑色粉末中一定有
(2)热还原法检验:按图1装置连接好仪器(图中夹持设备已略去),检查装置的气密性.往装置中添加药品.打开止水夹K通人氢气,持续一段时间后再点燃C处的酒精灯.
请回答下列问题:
①检查装置A气密性的方法是
②B中试剂的名称是
③若加热一段时间后,装置D中白色粉末变蓝色,对黑色粉末的组成得出的结论是
(3)为证明黑色粉末是否含Fe3O4,某同学设计实验方案如下:取少量黑色粉末于试管,加足量盐酸,充分振荡使黑色粉末完全溶解,滴入KSCN溶液,观察现象.请分析此方案是否可行,并解释原因.答:
二.沉淀法定量测定
按如图2实验流程进行测定.
(4)操作II的名称是
(5)通过以上数据,计算黑色粉末中各组分的质量分别为

考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:(1)还原Fe2O3的实验中,发现生成的黑色粉末各组分均能被磁铁吸引,往黑色粉末中滴加盐酸,观察到有气泡产生,证明含有金属铁;
(2)①装置A是启普发生器的原理应用,关闭止水夹,依据气体压强的关系,从长颈漏斗加入水至一定高度,看水面是否变化分析是否漏水;
②气体进入C装置前需要除去水蒸气,否则以炸裂玻璃管;
③D中白色粉末硫酸铜变蓝色证明反应有水生成,黑色固体中含有Fe3O4 被氢气还原生成水,判断可以含有;
(3)黑色粉末加入足量盐酸溶解后,滴入KSCN溶液,不变血红色可能有两种情况,一种是五铁离子存在,一种是有铁离子存在,和过量的铁反应生成亚铁离子;
(4)Ⅲ流程是黑色粉末加入过量盐酸溶解后,加入足量氨水沉淀离子,加入足量氢氧化钠保证碱性环境下离子全部沉淀,操作Ⅱ是过滤、洗涤得到沉淀,放在坩埚内灼烧制恒重得到红褐色固体为氧化铁;
(5)依据反应的化学方程式计算判断.
(2)①装置A是启普发生器的原理应用,关闭止水夹,依据气体压强的关系,从长颈漏斗加入水至一定高度,看水面是否变化分析是否漏水;
②气体进入C装置前需要除去水蒸气,否则以炸裂玻璃管;
③D中白色粉末硫酸铜变蓝色证明反应有水生成,黑色固体中含有Fe3O4 被氢气还原生成水,判断可以含有;
(3)黑色粉末加入足量盐酸溶解后,滴入KSCN溶液,不变血红色可能有两种情况,一种是五铁离子存在,一种是有铁离子存在,和过量的铁反应生成亚铁离子;
(4)Ⅲ流程是黑色粉末加入过量盐酸溶解后,加入足量氨水沉淀离子,加入足量氢氧化钠保证碱性环境下离子全部沉淀,操作Ⅱ是过滤、洗涤得到沉淀,放在坩埚内灼烧制恒重得到红褐色固体为氧化铁;
(5)依据反应的化学方程式计算判断.
解答:
解:(1)还原Fe2O3的实验中,发现生成的黑色粉末各组分均能被磁铁吸引,应为铁或四氧化三铁,换货二者混合物,往黑色粉末中滴加盐酸,观察到有气泡产生,证明含有金属铁;发生反应Fe+2HCl=FeCl2+H2↑黑色粉末中一定含有铁,故答案为:Fe;Fe+2H+=Fe2++H2↑;
(2)①装置A是启普发生器的原理应用,关闭止水夹,依据气体压强的关系,从长颈漏斗加入水至一定高度,看水面是否变化分析是否漏水;
故答案为:关闭止水夹K,往长颈漏斗加水至漏斗内的液面高于导气管,静置一段时间后液面差保持不变,说明装置A的气密性良好;
②气体进入C装置前需要除去水蒸气,否则以炸裂玻璃管;吸收氢气中的水蒸气用浓硫酸溶液,故答案为:浓硫酸;
③D中白色粉末硫酸铜变蓝色证明反应有水生成,黑色固体中含有Fe3O4 被氢气还原生成水,发生反应4H2+Fe3O4=3Fe+4H2O,判断可以含有;依据和酸反应生成氢气和验证生成水判断黑色固体为铁和四氧化三铁;
故答案为:黑色固体含有Fe和Fe3O4;
(3)黑色粉末加入足量盐酸溶解后,滴入KSCN溶液,不变血红色可能有两种情况,一种是五铁离子存在,一种是有铁离子存在,和过量的铁反应生成亚铁离子;所以方案不正确;
故答案为:不可行,因Fe3O4溶于盐酸生成Fe3+与Fe反应生成Fe2+,溶液不变色;
(4)Ⅲ流程是黑色粉末加入过量盐酸溶解后,加入足量氨水沉淀离子,加入足量氢氧化钠保证碱性环境下离子全部沉淀,操作Ⅱ是过滤、洗涤得到沉淀,放在坩埚内灼烧制恒重得到红褐色固体为氧化铁;
故答案为:过滤;洗涤;
(5)依据反应的化学方程式,结合铁元素守恒计算判断;
Fe+Fe3O4
FeCl2 FeCl3
Fe(OH)2 Fe(OH)3
Fe2O3;
依据反应过程中铁元素守恒,3.2gFe2O3物质的量=
=0.02mol;
设铁物质的量为X,四氧化三铁物质的量为Y,得到:56X+232Y=2.88 X+3Y=0.02×2
解方程得到X=0.01mol;Y=0.01mol;铁的质量为5.6g;四氧化三铁的质量为2.32g;
故答案为:Fe、0.56g,Fe3O4、2.32g.
(2)①装置A是启普发生器的原理应用,关闭止水夹,依据气体压强的关系,从长颈漏斗加入水至一定高度,看水面是否变化分析是否漏水;
故答案为:关闭止水夹K,往长颈漏斗加水至漏斗内的液面高于导气管,静置一段时间后液面差保持不变,说明装置A的气密性良好;
②气体进入C装置前需要除去水蒸气,否则以炸裂玻璃管;吸收氢气中的水蒸气用浓硫酸溶液,故答案为:浓硫酸;
③D中白色粉末硫酸铜变蓝色证明反应有水生成,黑色固体中含有Fe3O4 被氢气还原生成水,发生反应4H2+Fe3O4=3Fe+4H2O,判断可以含有;依据和酸反应生成氢气和验证生成水判断黑色固体为铁和四氧化三铁;
故答案为:黑色固体含有Fe和Fe3O4;
(3)黑色粉末加入足量盐酸溶解后,滴入KSCN溶液,不变血红色可能有两种情况,一种是五铁离子存在,一种是有铁离子存在,和过量的铁反应生成亚铁离子;所以方案不正确;
故答案为:不可行,因Fe3O4溶于盐酸生成Fe3+与Fe反应生成Fe2+,溶液不变色;
(4)Ⅲ流程是黑色粉末加入过量盐酸溶解后,加入足量氨水沉淀离子,加入足量氢氧化钠保证碱性环境下离子全部沉淀,操作Ⅱ是过滤、洗涤得到沉淀,放在坩埚内灼烧制恒重得到红褐色固体为氧化铁;
故答案为:过滤;洗涤;
(5)依据反应的化学方程式,结合铁元素守恒计算判断;
Fe+Fe3O4
| 足量稀盐酸 |
| 足量氨水,足量氢氧化钠 |
| 灼烧至恒重 |
依据反应过程中铁元素守恒,3.2gFe2O3物质的量=
| 3.2g |
| 160g/mol |
设铁物质的量为X,四氧化三铁物质的量为Y,得到:56X+232Y=2.88 X+3Y=0.02×2
解方程得到X=0.01mol;Y=0.01mol;铁的质量为5.6g;四氧化三铁的质量为2.32g;
故答案为:Fe、0.56g,Fe3O4、2.32g.
点评:本题考查了探究物质组成,测定物质含量的定量实验操作和实验设计,主要考查铁及其化合物的性质应用,实验基本操作的分析判断,实验现象的推断和应用,元素守恒的计算应用,综合性较强,题目难度中等.

练习册系列答案
相关题目
把0.02mol/L CH3COOH溶液和0.01mol/L NaOH溶液等体积混合,则混合溶液中微粒浓度关系,正确的是( )
| A、c(CH3COO-)>c(Na+) |
| B、c(CH3COOH)>c(CH3COO-) |
| C、2c(H+)=c(CH3COO-)-c(CH3COOH) |
| D、c(CH3COOH)+c(CH3COO-)=0.01mol/L |
下列与有机物结构、性质相关的叙述错误的是( )
| A、乙酸分子中含有羧基,可与NaHCO3溶液反应生成CO2 |
| B、蛋白质和油脂都属于高分子化合物,一定条件下都能水解 |
| C、甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同 |
| D、甘氨酸和硝基乙烷是同分异构体 |
天然色素的提取往往应用到萃取操作,现在有用大量水提取的天然色素,下列溶剂不能用来萃取富集这些天然色素的是( )
| A、石油醚 | B、丙酮 | C、乙醇 | D、乙醚 |


 如图为实验室制取NH3且检验其某一性质的实验装置图.完成下列问题;
如图为实验室制取NH3且检验其某一性质的实验装置图.完成下列问题;