题目内容
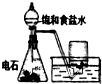
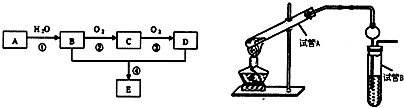
 如图为实验室制取NH3且检验其某一性质的实验装置图.完成下列问题;
如图为实验室制取NH3且检验其某一性质的实验装置图.完成下列问题;(1)如图中D仪器的名称为
(2)写出实验室制取NH3的化学方程式:
(3)该实验检验的是NH3的哪一个性质?
(4)若在烧杯的水中滴加几滴酚酞,则D中将有什么现象?
(5)若实验完成后水充满整个D瓶,且在标况下进行,则所得氨水的物质的量浓度为
考点:常见气体制备原理及装置选择
专题:实验题
分析:(1)由图可知,D仪器的名称圆底烧瓶;
(2)氨盐和碱反应生成氨气和水,实验室用氢氧化钙和氯化铵在加热条件下反应制备氨气;
(3)该实验为氨气的“喷泉实验”,检验的是氨气极易溶于水;
(4)氨水中存在:NH3?H2O?OH-+NH4+,电离出OH-,溶液显碱性,遇酚酞试液变红色;
(5)设氨气为VL,则氨气的物质的量为
mol,则反应后溶液体积为VL,所以浓度为c=
=
=
mol/L.
(2)氨盐和碱反应生成氨气和水,实验室用氢氧化钙和氯化铵在加热条件下反应制备氨气;
(3)该实验为氨气的“喷泉实验”,检验的是氨气极易溶于水;
(4)氨水中存在:NH3?H2O?OH-+NH4+,电离出OH-,溶液显碱性,遇酚酞试液变红色;
(5)设氨气为VL,则氨气的物质的量为
| V |
| 22.4 |
| n |
| V |
| ||
| VL |
| 1 |
| 22.4 |
解答:
解:(1)由图可知,D仪器的名称圆底烧瓶,
故答案为:圆底烧瓶;
(2)氨盐和碱反应生成氨气和水,实验室用氢氧化钙和氯化铵在加热条件下反应制备氨气,反应的化学方程式为Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O,
故答案为:Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O;
(3)该实验为氨气的“喷泉实验”,实验者用滴管把少量的水挤入一个充满了氨气的干燥容器中,氨气溶解在水中,使容器内产生负压,因此更多的水在大气压的作用下从另一个入口处进入,产生喷泉效应,检验的是氨气极易溶于水的性质,
故答案为:氨气极易溶于水;
(4)NH3+H2O?NH3?H2O,氨水中存在:NH3?H2O?OH-+NH4+,电离出OH-,溶液显碱性,遇酚酞试液变红色,
故答案为:可观察到红色喷泉;NH3+H2O?NH3?H2O?OH-+NH4+;
(5)设氨气为VL,则氨气的物质的量为
mol,则反应后溶液体积为VL,所以浓度为c=
=
=
mol/L,
故答案为:
.
故答案为:圆底烧瓶;
(2)氨盐和碱反应生成氨气和水,实验室用氢氧化钙和氯化铵在加热条件下反应制备氨气,反应的化学方程式为Ca(OH)2+2NH4Cl
| ||
故答案为:Ca(OH)2+2NH4Cl
| ||
(3)该实验为氨气的“喷泉实验”,实验者用滴管把少量的水挤入一个充满了氨气的干燥容器中,氨气溶解在水中,使容器内产生负压,因此更多的水在大气压的作用下从另一个入口处进入,产生喷泉效应,检验的是氨气极易溶于水的性质,
故答案为:氨气极易溶于水;
(4)NH3+H2O?NH3?H2O,氨水中存在:NH3?H2O?OH-+NH4+,电离出OH-,溶液显碱性,遇酚酞试液变红色,
故答案为:可观察到红色喷泉;NH3+H2O?NH3?H2O?OH-+NH4+;
(5)设氨气为VL,则氨气的物质的量为
| V |
| 22.4 |
| n |
| V |
| ||
| VL |
| 1 |
| 22.4 |
故答案为:
| 1 |
| 22.4 |
点评:本题考查了氨气的制备原理和装置选择,侧重于实验原理和计算,难度不大,注意根据实验原理分析实验现象.

练习册系列答案
相关题目
欲除去铜粉中少量的铁粉,可选用的试剂是( )
| A、水 | B、氢氧化钠溶液 |
| C、稀硫酸 | D、稀硝酸 |
 普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型).下列关系普伐他汀的性质描述正确的是( )
普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型).下列关系普伐他汀的性质描述正确的是( )| A、能与FeCl3溶液发生显色反应 |
| B、能使酸性KMnO4溶液褪色 |
| C、1mol该物质与足量钠发生反应生成4molH2 |
| D、1mol该物质最多可与1molNaOH反应 |