题目内容
11.水是地球表面上普遍存在的化合物,我们可以用我们学习的物质结构与性质的有关知识去认识它.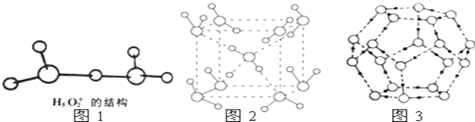
(1)氧的第一电离能在同周期元素中由大到小排第4位.
(2)根据等电子体原理,写出水合氢离子的一个等电子体(写电子式)
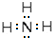 .
.(3)水分子可以形成许多水合物.
①水分子可以作配体和铜离子形成水合铜离子[Cu(H2O)4]2+,1mol水合铜离子中含有σ键数目为12NA.
②图1是水合盐酸晶体H5O2+•Cl-中H5O2+离子的结构.在该离子中,存在的作用力有abfi.
a.配位键 b.极性键 c.非极性键 d.离子键 e.金属键
f.氢键 g.范德华力 h.π 键 i.σ键
(4)韩国首尔大学科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成了“暖冰”.请从结构上解释生成暖冰的原因水分子是极性分子,在电场作用下定向有规则的排列,分子间通过氢键结合而成固体.
(5)最新研究发现,水能凝结成13种类型的结晶体,除普通冰以外其余各自的冰都有自己奇特的性质:有在-30℃才凝固的超低温冰,它的坚硬程度可和钢相媲美,能抵挡炮弹轰击;有在180℃高温下依然不变的热冰;还有的冰密度比水大,号称重冰.图2为冰的一种骨架形式,依此为单位向空间延伸.
①该冰中的每个水分子有2个氢键;
②如果不考虑晶体和键的类型,哪一物质的空间连接方式与这种冰连接类似?SiO2;
③已知O-H…O距离为295pm,列式计算此种冰晶体的密度$\frac{18×2}{(\frac{2×295×1{0}^{-10}}{\sqrt{3}})×6.02×1{0}^{23}}$=1.51g/cm3.
(已知2952=8.70×104,2953=2.57×107,$\sqrt{2}$=1.41,$\sqrt{3}$=1.73)
(6)冰融化后,在液态水中,水分子之间仍保留有大量氢键将水分子联系在一起,分子间除了无规则的分布及冰结构碎片以外,一般认为还会有大量呈动态平衡的、不完整的多面体的连接方式.图3的五角十二面体是冰熔化形成的理想多面体结构.
①该五角十二面体有20顶点,160条对角线;
②假设图2中的冰熔化后的液态水全部形成如图3的五角十二面体,且该多面体之间无氢键,则该冰熔化过程中氢键被破坏的百分比为25%.
分析 (1)同周期中稀有气体的电离能最大,其它元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族、第VA族元素的第一电离能大于相邻元素;
(2)原子总数相等、价电子总数也相等的微粒互为等电子体;
(3)①铜离子含有空轨道,水分子含有孤对电子对,铜离子与水分子之间形成配位键,铜离子配体数为4,1个H2O含2个O-H键,则[Cu(H2O)4]2+含有12个σ键;
②氢离子含有空轨道,氧原子含有孤电子对,能形成配位键,O-H为极性键,单键属于σ键,O原子与H原子之间会形成氢键;
(4)暖冰为分子晶体,暖冰中水分子之间主要的作用力为氢键,电场作用下,水分子间更易制得“暖冰”;
(5)①以立方体中的水分子为研究对象,每个水分子形成4条氢键;每一条氢键连接2个水分子,故冰晶体中氢键数目为水分子数目的2倍;
②以立方体中的水分子为研究对象,每个水分子与周围4个水分子形成4个氢键,为正四面体构型,SiO2空间连接方式与这种冰连接类似;
③设体心立方中晶胞的棱长为X,O-H…O距离为A,则3X2=(2A)2,故X=$\frac{2A}{\sqrt{3}}$,利用均摊法计算晶胞中水分子数目,表示出晶胞质量,再根据ρ=$\frac{m}{V}$计算;
(6)①正十二面体每三个相邻的面都有一个公共顶点,这个公共顶点分别是这三个小正五边形的一个顶点,对角线为任意两点间的连线减去棱数;
②冰融化为液态水时,水分子数目不变,利用均摊法计算图2、图3中每个水分子形成氢键,减少的氢键即为破坏氢键;.
解答 解:(1)同一周期内主族元素的第一电离能从左到右在总体增大的趋势中有些曲折.当外围电子在能量相等的轨道上形成全空、半满或全满结构时,原子的能量较低,元素的第一电离能较大,由于N元素的2p能级3个轨道处于半满,He元素的2P能级3个轨道处于全满,所以第二周期的第一电离能大小顺序是I1(He)>I1(F)>I1(N)>I1(O)>I1(C)>I1(Be)>I1(B),氧的第一电离能在同周期元素中由大到小排第4位,
故答案为:4;
(2)H3O+中O原子的质子数为8,H原子的质子数为1,所以H3O+的质子数为11,电子数=11-1=10,NH3的原子数目为4,电子数目为10,则与H3O+互为等电子体,电子式为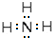 ,
,
故答案为: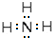 ;
;
(3)①Cu2+含有空轨道,H2O含有孤对电子,可形成配位键,铜离子配体数为4,配离子[Cu(H2O)4]2+中1个Cu2+与4个H2O形成配位键,1个H2O含2个O-H键,所以1mol水合铜离子中含有σ键数目为12NA,
故答案为:12NA;②根据图1水合盐酸晶体H5O2+•Cl-中H5O2+离子的结构知:
a.氢离子含有空轨道,氧原子含有孤电子对,所以能形成配位键;
b.O-H形成极性键;
c.无非极性键;
d.因H5O2+中无阴阳离子,所以不存在离子键;
e.因H5O2+中无金属所以不存在金属键;
f.氢键存在于不直接相连的H与电负性较大的O原子间;
g.因H5O2+中无分子,所以不存在范德华力;
h.因H5O2+中无双键或三键,所以不存在π键;
i.O-H形成σ键,
故答案为:a b f i;
(4)水分子之间主要通过氢键形成固体,水分子是极性分子,在电场作用下定向有规则的排列,水分子间更易形成氢键,
故答案为:水分子是极性分子,在电场作用下定向有规则的排列,分子间通过氢键结合而成固体;
(5)①晶体冰中,每两个水分子间有一个氢键,平均属于每个水分子有半个,一个水分子与周围的四个水分子以氢键结合,故1mol冰中有2 mol氢键,
故答案为:2;
②二氧化硅是原子晶体,Si-O通过共价键形成四面体结构,四面体之间通过共价键形成空间网状结构,以立方体中的水分子为研究对象,每个水分子形成4条氢键,SiO2空间连接方式与这种冰连接类似,
故答案为:SiO2;
③体心立方晶胞中水分子个数=1+8×$\frac{1}{8}$=2;设体心立方中晶胞的棱长为X,O-H…O距离为A,则3X2=(2A)2,体心立方的密度ρ=$\frac{m}{V}$=$\frac{2m}{{N}_{A}×{X}^{3}}$
=$\frac{18×2}{(\frac{2×295×1{0}^{-10}}{\sqrt{3}})×6.02×1{0}^{23}}$=1.51g/cm3,
故答案为:$\frac{18×2}{(\frac{2×295×1{0}^{-10}}{\sqrt{3}})×6.02×1{0}^{23}}$=1.51;
(6)①这个正十二面体的顶点的个数是原来12个小正五边形的顶点总和的$\frac{1}{3}$,由此即可得出正十二面体的顶点个数;5×12×$\frac{1}{3}$=20(个),从20个点选两个就可以连线,棱数为:5×$12×\frac{1}{2}$=30,对角线为任意两点间的连线减去棱数,即$\frac{20×19}{2}$-30=160,
故答案为:20;160;
②冰融化为液态水时,水分子数目不变,图2中每个水分子平衡含有氢键数目为4×$\frac{1}{2}$=2,图3中每个水分子平衡含有氢键数目为3×$\frac{1}{2}$=1.5,则该冰熔化过程中氢键被破坏的百分比为 $\frac{2-1.5}{2}$×100%=25%,
故答案为:25%.
点评 本题考查较为综合,涉及分子的立体构型、晶胞的计算,氢键、分子结构等知识,注意晶体类型的有关计算,需要全面掌握基础知识,并能运用分析解决问题,难点是晶胞计算,题目难点中等.

| A. | 体系的总压强不变 | |
| B. | 体系内各物质的质量分数不再发生变化 | |
| C. | 体系内气体密度不再发生变化 | |
| D. | 单位时间消耗0.1molCO(g)的同时生成0.1molH2O(g) |
 环境监测测定水中溶解氧的方法是:
环境监测测定水中溶解氧的方法是:①量取25mL水样,迅速加入固定剂MnSO4溶液和碱性KI溶液(含KOH),立即塞好瓶塞,反复振荡,使之充分反应,其反应式为:2Mn2++O2+4OH-=2MnO(OH)2(该反应极快)
②测定:开塞后迅速加入1mL~2mL浓硫酸(提供H+),使之生成I2,再用0.1000mol/L的Na2S2O3溶液滴定(以淀粉为指示剂),消耗VmL. 有关反应式为:MnO(OH)2+2I-+4H+=Mn2++I2+3H2O I2+2S2O32-=2I-+S4O62-.
请填写下列空白:
(1)用标准的Na2S2O3溶液滴定待测溶液时,左手握滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化,直到因加入一滴Na2S2O3溶液后,溶液由蓝色变为无色,且在半分钟内不变色为止.
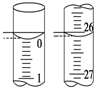
(2)若滴定开始和结束时,碱式滴定管中的液面如图所示,则所
用Na2S2O3溶液的体积为26.10mL.
(3)下列操作中引起的误差偏低的是A、D(填字母序号).
A.读数:滴定前平视,滴定后俯视
B.未用标准液润洗滴定管
C.用固体配制Na2S2O3溶液时,其固体中含有对反应体系无影响的杂质
D.待测液的滴定管之前有气泡,取液后无气泡
(4)某学生根据3次实验分别记录有关数据如下表:
| 滴定次数 | 待测液的体积/mL | 0.1000mol•L-1 Na2S2O3的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | Fe3+Br2 | Cl- | |
| ② | KClO3 | 浓盐酸 | Cl2 | ||
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| A. | 表中①组的反应可能有一种或两种元素被氧化 | |
| B. | 氧化性强弱的比较:KClO3>Fe3+>Cl2>Br2 | |
| C. | 表中②组反应的还原产物是KCl,电子转移数目是6e- | |
| D. | 表中③组反应的离子方程式为:2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O |
| A. | 冰的密度比水小,能浮在水面上 | |
| B. | 接近沸点的水蒸气的相对分子质量测量值大于18 | |
| C. | 邻羟基苯甲醛的沸点低于对羟基苯甲醛 | |
| D. | H2O比H2S稳定 |
| A. | 1L1mol/L的甲醇水溶液中含有氢原子总数为4NA | |
| B. | 50mL18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA | |
| C. | 反应KIO3+6HI═KI+3H2O+3I2中,生成3molI2转移电子的总数为5NA | |
| D. | 12g石墨和C60的混合物中质子总数为12NA |
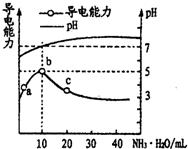
| A. | HR为强酸 | |
| B. | a、b、c三点所示溶液中水的电离程度相同 | |
| C. | b点溶液中c(NH4+)>c(R-)>c(OH-)>c(H+) | |
| D. | a~c任意点溶液均有c(H+)×c(OH-)=Kw=l.0×l0-14 |
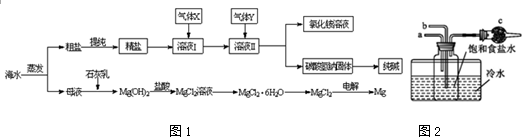
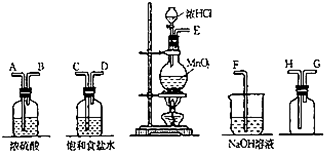 实验室中用二氧化锰与浓盐酸反应制备干燥纯净的氯气.进行此实验,所用仪器如图:
实验室中用二氧化锰与浓盐酸反应制备干燥纯净的氯气.进行此实验,所用仪器如图: