题目内容
7.在一定条件下,向某固定容积的密闭容器中加入1molCO(g)和1molH2O(g),发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g).此反应达到平衡的标志是( )| A. | 体系的总压强不变 | |
| B. | 体系内各物质的质量分数不再发生变化 | |
| C. | 体系内气体密度不再发生变化 | |
| D. | 单位时间消耗0.1molCO(g)的同时生成0.1molH2O(g) |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、两边气体计量数相等,所以体系的总压强一直不变,故A错误;
B、体系内各物质的质量分数不再发生变化,说明各物质的量不变,说明反应达平衡状态,故B正确;
C、体系内气体密度一直不发生变化,故C错误;
D、单位时间消耗0.1molCO(g)等效于消耗0.1molH2O(g),同时生成0.1molH2O(g),正逆反应速率相等,反应达平衡状态,故D正确;
故选BD.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
20.某有机物M的结构简式如图所示,下列说法正确的是( )
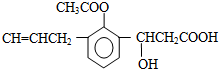

| A. | M中至少有8个碳原子共面 | |
| B. | M能发生还原、氧化、中和、缩聚、取代、加成、银镜等反应 | |
| C. | M中苯环上的一氯取代物有两种不同的结构 | |
| D. | 1molM消耗Na、NaOH、NaHCO3的物质的量的比是2:2:1 |
2.3.0gFe2O3和Al2O3组成的混合物全部溶于200mLpH=0的硫酸,反应后向所得溶液中加入100mLNaOH溶液,恰好使Fe3+、Al3+完全沉淀,则加入的NaOH的浓度c(NaOH)为( )
| A. | 1mol/L | B. | 2mol/L | C. | 4mol/L | D. | 8mol/L |
12.雾霾天气已经严重影响了我国的生活.下列措施不利于“蓝天工程”建设的是( )
| A. | 加高工厂烟囱,使烟尘和废气远离地表 | |
| B. | 推广使用燃煤脱硫技术,防止SO2污染 | |
| C. | 研制新型高效可充电电池,发展电动汽车 | |
| D. | 开发利用绿色能源,替代化石燃料 |
19.下列晶体中,不是分子晶体的是( )
| A. | 氯化铵 | B. | 硫酸 | C. | 氦气 | D. | 三氧化硫 |
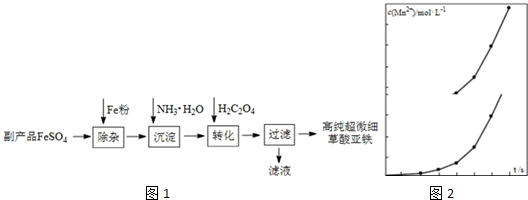
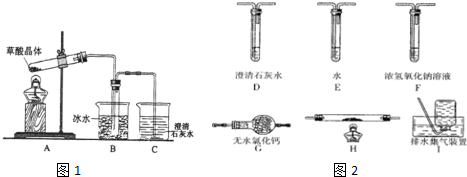
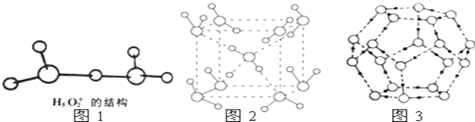
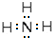 .
.