题目内容
1.饮用水质量是关系人类健康的重要问题.(1)氯气是最早用于饮用水消毒的物质,其消毒作用主要是氯气溶于水后生成了次氯酸,该反应的离子方程式为Cl2+H2O═H++Cl-+HClO.
(2)向AgNO3溶液中加入氯水,氯水中起作用的主要微粒是Cl-,反应的离子方程式是Cl-+Ag+=AgCl↓.
(3)向氯水中滴加石蕊试液,溶液变红,起作用的微粒是H+;然后又褪色,起作用的微粒是HClO.
(4)写出工业上制取漂白粉的化学反应方程式:2Cl2+2Ca(OH)2═Ca(ClO)2+CaCl2+2H2O.
分析 (1)氯气与水反应生成HCl、HClO,HClO具有消毒作用;
(2)向AgNO3溶液中加入氯水,氯水中氯离子可以和银离子之间反应生成氯化银沉淀;
(3)氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白性;
(4)氯气通入石灰乳中反应生成氯化钙、次氯酸钙、水.
解答 解:(1)氯气溶于水后生成了次氯酸和盐酸,氯气、水、次氯酸在离子反应中保留化学式,则离子反应为Cl2+H2O═H++Cl-+HClO,
故答案为:Cl2+H2O═H++Cl-+HClO;
(2)向AgNO3溶液中加入氯水,氯水中氯离子可以和银离子之间反应生成氯化银沉淀,即Cl-+Ag+=AgCl↓,氯水中起作用的主要微粒是Cl-,故答案为:Cl-;Cl-+Ag+=AgCl↓;
(3)氯气和水反应生成盐酸和次氯酸,盐酸具有酸性,氯水具有漂白性,向氯水中滴加石蕊试液,溶液变红,起作用的微粒是H+,后又褪色,起作用的微粒是HClO,
故答案为:H+;HClO
(4)氯气通入石灰乳中反应生成氯化钙、次氯酸钙、水,该反应为2Cl2+2 Ca(OH)2═Ca(ClO)2+CaCl2+2H2O,
故答案为:2Cl2+2 Ca(OH)2═Ca(ClO)2+CaCl2+2H2O.
点评 本题考查氯气的性质,为高频考点,把握发生的反应及电极反应为解答的关键,侧重分析与应用能力的考查,题目难度不大

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
12.若用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 22.4 L NH3中含氮原子数为 NA | |
| B. | 1 mol Na2O2与水完全反应时转移的电子数为NA | |
| C. | 100 mL 2.0 mol•L-1 NH4HCO3溶液中NH4+数为0.2NA | |
| D. | 1 mol O2和2 mol SO2在密闭容器中充分反应后的分子数等于2NA |
16.足量的氯气或盐酸分别跟下列金属反应,均有MCl2型化合物生成的是( )
| A. | Al | B. | Mg | C. | Fe | D. | Na |
6.在常温下,下列溶液不能溶解铁的是( )
| A. | 稀硫酸 | B. | FeCl3溶液 | C. | CuCl2 | D. | 浓硝酸 |
11.用NA表示阿伏加德罗常数的值,下列判断正确的是( )
| A. | 11.1 mol•L-1KCIO3溶液中含有的氯离子数目为NA | |
| B. | 标准状况下,22.4L H2O含有的分子数目为NA | |
| C. | 16g O2与16gO3含有的氧原子数目相等 | |
| D. | 1 mol Zn变为Zn2+时失去的电子数目为NA |
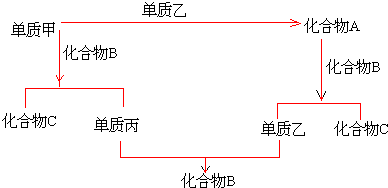

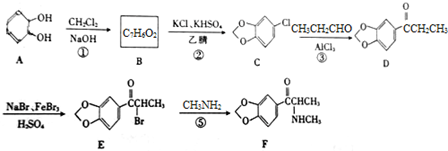
 ;
; (填结构简式);
(填结构简式); )的合成路线.
)的合成路线.