��Ŀ����
10��ij�о���ѧϰС��Թ���̿������������Ӧ���������ɷֽ����о�����1��������裺�ٸ÷�Ӧ�����������CO2�� �ڸ÷�Ӧ�����������CO���۸÷�Ӧ�����������CO2��CO�Ļ����
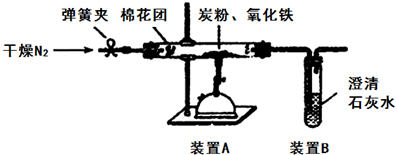
��Ʒ�����ͼ��ʾ����һ�������������ڸ��������������������̿����ȫ��Ӧ���ⶨ�μӷ�Ӧ��̼Ԫ������Ԫ�ص������ȣ�
��2���������ϣ���������̼��������������Ӧ��ʵ���ҿ������Ȼ�隣�����Һ���������ƣ�NaNO2��������Һ��ϼ��ȷ�Ӧ�Ƶõ�������д���÷�Ӧ�����ӷ���ʽ��NH4++NO2-$\frac{\underline{\;\;��\;\;}}{\;}$N2��+2H2O��
��3��ʵ�鲽�裺
�ٰ���ͼ����װ�ã������װ�õ������ԣ���ȡ3.20g��������2.00g̼�ۻ�Ͼ��ȣ�����48.48g��Ӳ�ʲ������У�
�ڼ���ǰ����ͨһ��ʱ�䴿������ĵ�����
��ֹͣͨ��N2�н����ɼУ�����һ��ʱ�䣬����ʯ��ˮ������������ǣ�
�ܴ���Ӧ�������ٻ���ͨ��һ��ʱ��ĵ�������ȴ�����£��Ƶ�Ӳ�ʲ����ܺ���������Ϊ52.24g��
�ݹ��˳�ʯ��ˮ�еij�����ϴ�ӡ���ɺ�Ƶ�����Ϊ2.00g��
����ڡ����ж��ֱ�ͨ��N2�������÷ֱ�Ϊ��Ӧǰ�ž�װ���ڵĿ�����ȷ����Ӧ�õ���CO2ȫ��ͨ��Bװ��
��4�����ݴ������Ը���ʵ�����ݷ�����д����ʵ������������̼������Ӧ�Ļ�ѧ����ʽ��Fe2O3+2C$\frac{\underline{\;����\;}}{\;}$2Fe+CO��+CO2����
��5��ʵ�鷴˼��ѧϰѧϰС����ͬѧ��ΪӦ��ʵ��װ�ý�һ�����ƣ�
�ټ�ͬѧ��Ϊ��Ӧ������ʯ��ˮ����Ba��OH��2��Һ����������Ba��OH��2���ܽ�ȴ���Ca��OH��2����֤������CO2ȫ����װ��B���գ��������ݳ���ɲⶨ��
�ڴ�װ�ô���һ��ȱ�ݣ�����ָ��û��β������װ�ã�
���� ��1���ڻ�ԭ�������ķ�Ӧ��̼�ȿ��Ա���������CO��Ҳ���ܱ���������CO2���ʼ����Ӧ��CO2��CO�Ļ���
��2������������ԭ��Ӧ��笠��������������������ɵ�����ˮ��
��3����ֹ�������뷴Ӧ��ʵ��ǰ�õ����ž�װ���еĿ�����ʵ�������ȷ����Ӧ�õ���CO2ȫ��ͨ��Bװ�ã�
��4�����ݢݿ�֪������CO2�����ʵ�����$\frac{2.00g}{100g/mol}$=0.02mol����������0.88g�����ݢܿ�֪��Ӧ�����ɵ����干48.48g+3.2g+2.0g-52.24g=1.44g�����CO��������1.44g-0.88g=0.56g�������ʵ�����$\frac{0.56g}{28g/mol}$=0.02mol����CO��CO2�����֮����1��1��
��5�����������Ƶ��ܽ��С������CO2��Ч��������������ܽ�ȴ�����CO2��Ч��Ҫ�ã���̼�ᱵ����Է�����������̼��Ƶģ�����ʱ���С��
��CO�ж������Ҫ��β������װ�ã�
��� �⣺��1���ڻ�ԭ�������ķ�Ӧ��̼�ȿ��Ա���������CO��Ҳ���ܱ���������CO2���ʼ����Ӧ��CO2��CO�Ļ����ʴ�Ϊ��CO2��CO�Ļ���
��2������������ԭ��Ӧ��笠��������������������ɵ�����ˮ����Ӧ���ӷ���ʽΪNH4++NO2-$\frac{\underline{\;\;��\;\;}}{\;}$N2��+2H2O���ʴ�Ϊ��NH4++NO2-$\frac{\underline{\;\;��\;\;}}{\;}$N2��+2H2O��
��3��ʵ�������Ӧ��ֹ�������뷴Ӧ������ʵ��ǰ�õ����ž�װ���еĿ�����ʵ�������Ϊ�˰����ɵ�����ȫ���ų�������Ҫ�õ����ž����ɵ����壬ȷ����Ӧ�õ���CO2ȫ��ͨ��Bװ�ã�
�ʴ�Ϊ����Ӧǰ�ž�װ���ڵĿ�����ȷ����Ӧ�õ���CO2ȫ��ͨ��Bװ�ã�
��4�����ݢݿ�֪������CO2�����ʵ�����$\frac{2.00g}{100g/mol}$=0.02mol����������0.88g�����ݢܿ�֪��Ӧ�����ɵ����干48.48g+3.2g+2.0g-52.24g=1.44g�����CO��������1.44g-0.88g=0.56g�������ʵ�����$\frac{0.56g}{28g/mol}$=0.02mol����CO��CO2�����֮����1��1����Ӧ����ʽΪ��Fe2O3+2C$\frac{\underline{\;����\;}}{\;}$2Fe+CO��+CO2����
�ʴ�Ϊ��Fe2O3+2C$\frac{\underline{\;����\;}}{\;}$2Fe+CO��+CO2����
��5�����������Ƶ��ܽ��С������CO2��Ч��������������ܽ�ȴ�����CO2��Ч��Ҫ�ã���̼�ᱵ����Է�����������̼��Ƶģ�����ʱ���С��
�ʴ�Ϊ��Ba��OH��2���ܽ�ȴ���Ca��OH��2����֤������CO2ȫ����װ��B���գ��������ݳ���ɲⶨ��
��CO�ж������Ҫ��β������װ�ã��ʴ�Ϊ��û��β������װ�ã�
���� ������Ҫ�ǿ���ʵ�鷽����ơ�̽�������۵ȣ�ע��̽��ʵ���һ�㲽�裬ˮ��ѧ���ۺ������Ŀ��飬Ϊ�߿��������ͣ�ע������Ԫ�ػ�����֪ʶ��ע��ʵ������������ʶ������ʵ����ȷ�ԣ��Ѷ��еȣ�

 �Ͻ�ƽСѧ��������ϵ�д�
�Ͻ�ƽСѧ��������ϵ�д� �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�| A�� | ��֪��H2��g��+$\frac{1}{2}$O2��g���TH2O��l������H=-285.8 kJ•mol-1����H2��ȼ����Ϊ-285.8 kJ•mol-1 | |
| B�� | ��֪��S��g��+O2��g���TSO2��g����H1=-Q1��S��s��+O2��g���TSO2��g����H2=-Q2����Q1��Q2 | |
| C�� | ��֪��$\frac{1}{2}$H2SO4��Ũ��+NaOH��aq���T$\frac{1}{2}$Na2SO4��aq��+H2O��l����H1�� CH3COOH��aq��+NH3•H2O��aq���TCH3COONH4��aq��+H2O��l����H2������|��H1|��|��H2| | |
| D�� | ��֪��Fe2O3��s��+3C��ʯī���T2Fe��s��+3CO��g����H=+489.0 kJ•mol-1 CO��g��+$\frac{1}{2}$O2��g���TCO2��g����H=-283.0 kJ•mol-1 C��ʯī��+O2��g���TCO2��g����H=-393.5 kJ•mol-1 ��4Fe��s��+3O2��g���T2Fe2O3��s����H=-1641.0 kJ•mol-1 |
������⣺Fe3+��Br2˭�������Ը�ǿ��
��1�����룺
�ټ�ͬѧ��Ϊ�����ԣ�Fe3+��Br2��������ʵ�������Ƿ�����ѧ��Ӧ���£�����Һ�ʻ�ɫ�Ǻ�Br2���ѧʽ����ͬ�����£�
����ͬѧ��Ϊ�����ԣ�Br2��Fe3+��������ʵ�������Ƿ�����ѧ��Ӧ���£�����Һ�ʻ�ɫ�Ǻ�Fe3+���£�
��2�����ʵ�鲢��֤
��ͬѧΪ��֤��ͬѧ�Ĺ۵㣬ѡ������ijЩ�Լ���Ƴ����ַ�������ʵ�飬��ͨ���۲�ʵ������֤������ͬѧ�Ĺ۵�ȷʵ����ȷ�ģ�
��ѡ�õ��Լ���a����̪��Һ��b��CCl4��c����ˮ�ƾ���d��KSCN��Һ��
�����ڱ���д����ͬѧѡ�õ��Լ���ʵ���й۲쵽�������Լ�����ţ�
| ѡ���Լ� | ʵ������ | |
| ����1 | ||
| ����2 |
��4��ʵ����˼��
�ٸ�������ʵ���Ʋ⣬�����廯������Һ��ͨ�����������ȱ������������ǣ�Fe2+�������ӵĻ�ѧʽ����
����100mL FeBr2��Һ��ͨ��2.24L Cl2����״��������Һ����1/2��Br-�������ɵ���Br2����ԭFeBr2��Һ��FeBr2�����ʵ���Ũ��Ϊ1mol•L-1��
| A�� | Na2FeO4 ����ˮ������Ӧ����Fe��OH��3 ��O2���ʿ�����ˮ���������;����� | |
| B�� | �������濾������һ�����ܵ�Fe3O4��������ʴ���� | |
| C�� | ̫���ܡ������ǿ�������Դ��Ӧ�����ƹ�̫���ܡ����ܵ�ʹ�� | |
| D�� | ������Դ������ͺͿ����͵���Ҫ��ѧ�ɷ���ͬ |
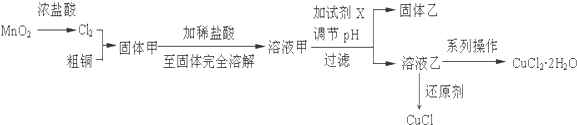

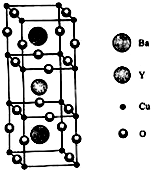 ͭ��Ԫ�ذ���Cu��Ag��Au���䵥�ʾ�Ϊ�����������壮
ͭ��Ԫ�ذ���Cu��Ag��Au���䵥�ʾ�Ϊ�����������壮