题目内容
8.设NA为阿伏伽德罗常数的值.下列说法正确的是( )| A. | 通常情况下,32gO2和O3的混合气体含有的分子总数小于NA | |
| B. | 常温常压下,0.1mol•L-1的硝酸铵溶液中氮原子数目为0.2NA | |
| C. | 1mol有机物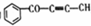 中最多有6NA个原子在一条直线上 中最多有6NA个原子在一条直线上 | |
| D. | 1mol甲基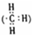 所含的电子数为7NA 所含的电子数为7NA |
分析 A、氧气和臭氧的摩尔质量不同,臭氧的摩尔质量大于氧气;
B、溶液体积不明确;
C、 中可以有7个原子共直线;
中可以有7个原子共直线;
D、甲基中含9个电子.
解答 解:A、氧气和臭氧的摩尔质量不同,臭氧的摩尔质量大于氧气,当32g全部为氧气时,分子个数为NA个,而当混有摩尔质量大于32g/mol的臭氧时,分子个数小于NA个,故A正确;
B、溶液体积不明确,故溶液中的氮原子个数无法计算,故B错误;
C、苯环为正六边形结构,夹角均为120°C,所以最多有7个原子共线,故C错误;
D、甲基中含9个电子,故1mol甲基中含9NA个电子,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
18.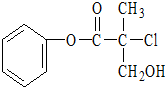 某有机物A是农药生产中的一种中间体,其结构简式如图所示:下列关于A的叙述正确的是( )
某有机物A是农药生产中的一种中间体,其结构简式如图所示:下列关于A的叙述正确的是( )
 某有机物A是农药生产中的一种中间体,其结构简式如图所示:下列关于A的叙述正确的是( )
某有机物A是农药生产中的一种中间体,其结构简式如图所示:下列关于A的叙述正确的是( )| A. | 属于卤代烃,易溶于水 | |
| B. | 在酸性或碱性条件下都能发生水解反应 | |
| C. | 1molA可以与2molNaOH反应 | |
| D. | 一定条件下可发生加成反应和消去反应 |
19.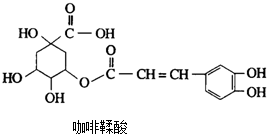 金银花中含有绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法不正确的是( )
金银花中含有绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法不正确的是( )
 金银花中含有绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法不正确的是( )
金银花中含有绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法不正确的是( )| A. | 绿原酸能与FeCl3发生显色反应 | |
| B. | 1个绿原酸分子中含有4个手性碳原子 | |
| C. | 绿原酸与足量的NaOH反应,其中一种产物的化学式为C9H5O4Na3 | |
| D. | 1mol绿原酸最多能与6molH2发生反应 |
16.下列关于有机物性质的叙述错误的是( )
| A. | 甲烷和氯气在光照条件下反应产生油状液滴 | |
| B. | 乙烯能使溴的四氯化碳溶液褪色 | |
| C. | 苯能使酸性高锰酸钾溶液褪色 | |
| D. | 乙醇可以和金属钠反应放出氢气 |
3.对溶液中的离子进行鉴定,下列实验所得结论不合理的是( )
| A. | 溶液中加入HCl酸化后,再加入BaCl2溶液,有白色沉淀产生,则溶液中含有SO42- | |
| B. | 溶液中加入KSCN溶液,无红色出现,继续加入氯水,溶液变红,说明溶液中一定含有Fe2+ | |
| C. | 溶液中加入NaOH溶液,加热后产生使湿润的红色石蕊试纸变蓝的气体,则可推测该溶液中含有NH4+ | |
| D. | 向溶液中加入盐酸,有使澄清石灰水变浑浊的无色无味的气体放出,可推测溶液中含有CO32- |
13.下列化学方程式书写正确的是( )
| A. | CO2+H2O+CaCl2═2HCl+CaCO3↓ | B. | 2NaCl+MgSO4═Na2SO4+MgCl2 | ||
| C. | 2HgO═2Hg+O2 | D. | 2KOH+CO2═K2CO3+H2O |
20.下列各组元素中按微粒半径递增顺序排列的是( )
| A. | Li Na K | B. | Ba2+ Ca2+ Mg2+ | C. | Cl-K+ Ca2+ | D. | N O F |
18.下列方案能够达到实验目的是( )
| A. | 用浓溴水除去苯中的苯酚 | |
| B. | 除去苯中的少量甲苯,先用酸性高锰酸钾溶液,后用氢氧化钠溶液处理 | |
| C. | 在加热条件下,用乙醇除去乙酸乙酯中的乙酸 | |
| D. | 将溴乙烷和氢氧化钠溶液混合加热后,再加入硝酸银溶液,检验溴元素 |
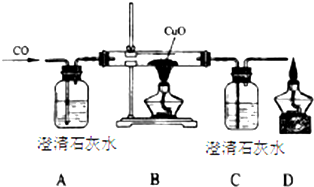 甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物.实验时,在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验.
甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物.实验时,在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验.