题目内容
16.下列关于有机物性质的叙述错误的是( )| A. | 甲烷和氯气在光照条件下反应产生油状液滴 | |
| B. | 乙烯能使溴的四氯化碳溶液褪色 | |
| C. | 苯能使酸性高锰酸钾溶液褪色 | |
| D. | 乙醇可以和金属钠反应放出氢气 |
分析 A.甲烷中H被Cl取代生成氯代烃;
B.乙烯中含碳碳双键,与溴发生加成反应;
C.苯与高锰酸钾不反应;
D.乙醇含-OH.
解答 解:A.甲烷中H被Cl取代生成氯代烃,则反应产生油状液滴,故A正确;
B.乙烯中含碳碳双键,与溴发生加成反应,则乙烯能使溴的四氯化碳溶液褪色,故B正确;
C.苯与高锰酸钾不反应,则苯不能使酸性高锰酸钾溶液褪色,故C错误;
D.乙醇含-OH,与Na反应生成氢气,故D正确;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意有机反应的判断,题目难度不大.

练习册系列答案
相关题目
6.下列实验设计及其对应的离子方程式均正确的是( )
| A. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ | |
| B. | Na2O2与H2O反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| C. | 将氯气溶于水制备次氯酸:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
4.下列除去杂质的方法不正确的是( )
| A. | 除去甲烷中少量的乙烯:气体通过溴水溶液的洗气瓶 | |
| B. | 除去乙酸乙酯中少量的乙酸:用氢氧化钠溶液洗涤,分液、干燥、蒸馏 | |
| C. | 除去CO2中少量的SO2:气体通过盛饱和碳酸氢钠氢溶液的洗气瓶 | |
| D. | 除去乙醇中少量的乙酸:加足量生石灰,蒸馏 |
11.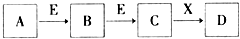 中学常见物质A、B、C、D、E、X,存在下图转化关系 (部分生成物和反应条件略去).下列推断不正确的是( )
中学常见物质A、B、C、D、E、X,存在下图转化关系 (部分生成物和反应条件略去).下列推断不正确的是( )
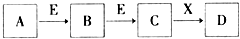 中学常见物质A、B、C、D、E、X,存在下图转化关系 (部分生成物和反应条件略去).下列推断不正确的是( )
中学常见物质A、B、C、D、E、X,存在下图转化关系 (部分生成物和反应条件略去).下列推断不正确的是( )| A. | 若D是一种强碱,则A、B、C均可与X反应生成D | |
| B. | 若D为NaCl,且A可与C反应生成B,则E可能是CO2 | |
| C. | 若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁 | |
| D. | 若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C |
1.下列关于放射性原子氡${\;}_{86}^{222}$Rn的说法正确的是( )
| A. | 原子的核外电子数为86 | B. | 中子数为86 | ||
| C. | Rn元素的相对原子量为222 | D. | 质子数为136 |
8.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 通常情况下,32gO2和O3的混合气体含有的分子总数小于NA | |
| B. | 常温常压下,0.1mol•L-1的硝酸铵溶液中氮原子数目为0.2NA | |
| C. | 1mol有机物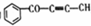 中最多有6NA个原子在一条直线上 中最多有6NA个原子在一条直线上 | |
| D. | 1mol甲基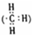 所含的电子数为7NA 所含的电子数为7NA |
5.下列说法中正确的一组是( )
| A. | H2和D2互为同位素 | B. |  和 和 互为同分异构体 互为同分异构体 | ||
| C. | 正丁烷和异丁烷是同系物 | D. | 正丁烷和异戊烷是同系物 |
6.下列不属于盐的是( )
| A. | NH4Cl | B. | MgO | C. | Fe2(SO4)3 | D. | NaHCO3 |