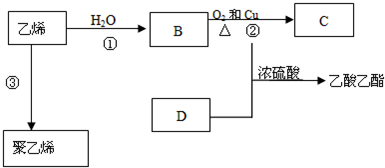
题目内容
13.下列化学方程式书写正确的是( )| A. | CO2+H2O+CaCl2═2HCl+CaCO3↓ | B. | 2NaCl+MgSO4═Na2SO4+MgCl2 | ||
| C. | 2HgO═2Hg+O2 | D. | 2KOH+CO2═K2CO3+H2O |
分析 A.碳酸不能制得盐酸;
B.复分解反应的条件是有沉淀、气体或水生成;
C.氧化汞分解要加热;
D.二氧化碳是酸性氧化物能与碱反应.
解答 解:A.碳酸是弱酸不能制得强酸盐酸,该反应不能发生,故A错误;
B.复分解反应的条件是有沉淀、气体或水生成,该反应不能发生,故B错误;
C.氧化汞分解要加热,反应方程式为2HgO$\frac{\underline{\;加热\;}}{\;}$2Hg+O2↑,故C错误;
D.二氧化碳是酸性氧化物能与碱反应生成盐和水,故D正确.
故选D.
点评 本题考查化学方程式的书写,明确反应原理、反应条件、沉淀气体符号、配平是解题关键,难度中等.

练习册系列答案
相关题目
3.向碘酸钠(NaIO3)的碱性溶液中通入氯气,可以得到钠盐Na2H3IO6.下列有关该反应的说法中错误的是( )
| A. | 在该反应中碘酸钠作还原剂 | |
| B. | 碱性条件下,氯气的氧化性强于高碘酸钠的氧化性 | |
| C. | 反应中氧化产物与还原产物的物质的量之比为2:1 | |
| D. | 反应中生成1 mol Na2H3IO6转移2 mol电子 |
4.下列除去杂质的方法不正确的是( )
| A. | 除去甲烷中少量的乙烯:气体通过溴水溶液的洗气瓶 | |
| B. | 除去乙酸乙酯中少量的乙酸:用氢氧化钠溶液洗涤,分液、干燥、蒸馏 | |
| C. | 除去CO2中少量的SO2:气体通过盛饱和碳酸氢钠氢溶液的洗气瓶 | |
| D. | 除去乙醇中少量的乙酸:加足量生石灰,蒸馏 |
1.下列关于放射性原子氡${\;}_{86}^{222}$Rn的说法正确的是( )
| A. | 原子的核外电子数为86 | B. | 中子数为86 | ||
| C. | Rn元素的相对原子量为222 | D. | 质子数为136 |
8.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 通常情况下,32gO2和O3的混合气体含有的分子总数小于NA | |
| B. | 常温常压下,0.1mol•L-1的硝酸铵溶液中氮原子数目为0.2NA | |
| C. | 1mol有机物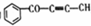 中最多有6NA个原子在一条直线上 中最多有6NA个原子在一条直线上 | |
| D. | 1mol甲基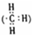 所含的电子数为7NA 所含的电子数为7NA |
5.下列说法中正确的一组是( )
| A. | H2和D2互为同位素 | B. |  和 和 互为同分异构体 互为同分异构体 | ||
| C. | 正丁烷和异丁烷是同系物 | D. | 正丁烷和异戊烷是同系物 |
2.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 1.7g OH- 所含电子数为0.8NA | |
| B. | 标准状况下,11.2L HCl 所含质子数为18NA | |
| C. | 常温下,11.2L Cl2所含原子数为NA | |
| D. | 0.5mol D2O 中所含质子数为5NA |
3.已知:a H2S(g)+b O2(g)═c X+d H2O(1)△H.当X为下列何种物质(状态)时,该反应热(△H)最小( )
| A. | S(s) | B. | S(g) | C. | SO2(l) | D. | SO2(g) |