题目内容
18.下列方案能够达到实验目的是( )| A. | 用浓溴水除去苯中的苯酚 | |
| B. | 除去苯中的少量甲苯,先用酸性高锰酸钾溶液,后用氢氧化钠溶液处理 | |
| C. | 在加热条件下,用乙醇除去乙酸乙酯中的乙酸 | |
| D. | 将溴乙烷和氢氧化钠溶液混合加热后,再加入硝酸银溶液,检验溴元素 |
分析 A.溴及三溴苯酚都能够溶于有机溶剂苯;
B.苯与Cu(OH)2悬浊液分层,乙醛与Cu(OH)2悬浊液反应生成砖红色沉淀,乙酸与Cu(OH)2悬浊液反应生成蓝色溶液;
C.乙醇溶于乙酸乙酯;
D.溴乙烷和NaOH溶液混合加热后,发生水解,但检验溴离子应在酸性条件下.
解答 解:A.溴和三溴苯酚都易溶于苯,会引入杂质,应该用NaOH溶液除去苯中的苯酚,故A错误;
B.苯与Cu(OH)2悬浊液分层,乙醛与Cu(OH)2悬浊液反应生成砖红色沉淀,乙酸与Cu(OH)2悬浊液反应生成蓝色溶液,现象不同,能鉴别,故B正确;
C.乙醇溶于乙酸乙酯,会引入杂质,则用饱和碳酸钠溶液除去乙酸乙酯中的乙酸,故C错误;
D.溴乙烷和NaOH溶液混合加热后,发生水解,应先加硝酸至酸性条件,再加入硝酸银溶液,检验溴元素,故D错误;
故选B.
点评 本题考查化学实验方案的评价,题目难度中等,涉及除杂、物质的鉴别、卤代烃水解等知识,侧重物质性质的考查,选项D为易错点,试题有利于提高学生的分析能力及化学实验能力.

练习册系列答案
相关题目
8.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 通常情况下,32gO2和O3的混合气体含有的分子总数小于NA | |
| B. | 常温常压下,0.1mol•L-1的硝酸铵溶液中氮原子数目为0.2NA | |
| C. | 1mol有机物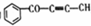 中最多有6NA个原子在一条直线上 中最多有6NA个原子在一条直线上 | |
| D. | 1mol甲基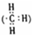 所含的电子数为7NA 所含的电子数为7NA |
9.下列图示与对应的叙述相符的是( )
| A. | 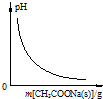 图表示向CH3COOH溶液中逐渐加入CH3COONa固体后,溶液pH的变化 | |
| B. | 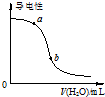 图表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b | |
| C. | 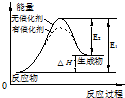 图表示催化剂能改变化学反应的焓变 | |
| D. | 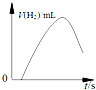 图表示表面有氧化膜的镁条投入稀盐酸中产生氢气的速率随时间的变化曲线 |
6.下列不属于盐的是( )
| A. | NH4Cl | B. | MgO | C. | Fe2(SO4)3 | D. | NaHCO3 |
13.金属铜的提炼多从黄铜矿(CuFeS2)开始,已知黄铜矿中铁为+2价.黄铜矿的焙烧过程中发生的主要反应为:2CuFeS2+O2=Cu2S+2FeS+SO2,下列说法不正确的是( )
| A. | SO2既是氧化产物又是还原产物 | |
| B. | CuFeS2既是氧化剂又是还原剂 | |
| C. | O2只做氧化剂 | |
| D. | 若有1mol O2参加反应,则反应中有4mol电子转移 |
3.已知:a H2S(g)+b O2(g)═c X+d H2O(1)△H.当X为下列何种物质(状态)时,该反应热(△H)最小( )
| A. | S(s) | B. | S(g) | C. | SO2(l) | D. | SO2(g) |
7.Mg-AgCl电池是一种以海水为电解质溶液的水激活电池.下列叙述错误的是( )
| A. | 负极反应式为Mg-2e-=Mg2+ | |
| B. | 正极反应式为Ag++e-=Ag | |
| C. | 电池放电时Cl-由正极向负极迁移 | |
| D. | 负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑ | |
| E. | 能被KCl溶液激活 | |
| F. | 可用于海上应急照明供电 |
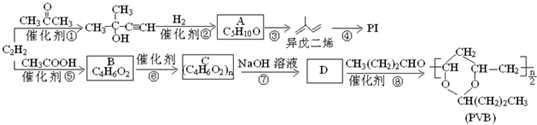

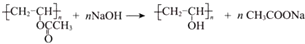 .
. ”改为“乙醛”,经过②、③、④后得到以顺式结构为主的高聚物,则用结构简式表示其顺式结构是
”改为“乙醛”,经过②、③、④后得到以顺式结构为主的高聚物,则用结构简式表示其顺式结构是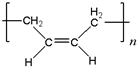 .
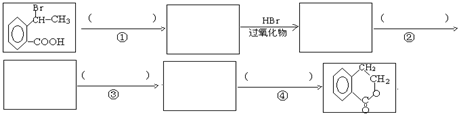
.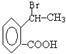 为原料合成
为原料合成 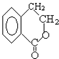 ,下列是合成流程图,在括号内注明反应条件,方框内写出有关物质的结构简式.
,下列是合成流程图,在括号内注明反应条件,方框内写出有关物质的结构简式.