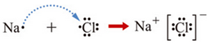��Ŀ����
12��ͼ��ʾ������֮���ת����ϵ����֪��������D��E��F��I��JΪ���壬H��I��J��Ϊ�����C����ɫ��ӦΪ��ɫ��MΪ���ɫ���壮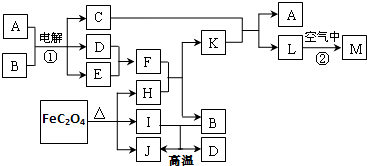
��1��д��K��Һ��E��Ӧ�����ӷ���ʽ2Fe2++Cl2=2Fe3++2Cl-������K�н��������ӵķ������ȵμ�KSCN��Һ���Ժ�ɫ���ټ�����ˮ�Ժ�ɫ�������Һ�еμ�NaOH��Һ��ˮ��������ɫ��״����¶���ڿ�����һ��ʱ�������Ϊ����ɫ������Ϊ���ɫ��˵����Fe2+��ʵ����������K��Һʱ��Ӧ��ô���������Ƚ��Ȼ������ܽ��������У��ټ�������ˮϡ�ͣ���������������
��2��д��Al��H��Ӧ���ɵ���2Al+3FeO $\frac{\underline{\;����\;}}{\;}$3Fe+Al2O3�������Ԫ��λ�����ڱ��е������ڢ����壬K��Һ��E��Ӧ���ɵĽ��������������13������
��3����֪��G�ֽ�õ���H��I��J���ߵ����ʵ�����ȣ���G�Ļ�ѧʽΪFeC2O4��
��4��д����A�ĵ���ʽ
 ����ͼ��A����ṹͼ�зָ�����IJ��ֽṹͼ�����жϷ���A����ṹͼ����AD��
����ͼ��A����ṹͼ�зָ�����IJ��ֽṹͼ�����жϷ���A����ṹͼ����AD��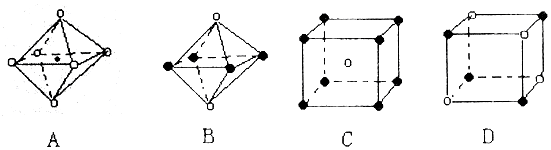
��5�����ڷ�Ӧ��ԭ���Ļ�ѧ��ҵ��Ϊ����ҵ�ϻ����Ե������A�������ֵ���X��E��Ŀǰ���������о�����һ�ָ��ܵ�أ����������ڵ�X��Y��Y��E�����Ԫ��ԭ��������1������Ϊ��������X���ӵ���Ħ�-Al2O3�մ����������ʣ���ӦʽΪ��2X+XY $?_{���}^{�ŵ�}$ X2Yx����д����طŵ�ʱ�����ĵ缫��Ӧʽ��xS+2e-=Sx2-���øõ������Դ���е�⺬��0.2mol CuSO4��0.2molA�Ļ����Һ500mLʱ�����˵�ع���һ��ʱ�������23gX���ʣ������������������Ϊ��6.72LL����״���£���������Һ��ˮϡ����2L����Һ��pHΪ��1��
���� L�����ڿ�������������ɫ�Ĺ���M����M��Fe��OH��3��L��Fe��OH��2��C����ɫ��ӦΪ��ɫ��˵��C������Ԫ�أ����A��B�Ļ�������ɺ�����Ԫ�صĻ������ͬʱ�����������壬���Ե�����NaCl��Һ����A��Bһ����NaCl��һ����H2O��B��һ�ֳ�������ɫҺ�壬ӦΪH2O����AΪNaCl��CΪNaOH��EΪ����ɫ���壬ӦΪCl2����DΪH2��FΪHCl��KΪFeCl2��HΪFeO��IΪCO������Ԫ���غ�֪DΪH2��J��CO2��
��1��K��Һ��E��Ӧ���Ȼ�������Һ������������Ӧ�����Ȼ�����K�н���������Ϊ�������ӣ��������������ɵ�������������������ɫ�仯���ʵ����飬ʵ����������K��ҺΪFeCl2����Ҫ��ֹ��������ˮ�⣻
��2��Al��HΪFeO��Ӧ���ɵ��ʣ����������û���Ӧ���������������ڱ���Ϊ�������ڵڢ����壻K��ҺΪFeCl2����EΪCl2������Ӧ���ɵĽ���������Ϊ�����ӣ�����ԭ�ӽṹ����������������
��3����֪��G�ֽ�õ���H��I��J���ߵ����ʵ�����ȣ�HΪFeO��IΪCO��J��CO2��ԭ���غ���ƽ��д�õ�G�Ļ�ѧʽ��
��4��AΪNaClΪ���ӻ����NaClΪ���ӻ��������������������ͨ�����Ӽ���϶��ɣ��Ȼ��ƾ����У�ÿ��Na+��Χͬʱ����������ĵȾ����6��Cl-ͬ��ÿ��Cl-��Χͬʱ����������ĵȾ����6��Na+������Na+��Cl-����λ������6����Na+��Cl-�������ݴ˷������
��5����Ӧ��ԭ���Ļ�ѧ��ҵ��Ϊ�ȼҵ����ӦʽΪ��2X+XY $?_{���}^{�ŵ�}$ X2Yx������ΪX�õ��ӷ�����ԭ��Ӧ���������23g�Ƶ���ת��1mol���ӣ���⺬��0.2mol CuSO4��0.2molA�Ļ����Һʵ�����ȵ��CuCl20.1mol��CuSO40.1mol�������ˮ0.3mol�����������������=n��Cl2��+n��O2��=$\frac{0.2}{2}$+$\frac{0.8}{4}$=0.3������õ�������������CuSO40.1mol�����H+���ɵ�ⷽ��ʽ�ɵù�ϵ��CuSO4-----2H+������������Ũ�ȵõ���ҺpH��
��� �⣺��1��K��Һ��E��Ӧ���Ȼ�������Һ������������Ӧ�����Ȼ�������Ӧ�����ӷ���ʽΪ��2Fe2++Cl2=2Fe3++2Cl-��K�н���������Ϊ�������ӣ��������������ɵ�������������������ɫ�仯���ʵ����飬����K�н��������ӵķ����ǣ��ȵμ�KSCN��Һ���Ժ�ɫ���ټ�����ˮ�Ժ�ɫ�������Һ�еμ�NaOH��Һ��ˮ��������ɫ��״����¶���ڿ�����һ��ʱ�������Ϊ����ɫ������Ϊ���ɫ��˵����Fe2+��ʵ����������K��ҺΪFeCl2����Ҫ��ֹ��������ˮ�⣬ʵ����������K��Һʱ���Ƚ��Ȼ������ܽ��������У��ټ�������ˮϡ�ͣ��������������ۣ�
�ʴ�Ϊ��2Fe2++Cl2=2Fe3++2Cl-���ȵμ�KSCN��Һ���Ժ�ɫ���ټ�����ˮ�Ժ�ɫ�������Һ�еμ�NaOH��Һ��ˮ��������ɫ��״����¶���ڿ�����һ��ʱ�������Ϊ����ɫ������Ϊ���ɫ��˵����Fe2+�����Ƚ��Ȼ������ܽ��������У��ټ�������ˮϡ�ͣ��������������ۣ�
��2��Al��H��Ӧ���ɵ��ʵĻ�ѧ����ʽΪ��2Al+3FeO$\frac{\underline{\;����\;}}{\;}$3Fe+Al2O3���������ڱ���Ϊ�������ڵڢ����壬K��ҺΪFeCl2����EΪCl2������Ӧ���ɵĽ���������Ϊ�����ӣ������ӽṹʾ��ͼΪ�� ������������Ϊ13��
������������Ϊ13��
�ʴ�Ϊ��2Al+3FeO$\frac{\underline{\;����\;}}{\;}$3Fe+Al2O3���ģ�����13��
��3����֪��G�ֽ�õ���H��I��J���ߵ����ʵ�����ȣ�HΪFeO��IΪCO��J��CO2��FeC2O4$\frac{\underline{\;\;��\;\;}}{\;}$FeO+CO��+CO2����Ԫ��ԭ���غ�����Ƴ�G�Ļ�ѧʽFeC2O4��
�ʴ�Ϊ��FeC2O4��
��4��NaClΪ���ӻ�������������������ӹ��ɣ�����ʽΪ�� ��������NaCl�����У�ÿ��Na+��Χͬʱ����������ĵȾ����6��Cl-ͬ��ÿ��Cl-��Χͬʱ����������ĵȾ����6��Na+��ͼA��������������������ӣ�����Χ����Ϊ�����ӣ�������������Aͼ������������ѡA��
��������NaCl�����У�ÿ��Na+��Χͬʱ����������ĵȾ����6��Cl-ͬ��ÿ��Cl-��Χͬʱ����������ĵȾ����6��Na+��ͼA��������������������ӣ�����Χ����Ϊ�����ӣ�������������Aͼ������������ѡA��
�ʴ�Ϊ�� ��A��
��A��
��5����Ӧ���ǵ�ⱥ��ʳ��ˮ����Ӧԭ���Ļ�ѧ��ҵ��Ϊ�ȼҵ�����ܵ�أ����������ڵ�X��Y��Y��E�����Ԫ��ԭ��������1������Ϊ��������X���ӵ���Ħ�-Al2O3�մ����������ʣ���ӦʽΪ��2X+XY $?_{���}^{�ŵ�}$ X2Yx��������S���ʵõ��ӷ�����ԭ��Ӧ��xS+2e-=Sx2-��
�������23g�Ƶ���ת��1mol���ӣ�
��⺬��0.2mol CuSO4��0.2molNaCl�Ļ����Һ��
�缫��ӦΪ������Ϊ��2Cl--2e-=Cl2����4OH--4e-=2H2O+O2��������Ϊ��Cu2++2e-=Cu�����ݵ����غ������
ʵ�����ȵ��CuCl20.1mol��CuSO40.1mol�������ˮ0.3mol��
���������������=n��Cl2��+n��O2��=$\frac{0.2}{2}$mol+$\frac{0.8}{4}$mol=0.3mol��
��������ڱ�״����=0.3mol��22.4L/mol=6.72L��
���CuSO40.1mol�����H+��
�ɵ�ⷽ��ʽ�ɵù�ϵ��CuSO4-----2H+��
n��H+��=0.1mol��2=0.2 c��H+��=$\frac{0.2}{2}$mol=0.1mol/l��
pH=1��
�ʴ�Ϊ��xS+2e-=Sx2-�� 6.72��1��
���� ���⿼�����������ʡ�����ת����ϵ����Ӧ������������жϡ�����ṹ��ԭ��غ͵��ԭ�����������ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�

 ������������ϵ�д�
������������ϵ�д�| A�� | CH2=CH-CH=CH2 1��3-����ϩ | |
| B�� | CH3COOCH2CH2OOCCH3 �Ҷ�������� | |
| C�� | CH3CH2CH��OH��CH3 3-���� | |
| D�� |  2-������ 2-������ |
| A�� | ����������������ɢϵ�ı��������Ǿ��ж�������� | |
| B�� | ����������һ���ǽ�����������������ﲻһ���Ǽ��������� | |
| C�� | ���ݻ������к�����Ŀ�Ķ��٣��ѻ������ΪһԪ�ᡢ��Ԫ�ᡢ��Ԫ��� | |
| D�� | ǿ�������Һ�ĵ�������һ��ǿ�����������Һ |
| A�� | MgO��Al2O3�ڹ�ҵ�������������²��ϣ�Ҳ�����ڵ�ⷨұ��Mg��Al | |
| B�� | ˮ��ұ���ø�ѹ���ȥ�����̳��������˽�������� | |
| C�� | �߿ճ���������̫�������ߣ��������������Ӧ3O2�T2O3�е��ʲμӣ�����������ԭ��Ӧ | |
| D�� | ��ˮ�м�����������ɱ������ |
| A�� | ��������̼ͨ����������ʹ������ag ��Ӧ��ת�Ƶ�����Ϊ $\frac{a{N}_{A}}{14}$ | |
| B�� | 1mol Cl2 ͨ��ˮ�У���n��HClO��+n��Cl-��+n��ClO-��=2NA | |
| C�� | ���³�ѹ�£�3�˺���ȩ�ı������к��е�ԭ������Ϊ0.4NA | |
| D�� | 2.24���ļ����к��е�C-H����Ϊ0.4NA |
| �� ���� | I A | ��A | ��A | ��A | ��A | ��A | ��A | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
��2������������ˮ���������ǿ����NaOH��������ǿ����HClO4�������Ե���Al��OH��3��
��3��A�ֱ���D��E��F��G��H�γɵĻ������У����ȶ���HF
��4��A��B��E��F��G��H�У�ԭ�Ӱ뾶˳����Na��P��Cl��N��F��H
��5����ҵ���Ʊ�C��ԭ��2Al2O3$\frac{\underline{\;ͨ��\;}}{\;}$4A1+3O2��
��6��B������������ˮ�����C��������������Ӧ�����ӷ���ʽAl��OH��3+OH-�TAlO2-+2H2O��
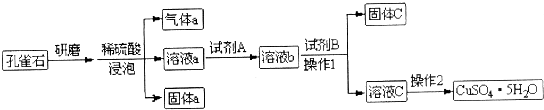
����ʵ��������̺�ʵ��Ŀ�ģ��ж�����˵���д�����ǣ�������
| A�� | ��ĥ��ȸʯ��Ŀ������������������Ӷ��ӿ췴Ӧ���� | |
| B�� | �Լ�AĿ���ǽ���Һ��Fe2+ת��ΪFe3+����ѡ��˫��ˮ�������� | |
| C�� | �Լ�BĿ������pH���ڼ���ʹFe3+ת��Ϊ���� | |
| D�� | �Լ�B����ѡ��NaOH��ˮ�ȼ����Լ� |
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| ��2���� | �� | �� | ||||||
| ��3���� | �� | �� | �� | �� | �� | �� | ||
| ��4���� | �� | �� |
��2��������������õĽ��������ӵĽṹʾ��ͼ��
 ��
����3���ȽϢڢۢ�����Ԫ�ص����Ӱ뾶��СCl-��F-��Mg2+
��4����ˮ����ĸ����������â�һ�����������ĵ���ϡ��Һ��Ӧ���ﵽ������ȡ��Ŀ�ģ�д�������ӷ���ʽSO2+Cl2+2H2O=4H++2Cl-+SO42-
��5�����һ��ʵ�飬�ȽϢۺ͢�����Ԫ�ؽ����Ե�ǿ��ȡ��ͬ��С��Mg��Al���ֱ����Ũ�ȵ����ᷴӦ��