题目内容
15.同温同压下,已知O2的密度为ρg•L-1,则Cl2的密度为( )| A. | $\frac{71ρ}{32}$g•L-1 | B. | $\frac{32ρ}{71}$g•L-1 | C. | $\frac{32}{71ρ}$g•L-1 | D. | $\frac{71}{32ρ}$g•L-1 |
分析 根据ρ=$\frac{M}{{V}_{m}}$可知相同条件下气体的密度与摩尔质量成正比,据此计算氯气的密度.
解答 解:同温同压下,气体摩尔体积相同,根据ρ=$\frac{M}{{V}_{m}}$可知相同条件下气体的密度与摩尔质量成正比,
已知O2的密度为ρg•L-1,则Cl2的密度=ρg•L-1×$\frac{71g/mol}{32g/mol}$=$\frac{71}{32}$ρg•L-1,
故选A.
点评 本题考查了物质的量的计算,题目难度不大,明确相同条件下气体密度与摩尔质量的关系为解答关键,试题侧重基础知识的考查,有利于提高学生的化学计算能力.

练习册系列答案
相关题目
2.下列说法正确的是( )
| A. | 氯气是一种紫色重要的化工原料 | |
| B. | 钠和钾的合金在常温下是固体 | |
| C. | 用二氧化硅具有很强的导光能力,可用于制作光缆 | |
| D. | 发酵粉中含有碳酸钠,能使焙制出的糕点疏松多孔 |
10.下列实验事故的处理方法正确的是( )
| A. | 实验桌上的酒精灯倾倒了燃烧起来,马上用湿布扑灭 | |
| B. | 不慎将酸或碱液溅入眼内,立即闭上眼睛,用手揉擦 | |
| C. | 皮肤上溅有较多的浓硫酸,赶紧用水冲洗 | |
| D. | 实验室金属钠着火,立即用水浇灭 |
20.设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
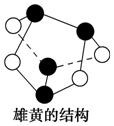

| A. | 25℃时,pH=2的1.0 L H2SO4溶液中含有H+的数目为0.02 NA | |
| B. | 0.5 mol雄黄(As4S4,所有原子都满足8电子结构,结构如图)含有NA个S-S键 | |
| C. | 39 g苯分子中共含6 NA个共价单键 | |
| D. | 向FeI2、NaBr的混合溶液中通入适量氯气,当有1 molFe2+被氧化时,该反应转移电子的数目至少为3 NA |
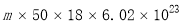 B.
B.
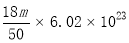 D.
D.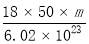
 实验室需要0.1mol/LNaOH溶液450ml和0.51mol/L硫酸溶液500ml,根据这两种溶液的配制情况回答下列问题:
实验室需要0.1mol/LNaOH溶液450ml和0.51mol/L硫酸溶液500ml,根据这两种溶液的配制情况回答下列问题: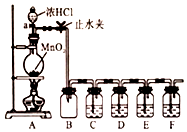 某化学学习小组为探究Cl2、Br2、I2、Fe3+的氧化性强弱,设计了如图实验装置:
某化学学习小组为探究Cl2、Br2、I2、Fe3+的氧化性强弱,设计了如图实验装置: