题目内容
10.下列实验事故的处理方法正确的是( )| A. | 实验桌上的酒精灯倾倒了燃烧起来,马上用湿布扑灭 | |
| B. | 不慎将酸或碱液溅入眼内,立即闭上眼睛,用手揉擦 | |
| C. | 皮肤上溅有较多的浓硫酸,赶紧用水冲洗 | |
| D. | 实验室金属钠着火,立即用水浇灭 |
分析 A.酒精易溶于水,可用沙子或湿抹布盖灭;
B.不慎将酸或碱液溅入眼内,应用大量的水冲洗;
C.浓硫酸溶于水放出大量的热;
D.钠与水反应生成氢气.
解答 解:A.酒精易溶于水,实验桌上的酒精灯倾倒了燃烧起来,可用沙子或湿抹布盖灭,故A正确;
B.不慎将酸或碱液溅入眼内,应用大量的水冲洗,不能闭上眼睛,用手揉擦,否则导致眼睛更为严重的损害,故B错误;
C.浓硫酸溶于水放出大量的热,会导致损害加剧,应先用干抹布拭去,再用大量的水冲洗,故C错误;
D.钠与水反应生成氢气,易爆炸,应用沙土扑灭,故D错误.
故选A.
点评 本题考查化学实验方案的评价,为高考常见题型,侧重考查学生的分析能力、实验能力,注意把握实验操作的方法以及注意事项,难度不大.

练习册系列答案
相关题目
17.现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液中提取乙醇 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
2.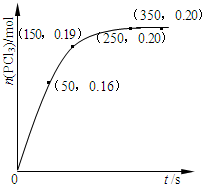 温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据如图.下列说法正确的是( )
温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据如图.下列说法正确的是( )
 温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据如图.下列说法正确的是( )
温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据如图.下列说法正确的是( )| A. | 反应在前50 s 的平均速率v(PCl3)=0.0032 mol•L-1•s-1 | |
| B. | 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol•L-1,则反应的△H<0 | |
| C. | 相同温度下,起始时向容器中充入2.0 mol PCl3和2.0mol Cl2,达到平衡时,PCl3 的转化率小于80% | |
| D. | 相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3 和0.20 mol Cl2,反应达到平衡前v(正)>v(逆) |
18.Ⅰ.氮的固定是几百年来科学家一直研究的课题.
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值.
①分析数据可知:大气固氮反应属于吸热(填“吸热”或“放热”)反应.
②分析数据可知;人类不适合大规模模拟大气固氮的原因K值小,正向进行的程度小(或转化率低),不适合大规模生产.
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(P1、P2)下随温度变化的曲线,如图所示的图示中,正确的是A(填“A”或“B”);比较p1、p2的大小关系:p2>pl.
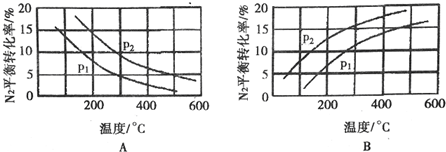
Ⅱ. 目前工业合成氨的原理是:N2(g)+3H2(g)?2NH3(g)
(3)在一定温度下,将1mol N2和3mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol.
①达平衡时,H2的转化率α1=60%.
②已知平衡时,容器压强为8MPa,则平衡常数Kp=0.26 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值.
| 反应 | 大气固氮N2(g)+O2(g)?2NO(g) | 工业固氮N2(g)+3H2(g)?2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.8×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
②分析数据可知;人类不适合大规模模拟大气固氮的原因K值小,正向进行的程度小(或转化率低),不适合大规模生产.
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(P1、P2)下随温度变化的曲线,如图所示的图示中,正确的是A(填“A”或“B”);比较p1、p2的大小关系:p2>pl.

Ⅱ. 目前工业合成氨的原理是:N2(g)+3H2(g)?2NH3(g)
(3)在一定温度下,将1mol N2和3mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol.
①达平衡时,H2的转化率α1=60%.
②已知平衡时,容器压强为8MPa,则平衡常数Kp=0.26 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
5.某同学需要用450mL 0.2000mol/L NaOH 溶液进行中和滴定实验,请你帮助他完成该溶液配制的相关实验步骤.
(1)他需要选择的主要仪器有托盘天平(砝码)、500mL容量瓶、胶头滴管、药匙、烧杯和玻璃棒;玻璃棒的作用是搅拌和引流.
(2)进行实验:
①该同学通过计算需要准确称量4.0g NaOH固体;
②将称量好的NaOH固体放在小烧杯中,加适量水使其溶解并恢复至室温;
③将溶液转移至事先试过漏的仪器中;
④用适量的蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部转入容器中;
⑤定容:先沿着玻璃棒向容量瓶中加入蒸馏水至距离刻度线1~2cm处,再改用胶头滴管滴加蒸馏水至凹液面与刻度线水平相切(填操作过程);
⑥振荡、摇匀、转移、装瓶.
(3)由于该同学态度不够端正,所以在实验过程中出现了一些不规范的操作,请你帮他认真分析一下这些操作对所配制溶液的浓度会造成怎样的影响,并将结果填入下表空白(填“偏高”、“偏低”或“无影响”).
(1)他需要选择的主要仪器有托盘天平(砝码)、500mL容量瓶、胶头滴管、药匙、烧杯和玻璃棒;玻璃棒的作用是搅拌和引流.
(2)进行实验:
①该同学通过计算需要准确称量4.0g NaOH固体;
②将称量好的NaOH固体放在小烧杯中,加适量水使其溶解并恢复至室温;
③将溶液转移至事先试过漏的仪器中;
④用适量的蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部转入容器中;
⑤定容:先沿着玻璃棒向容量瓶中加入蒸馏水至距离刻度线1~2cm处,再改用胶头滴管滴加蒸馏水至凹液面与刻度线水平相切(填操作过程);
⑥振荡、摇匀、转移、装瓶.
(3)由于该同学态度不够端正,所以在实验过程中出现了一些不规范的操作,请你帮他认真分析一下这些操作对所配制溶液的浓度会造成怎样的影响,并将结果填入下表空白(填“偏高”、“偏低”或“无影响”).
| 操 作 | 溶液浓度 |
| 砝码放在左盘、NaOH固体放右盘进行称量(1g以下使用游码) | ① |
| 转移溶液时有少量液体洒落到容器外 | ② |
| 定容时俯视刻度线 | ③ |
| 摇匀后观察到液面低于刻度线,立即补充水到凹液面与刻度线水平相切 | ④ |
15.同温同压下,已知O2的密度为ρg•L-1,则Cl2的密度为( )
| A. | $\frac{71ρ}{32}$g•L-1 | B. | $\frac{32ρ}{71}$g•L-1 | C. | $\frac{32}{71ρ}$g•L-1 | D. | $\frac{71}{32ρ}$g•L-1 |
19. 某同学欲用已知物质的量浓度为0.100 0mol•L-1的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某同学欲用已知物质的量浓度为0.100 0mol•L-1的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
(1)用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化.直到因加入一滴盐酸,溶液的颜色由红色变为无色,且半分钟不恢复原色,立即停止滴定.
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是D、E(填序号).
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
E.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出
(3)若第一次滴定开始和结束时,酸式滴定管中的液面如图所示.则起始读数为V1=9.00mL,终点读数V2=26.10mL.
(4)再结合表数据,计算被测氢氧化钠溶液的物质的量浓度是0.1710mol•L-1.
 某同学欲用已知物质的量浓度为0.100 0mol•L-1的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某同学欲用已知物质的量浓度为0.100 0mol•L-1的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:(1)用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化.直到因加入一滴盐酸,溶液的颜色由红色变为无色,且半分钟不恢复原色,立即停止滴定.
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是D、E(填序号).
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
E.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出
(3)若第一次滴定开始和结束时,酸式滴定管中的液面如图所示.则起始读数为V1=9.00mL,终点读数V2=26.10mL.
(4)再结合表数据,计算被测氢氧化钠溶液的物质的量浓度是0.1710mol•L-1.
| 滴定 | 待测溶液 体积/mL | 标准酸体积 | |
| 滴定前的刻度/mL | 滴定后的刻度/mL | ||
| 第一次 | 10.00 | V1 | V2 |
| 第二次 | 10.00 | 4.10 | 21.10 |
| 第三次 | 10.00 | 0.40 | 17.60 |
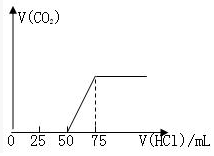 有50mLNaOH溶液,向其中逐渐通入一定量的CO2,随后向溶液中逐滴加入0.1mol•L-1的盐酸,产生的CO2气体体积(标准状况下)与所加入的盐酸的体积之间的关系如图所示:试分析向NaOH溶液中通入CO2气体后,所得溶液中的溶质是什么?其物质的量之比是多少?产生的CO2气体体积(标准状况)是多少?
有50mLNaOH溶液,向其中逐渐通入一定量的CO2,随后向溶液中逐滴加入0.1mol•L-1的盐酸,产生的CO2气体体积(标准状况下)与所加入的盐酸的体积之间的关系如图所示:试分析向NaOH溶液中通入CO2气体后,所得溶液中的溶质是什么?其物质的量之比是多少?产生的CO2气体体积(标准状况)是多少?