题目内容
14.下列说法不正确的是( )| A. | 生物质能来深于植物及其加工产品所贮存的能量,直接燃烧是利用方式之一 | |
| B. | 石油的裂化与裂解都是化学变化,而煤的气化与液化是物理变化 | |
| C. | 用高压氢气、氧气制作燃料电池是氢能源利用的一种重要方式 | |
| D. | 化学反应过程中反应物的总能量小于生成物的总能量,往往伴随热量的吸收 |
分析 A.生物质能就是太阳能以化学能形式贮存在生物质中的能量形式,它直接或间接地来源于绿色植物的光合作用;
B.煤的气化利用煤与水蒸气反应产生的H2和CO;煤的液化是将煤与H2在催化剂作用下转化为液体燃料或利用煤产生的H2和CO通过化学合成产生液体燃料或其他液体化工产品的过程;
C.用高压氢气、氧气制作燃料电池产物为水,无任何污染;
D.吸热反应中,反应物的总能量小于生成物的总能量.
解答 解:A.生物质能就是太阳能以化学能形式贮存在生物质中的能量形式,即以生物质为载体的能量,它直接或间接地来源于绿色植物的光合作用,所以生物质能来源于植物及其加工产品所贮存的能量,其主要利用形式有:直接燃烧、生物化学转化、热化学转换等,故A正确;
B.通过石油的裂化、裂解可以得到小分子化合物,石油的裂化、裂解是化学变化;煤的气化利用煤与水蒸气反应产生的H2和CO,属于化学变化;煤的液化是将煤与H2在催化剂作用下转化为液体燃料或利用煤产生的H2和CO通过化学合成产生液体燃料或其他液体化工产品的过程,属于化学变化,故B错误;
C.用高压氢气、氧气制作燃料电池产物为水,无任何污染,所以是氢能源利用的一种重要方式,故C正确;
D.反应物的总能量小于生成物的总能量时发生的反应是吸热反应,故D正确.
故选B.
点评 本题考查了生物质能、绿色化学、煤和石油的应用以及反应与能量的关系等知识,注意化学与生产和生活,题目难度不大.

练习册系列答案
相关题目
16.下列实验方法能达到实验目的是( )
| A. | 用淀粉溶液检验溶液中是否存在碘单质 | |
| B. | 用分液漏斗分离乙酸乙酯与乙醇的混合物 | |
| C. | 用NaOH溶液除去乙酸乙酯中混有的乙酸 | |
| D. | 用排水集气法收集氨气 |
2.用98%、密度为1.84g/cm3的浓H2SO4配制l mol/L的稀硫酸100mL,现给出下列可能用到仪器:
①100mL量筒;
②10mL量筒;
③50mL烧杯;
④托盘天平;
⑤100mL容量瓶;
⑥胶头滴管;
⑦玻璃棒
按使用仪器先后顺序排列正确的是( )
①100mL量筒;
②10mL量筒;
③50mL烧杯;
④托盘天平;
⑤100mL容量瓶;
⑥胶头滴管;
⑦玻璃棒
按使用仪器先后顺序排列正确的是( )
| A. | ②③⑦⑤⑥ | B. | ②⑤⑦⑥ | C. | ①③⑤⑦④⑥ | D. | ④③⑦ |
9.反应物X转化为Y和Z的能量变化如图所示,下列说法正确的是( )
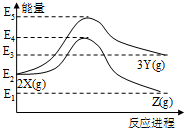

| A. | 由X→Y反应的△H=E5-E2 | |
| B. | 由X→Z反应的△H>0 | |
| C. | 由图可知等物质的量的Y的能量一定比X的能量高 | |
| D. | 升高温度可提高X→Z的反应速率 |
3.下列有关化学用语表示正确的是( )
| A. | 氧化钠的电子式: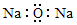 | |
| B. | 质子数为35、中子数为45的溴原子:${\;}_{35}^{80}$Br | |
| C. | 硫离子的结构示意图: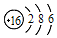 | |
| D. | CCl4的球棍模型: |
1.在某温度下2L密闭容器中,3种气体加入起始状态和平衡状态时的物质的量(n)如下表所示:
下列有关说法正确的是( )
| X | Y | W | |
| 起始状态(mol) | 2 | 1 | 0 |
| 平衡状态(mol) | 1 | 0.5 | 1.5 |
| A. | 该温度下,该反应的平衡常数K=9 | |
| B. | 升高温度,若W的体积分数减小,此反应△H>0 | |
| C. | 该温度下,该反应的方程式为 2X(g)+Y(g)?3W(g) | |
| D. | 增大压强,正、逆反应速率都增大,平衡向正反应方向移动 |