题目内容
2.用98%、密度为1.84g/cm3的浓H2SO4配制l mol/L的稀硫酸100mL,现给出下列可能用到仪器:①100mL量筒;
②10mL量筒;
③50mL烧杯;
④托盘天平;
⑤100mL容量瓶;
⑥胶头滴管;
⑦玻璃棒
按使用仪器先后顺序排列正确的是( )
| A. | ②③⑦⑤⑥ | B. | ②⑤⑦⑥ | C. | ①③⑤⑦④⑥ | D. | ④③⑦ |
分析 配制溶液的步骤为:计算、量取、稀释、冷却、转移、定容、摇匀、装瓶,结合实验步骤选择仪器,以此来解答.
解答 解:用98%的浓硫酸(密度为1.84g•cm-3)配制100mL1mol/L的稀硫酸,选择100mL容量瓶,设需要浓硫酸的体积为V,
由稀释前后溶质的物质的量不变,可知V×$\frac{1000×1.84×98%}{98}$=0.1L×1mol/L,
解得V=0.0054L=5.4mL,
应选择10mL量筒,
然后在50mL烧杯中稀释、转移到100mL容量瓶中定容,还需要玻璃棒、胶头滴管,
则按使用仪器的先后顺序为②③⑦⑤⑥,
故选A.
点评 本题考查配制一定物质的量的溶液,为高频考点,把握配制溶液的步骤、操作、仪器为解答的关键,侧重分析与应用能力的考查,注意容量瓶的选择,题目难度不大.

练习册系列答案
相关题目
4.下列离子能大量共存且溶液为无色透明的是( )
| A. | Na+、OH-、NO3-、HCO3- | B. | Na+、Fe3+、Cl-、SCN- | ||
| C. | Na+、Al3+、NO3-、Cl- | D. | K+、Cu2+、SO42-、OH- |
14.下列说法不正确的是( )
| A. | 生物质能来深于植物及其加工产品所贮存的能量,直接燃烧是利用方式之一 | |
| B. | 石油的裂化与裂解都是化学变化,而煤的气化与液化是物理变化 | |
| C. | 用高压氢气、氧气制作燃料电池是氢能源利用的一种重要方式 | |
| D. | 化学反应过程中反应物的总能量小于生成物的总能量,往往伴随热量的吸收 |
11.下列实验操作中正确的是( )
| A. | 配制450mL溶液需要用到450mL容量瓶 | |
| B. | 用酒精萃取碘水中的碘 | |
| C. | 称量NaOH 固体时,将NaOH 固体放在托盘天平左盘的纸上 | |
| D. | 蒸馏时,应将温度计水银球靠近蒸馏烧瓶的支管口 |
9.加热N2O5依次发生的分解反应为:①N2O5?N2O3+O2,②N2O3?N2O+O2;在2L密闭容器中充入8mol N2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol,则t℃时反应①的平衡常数为( )
| A. | 10.7 mol/L | B. | 8.5 mol/L | C. | 9.6 mol/L | D. | 10.2 mol/L |
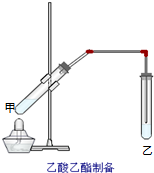 如图在试管甲中先加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5mL饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答:
如图在试管甲中先加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5mL饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答: 如图是实验室制乙酸乙酯的装置.
如图是实验室制乙酸乙酯的装置.