题目内容
10.已知反应:2CH3OH(g)?CH3OCH3(g)+H2O(g),某温度下的平衡常数为400.在此温度下,向密闭容器中加入一定量CH3OH,反应到5min时测得各组分的浓度如表所示:| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
(2)比较此时正、逆反应速率的大小:v正>v逆,理由是浓度商Qc=$\frac{0.6×0.6}{0.4{4}^{2}}$=1.36<K=400,反应向正反应进行.
(3)前5min时,用CH3OCH3表示该反应的速率为0.12mol/(L.min).
(4)再过一段时间后,反应达到平衡状态.能判断该反应已达到化学平衡状态的依据是B(填字母).
A.容器中压强不变 B.混合气体中c(CH3OH)不变
C.v生成(CH3OH)=2v消耗(H2O) D.c(CH3OCH3)=c (H2O)
(5)达到平衡状态时,CH3OH的转化率97.6%(计算结果保留到小数点后1位).
分析 (1)低温下(此时水为液态)能自发进行,而正反应为气体物质的量减小的反应,是熵减反应,△G=△H-T△S<0反应自发进行;
(2)计算浓度商Qc,若Qc=K,处于平衡状态,若Qc<K,反应向正反应进行,若Qc>K,反应向逆反应进行,进而判断v正、v逆相对大小;
(3)根据v=$\frac{△c}{△t}$计算用CH3OCH3表示该反应的速率;
(4)可逆反应到达平衡时,同种物质的正逆速率相等,各组分的浓度、含量保持不变,由此衍生的气体一些物理量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不再变化,说明反应到达平衡;
(5)由表中数据可知,甲醇的起始浓度为(0.44+0.6×2)mol/L=1.64mol/L,设平衡时甲醇浓度变化量为xmol/L,则:
2CH3OH(g)?CH3OCH3(g)+H2O(g)
起始量(mol/L):1.64 0 0
变化量(mol/L):x 0.5x 0.5x
平衡量(mol/L):1.64-x 0.5x 0.5x
根据平衡常数列方程计算解答.
解答 解:(1)低温下(此时水为液态)能自发进行,而正反应为气体物质的量减小的反应,是熵减反应,△G=△H-T△S<0反应自发进行,则△H<0,故答案为:<;
(2)浓度商Qc=$\frac{0.6×0.6}{0.4{4}^{2}}$=1.36<K=400,反应向正反应进行,则v正>v逆,
故答案为:>;浓度商Qc=$\frac{0.6×0.6}{0.4{4}^{2}}$=1.36<K=400,反应向正反应进行;
(3)前5min内,用CH3OCH3表示该反应的速率为$\frac{0.6mol/L}{5min}$=0.12mol/(L.min),
故答案为:0.12mol/(L.min);
(4)A.反应前后气体的物质的量不变,恒温下容器中压强始终不变,故A错误;
B.混合气体中c(CH3OH)不变,说明到达平衡,故B正确;
C.v生成(CH3OH)=2v消耗(H2O)均为逆反应速率,反应开始后始终为该比例关系,故C错误;
D.甲醚与水的按物质的量1:1生成,二者浓度始终相等,故D错误,
故选:B;
(5)由表中数据可知,甲醇的起始浓度为(0.44+0.6×2)mol/L=1.64mol/L,设平衡时甲醇浓度变化量为xmol/L,则:
2CH3OH(g)?CH3OCH3(g)+H2O(g)
起始量(mol/L):1.64 0 0
变化量(mol/L):x 0.5x 0.5x
平衡量(mol/L):1.64-x 0.5x 0.5x
所以$\frac{0.5x×0.5x}{(1.64-x)^{2}}$=400,解得x=1.6,甲醇的转化率为$\frac{1.6mol/L}{1.64mol/L}$×100%=97.6%,
故答案为:97.6%.
点评 本题考查化学平衡计算、反应速率计算、平衡状态判断、平衡常数应用等,注意掌握平衡常数的有关应用,难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 单位体积溶液里所含的溶质的物质的量,叫做物质的量浓度 | |
| B. | 气体摩尔体积就是22.4L mol- | |
| C. | 摩尔质量就是微粒的相对分子质量或者相对原子质量 | |
| D. | 物质的量就是物质的质量 |
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(CO2)(mol) | 0.40 | 0.35 | 0.31 | 0.3 | 0.3 | 0.3 |
(1)则a与b的关系是?(请写出计算过程,没有计算过程不得分)
(2)请补全反应方程式
1 CO2(g)+3H2(g)?1CH3OH(g)+1H2O(g)
| A. | H+、Na+、SO42-、HCO3-? | B. | Mg2+、K+、SO42-、OH- | ||
| C. | K+、Na+、Fe3+、NO3- | D. | Ba2+、OH-、NO3-、Na+ |
| A. | K+、H+、Cl-、OH- | B. | K+、H+、HCO3-、Cl- | ||
| C. | Fe2+、H+、Br-、OH- | D. | K+、NH4+、SO42-、Cl- |
 .
.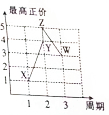 X、Y、Z、W、V是五种短周期主族元素,部分元素的周期序数与最高正价的关系如图所示.已知V元素的原子序数是下一周期同族元素的原子序数的一半.
X、Y、Z、W、V是五种短周期主族元素,部分元素的周期序数与最高正价的关系如图所示.已知V元素的原子序数是下一周期同族元素的原子序数的一半.