题目内容
18.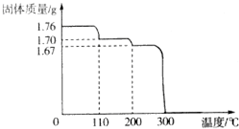 将1.76gHIO3固体样品放在热重分析仪中进行热重分析,测得其热重分析曲线(样品质量随温度变化的曲线)如图所示:
将1.76gHIO3固体样品放在热重分析仪中进行热重分析,测得其热重分析曲线(样品质量随温度变化的曲线)如图所示:(1)110℃和200℃均为样品的脱水过程,试确定200℃时是否脱水完全:是(填“是”或“否”).
(2)从200℃加热到300℃时发生的化学方程式为2I2O5$\frac{\underline{\;\;△\;\;}}{\;}$2I2↑+5O2↑.
分析 (1)发生2HIO3$\frac{\underline{\;\;△\;\;}}{\;}$I2O5+H2O,图象可知200℃时固体质量减少1.76g-1.67g=0.09g,结合反应计算;
(2)从200℃加热到300℃时,无固体剩余,则分解产物为碘、氧气.
解答 解:(1)图象可知200℃时固体质量减少1.76g-1.67g=0.09g,则
2HIO3$\frac{\underline{\;\;△\;\;}}{\;}$I2O5+H2O
2×176 18
x 0.09g,
则x=$\frac{2×176×0.09}{18}$=1.76g,则200℃时脱水完全,
故答案为:是;
(2)从200℃加热到300℃时,无固体剩余,则分解产物为碘、氧气,发生的反应为2I2O5$\frac{\underline{\;\;△\;\;}}{\;}$2I2↑+5O2↑,
故答案为:2I2O5$\frac{\underline{\;\;△\;\;}}{\;}$2I2↑+5O2↑.
点评 本题考查化学反应计算及图象的应用,为高频考点,把握图中质量变化及反应的对应关系为解答的关键,侧重分析与计算能力的考查,注意300℃时无固体剩余,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.40℃时,在氨-水体系中不断通入CO2,各种离子的变化趋势如图所示.下列说法不正确的是( )
| A. | 在pH=9.0时,c(NH4+)>c(HCO3-)>c(NH2COO-)>c(CO32-) | |
| B. | 如图随着CO2的通入,$\frac{{c(OH}^{-})}{{c(NH}_{3}•{H}_{2}O)}$不断减小 | |
| C. |  在如图所示不同pH的溶液中一定存在关系:c(NH4+)≥2c(CO32-)+c(HCO3-)+c(NH2COO-) | |
| D. | 在溶液pH不断降低的过程中,有含NH2COO-的中间产物生成 |
9.设NA为阿伏加德罗常数的值,下列叙述不正确的是( )
| A. | 46g乙醇中存在的共价键总数为8NA | |
| B. | 0.5 mol•L-1 CuCl2溶液中含有的Cl-个数为NA | |
| C. | 标准状况下,H2和CO混合气体8.96L在足量O2中充分燃烧消耗O2分子数为0.2NA | |
| D. | 在反应4Cl2+8NaOH═6NaCl+NaClO+NaClO3+4H2O中,消耗1mol Cl2时转移的电子总数为1.5NA |
13.下列有关物质检验的实验结论不正确的是( )
| 选项 | 实验操作现象 | 实验结论 |
| A | 向取了少量的KClO3晶体的试管中加入适量的蒸馏水,再向其中加入硝酸酸化的AgNO3溶液 | 该方法可以检验KClO3中是否含有氯元素 |
| B | 向某溶液中加入2滴KSCN溶液,溶液不显红色,再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有 Fe2+ |
| C | 将某气体通入品红溶液中,品红溶液褪色,将褪色溶液加热,品红颜色复原 | 该气体一定是SO2 |
| D | 向AgNO3溶液中加入足量的NaCl溶液,再加入KI溶液,再加入Na2S溶液,先后有白色沉淀变为黄色沉淀,最后又白色变为黑色沉淀 | Ksp(AgCl)>Ksp(AgI)>Ksp(Ag2S) |
| A. | A | B. | B | C. | C | D. | D |
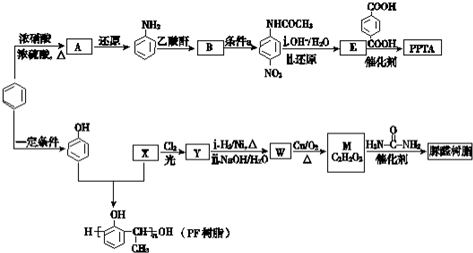
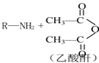 →R-NHCOCH2+CH2COOH(R为烃基)
→R-NHCOCH2+CH2COOH(R为烃基)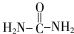 (尿素)氮原子上的氢原子可以像苯酚上的氢原子那样与甲醛发生加成反应,并缩聚成高分子.
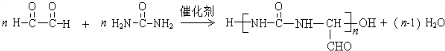
(尿素)氮原子上的氢原子可以像苯酚上的氢原子那样与甲醛发生加成反应,并缩聚成高分子. →B 的反应类型是取代反应.
→B 的反应类型是取代反应. .
. .
.
 .
.