题目内容
6.高分子化合物 PPTA 树脂、PF 树脂、脲醛树脂合成路线如下.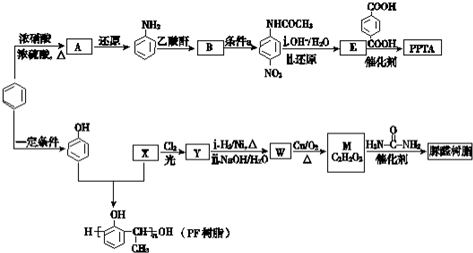
已知:
I.
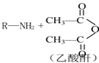 →R-NHCOCH2+CH2COOH(R为烃基)
→R-NHCOCH2+CH2COOH(R为烃基)II.
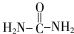 (尿素)氮原子上的氢原子可以像苯酚上的氢原子那样与甲醛发生加成反应,并缩聚成高分子.
(尿素)氮原子上的氢原子可以像苯酚上的氢原子那样与甲醛发生加成反应,并缩聚成高分子.(1)
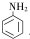 →B 的反应类型是取代反应.
→B 的反应类型是取代反应.(2)条件a选择的化学试剂是浓硝酸、浓硫酸.
(3)E中有两种不同化学环境的氢原子,PPTA 树脂的结构简式是
 .
.(4)W中只有一种含氧官能团.下列说法正确的是c.
a.Y分子中只有一种官能团
b.M与HCHO 互为同系物
c.W的沸点高于C2H6
(5)Y→W 时,条件ⅰ、ⅱ转化的官能团分别是醛基、氯原子.
(6)合成脲醛树脂的化学方程式是
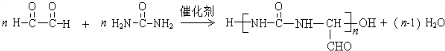 .
.
分析 苯发生硝化反应生成A为 ,苯胺与乙酸酐发生信息I中的反应生成B为
,苯胺与乙酸酐发生信息I中的反应生成B为 ,B在浓硝酸、浓硫酸并加热条件下发生取代反应生成
,B在浓硝酸、浓硫酸并加热条件下发生取代反应生成 ,再发生水解反应、还原反应得到E,E中有两种不同化学环境的氢原子,则E为
,再发生水解反应、还原反应得到E,E中有两种不同化学环境的氢原子,则E为 ,E与对苯二甲酸发生缩聚反应得到高聚物PPTA为
,E与对苯二甲酸发生缩聚反应得到高聚物PPTA为 .苯酚与X反应得到PF树脂,由PF的结构可知X为CH3CHO,X与氯气在光照条件下生成Y,Y能与氢气发生加成反应,再在氢氧化钠水溶液条件下发生水解反应W,则X中甲基上H原子被Cl原子取代,由于W氧化得到M,结合M的分子式可知,M为OHC-CHO,故W为HOCH2CH2OH,Y为ClCH2CHO,由题目信息Ⅱ可知,脲醛树脂为
.苯酚与X反应得到PF树脂,由PF的结构可知X为CH3CHO,X与氯气在光照条件下生成Y,Y能与氢气发生加成反应,再在氢氧化钠水溶液条件下发生水解反应W,则X中甲基上H原子被Cl原子取代,由于W氧化得到M,结合M的分子式可知,M为OHC-CHO,故W为HOCH2CH2OH,Y为ClCH2CHO,由题目信息Ⅱ可知,脲醛树脂为 ,据此解答.
,据此解答.
解答 解:苯发生硝化反应生成A为 ,苯胺与乙酸酐发生信息I中的反应生成B为
,苯胺与乙酸酐发生信息I中的反应生成B为 ,B在浓硝酸、浓硫酸并加热条件下发生取代反应生成
,B在浓硝酸、浓硫酸并加热条件下发生取代反应生成 ,再发生水解反应、还原反应得到E,E中有两种不同化学环境的氢原子,则E为
,再发生水解反应、还原反应得到E,E中有两种不同化学环境的氢原子,则E为 ,E与对苯二甲酸发生缩聚反应得到高聚物PPTA为
,E与对苯二甲酸发生缩聚反应得到高聚物PPTA为 .苯酚与X反应得到PF树脂,由PF的结构可知X为CH3CHO,X与氯气在光照条件下生成Y,Y能与氢气发生加成反应,再在氢氧化钠水溶液条件下发生水解反应W,则X中甲基上H原子被Cl原子取代,由于W氧化得到M,结合M的分子式可知,M为OHC-CHO,故W为HOCH2CH2OH,Y为ClCH2CHO,由题目信息Ⅱ可知,脲醛树脂为
.苯酚与X反应得到PF树脂,由PF的结构可知X为CH3CHO,X与氯气在光照条件下生成Y,Y能与氢气发生加成反应,再在氢氧化钠水溶液条件下发生水解反应W,则X中甲基上H原子被Cl原子取代,由于W氧化得到M,结合M的分子式可知,M为OHC-CHO,故W为HOCH2CH2OH,Y为ClCH2CHO,由题目信息Ⅱ可知,脲醛树脂为 .
.
(1) →B的反应中氨基中H原子被-COCH3取代,属于取代反应,
→B的反应中氨基中H原子被-COCH3取代,属于取代反应,
故答案为:取代反应;
(2) 在浓硝酸、浓硫酸并加热条件下发生取代反应生成
在浓硝酸、浓硫酸并加热条件下发生取代反应生成 ,
,
故答案为:浓硝酸、浓硫酸;
(3)由上述分析可知,PPTA树脂的结构简式是: ,
,
故答案为: ;
;
(4)a.Y为ClCH2CHO,分子中官能团有:氯原子、醛基,故a错误;
b.M为OHC-CHO,与HCHO不是同系物,故b错误;
c.W为HOCH2CH2OH,分子间存在氢键,沸点高于C2H6,故c正确,
故答案为:c;
(5)Y→W时,条件ⅰ为醛基与氢气发生加成反应,条件ⅱ为氯原子发生取代反应引入羟基,
故答案为:醛基;氯原子;
(6)合成脲醛树脂的化学方程式是: ,
,
故答案为: .
.
点评 本题考查有机物推断与合成,需要学生对给予的信息进行利用,能较好的考查学生自学能力与迁移运用能力,注意根据转化关系中的结结构简式、分子式与反应条件进行推断,熟练掌握官能团的性质与转化,难度中等.

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案| 族 周期 | ⅠA | 0 | ||||||
| 1 | A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | He |
| 2 | B | C | D | |||||
| 3 | E | F | G | H | I | J | K | L |
(2)下列有关元素性质的递变规律正确的是C
A.氢氧化物的碱性E<F<G B.获得电子的能力I>J>K
C.气态氢化物的稳定性D>K D.原子半径H<I<J<K
(3)对于第三周期的非金属元素(除Ar外),从左到右,原子半径逐渐减小,单质的氧化性逐渐增强,最高价氧化物对应水化物的酸性逐渐增强.
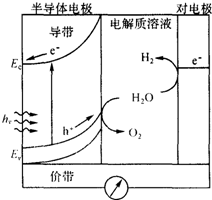 太阳能发电和阳光分解水制氢气,是清洁能源研究的主攻方向,研究工作之一集中在n-型半导体光电化学电池方面.如图是n-型半导体光电化学电池光解水制氢的基本原理示意图,图中的半导体导带是未充填电子的能级最低的能带,半导体价带是已充填价电子的能级最高的能带,图中的e-为电子、h+为空穴.在光照下,电子(e-)由价带跃迁到导带后,然后流向对电极.下列说法不正确的是( )
太阳能发电和阳光分解水制氢气,是清洁能源研究的主攻方向,研究工作之一集中在n-型半导体光电化学电池方面.如图是n-型半导体光电化学电池光解水制氢的基本原理示意图,图中的半导体导带是未充填电子的能级最低的能带,半导体价带是已充填价电子的能级最高的能带,图中的e-为电子、h+为空穴.在光照下,电子(e-)由价带跃迁到导带后,然后流向对电极.下列说法不正确的是( )| A. | 对电极表面发生的电极反应式为:4H++4e-→2H2 | |
| B. | 电池的总反应式为:2H2O$\stackrel{hv}{→}$O2+2H2↑ | |
| C. | 整个过程中实现了太阳能向电能化学能等的转化 | |
| D. | 装置中电流的方向是从半导体电极流向对电极 |
| A. | 向硫酸铝溶液中加入少量的氨水:Al3++3OH-═Al(OH) 3↓ | |
| B. | 向碳酸钠溶液中加入饱和石灰水:Ca(OH)2+CO32-═CaCO3↓+2OH- | |
| C. | 向氢氧化钠溶液中通入过量的氯气:Cl2+2OH-═ClO-+Cl-+H2O | |
| D. | 向稀硫酸中加入过量铁粉,先后发生两个反应:2Fe+6H+═2Fe3++3H2↑,Fe+2Fe3+═3Fe2+ |
| A. | 氢氧化钠 | B. | 亚硫酸钠 | C. | 氯化亚铁 | D. | 苯酚 |
| A. | 体积相等时具有的质量相等 | B. | 分子数相等时具有的中子数相等 | ||
| C. | 质量相等时具有的质子数相等 | D. | 体积相等时具有的原子数相等 |
| A. | 原子半径:Na<Mg<Al | B. | 热稳定性:HCl>HBr>HI | ||
| C. | 酸性强弱:H2SiO4<H2CO3<H2SO4 | D. | 熔点:SiO2>NaCl>CO2 |
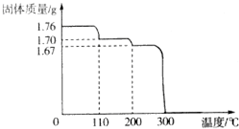 将1.76gHIO3固体样品放在热重分析仪中进行热重分析,测得其热重分析曲线(样品质量随温度变化的曲线)如图所示:
将1.76gHIO3固体样品放在热重分析仪中进行热重分析,测得其热重分析曲线(样品质量随温度变化的曲线)如图所示: