题目内容
11.硼是第IIIA族元素,单质硼在加热条件下能与多种非金属反应.某同学欲利用氯气和单质硼反应制备三氯化硼.已知BCl3的沸点为12.5℃,熔点为-107.3℃,遇水剧烈反应.(1)选用如图所示的装置(可以重复选用)进行实验,装置依次连接的合理顺序为ABDCEDF.
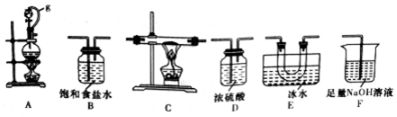
(2)图中g管的作用是保持气压平衡,便于分液漏斗中的液体流入蒸馏烧瓶,装置E的作用是冷凝并收集BCl3.
(3)开始实验时,先点燃A(填“A”或“B”)处的酒精灯.
(4)请写出BCl3遇水变质的化学方程式BCl3+3H2O=H3BO3+3HCl.
(5)硼酸是一元弱酸,其钠盐化学式为Na,则硼酸在水中电离方程式是H3BO3+H2O?[B(OH)4]-+H+.
(6)实验完成后,某同学向F (溶液中含有0.05mol/LNaC1 0、0.05mol/LNaCl、0.1mol/L NaOH)中滴加品红溶液,发现溶液褪色.现设计实验探究溶液褪色的原因,请将表中数据补充完整,完成实验方案.
| 实验序号 | 0.1mol/LNaClO溶液/mL | 0.1mol/LNaCl溶液/mL | 0.2mol/LNaOH溶液/mL | H2O/mL | 品红溶液 | 现象 |
| ① | 4.0 | 0 | 0 | x | 3滴 | 较快褪色 |
| ② | 0 | 4.0 | 4.0 | 0 | 3滴 | 不褪色 |
| ③ | 4.0 | 0 | 4.0 | 0 | 3滴 | 缓慢褪色 |
分析 用氯气和单质硼反应制备三氯化硼:在加热条件下,二氧化锰和浓盐酸发生氧化还原反应生成Cl2,但浓盐酸具有挥发性,水被加热也能蒸发,升高温度加快浓盐酸挥发、加快水蒸发,所以生成的Cl2中含有HCl、H2O,浓硫酸具有吸水性,饱和食盐水能吸收Cl2,浓硫酸能干燥气体,从而得到较纯净的Cl2,防止生成的B和HCl、BCl3水解;C中制得BCl3,然后用E得到BCl3固体,为防止生成的BCl3水解E装置之后需要干燥装置,F吸收未反应的Cl2,据此分析解答.
解答 解:(l)A中二氧化锰和浓盐酸发生氧化还原反应生成Cl2,生成的Cl2中含有HCl、H2O,故连接B装置用饱和食盐水吸收氯化氢,再连接D装置浓硫酸吸水干燥,C中生成BCl3,用E得到BCl3固体,为防止生成的BCl3水解E装置之后需要干燥装置D,最后用F吸收未反应的Cl2;
故答案为:ABDCEDF;
(2)g管的作用是保持气压平衡,便于分液漏斗中的液体流入蒸馏烧瓶,BC13的沸点为12.5℃,熔点为-107.3℃,故用E装置冰水冷凝并收集BC13;
故答案为:保持气压平衡,便于分液漏斗中的液体流入蒸馏烧瓶;冷凝并收集BCl3;
(3)开始实验时:先点燃A处酒精灯,待整套装置中都充满Cl2后再点燃D处酒精灯,使之发生反应;
故答案为:A;
(4)BCl3遇水变质生成HCl和H3BO3,反应为:BCl3+3H2O=H3BO3+3HCl;
故答案为:BCl3+3H2O=H3BO3+3HCl;
(5)硼酸是一元弱酸,其钠盐化学式为Na[B(OH)4〕,硼酸在水中电离方程式是:H3BO3+H2O?[B(OH)4]-+H+;
故答案为:H3BO3+H2O?[B(OH)4]-+H+;
(6)向F中(溶液含有0.05mol/LNaC10、0.05mol/LNaCl、0.1mol/LN a0H)滴加品红溶液,发现溶液褪色.探究溶液褪色的原因,三组对比试验应溶液总体积相同,都为8mL溶液,故实验②氢氧化钠溶液为4.0mL,实验①③褪色,说明NaClO使品红溶液褪色,实验③褪色较慢,则溶液碱性越强褪色越慢;
故答案为:4.0;NaClO使品红溶液褪色,溶液碱性越强褪色越慢.
点评 本题考查性质实验方案设计,侧重考查学生知识综合应用、实验基本操作能力及实验方案设计能力,综合性较强,题目难度中等.

| A. | 大力发展电动车,减少燃油汽车的尾气排放量 | |
| B. | 开发利用各种新能源,减少对化石燃料的依赖 | |
| C. | PM2.5含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素 | |
| D. | 多环芳烃是强致癌物,能吸附在PM2.5的表面进入人体 |
( )
| A. | 若混合后溶液中c(H+)>c(OH-),则一定有V1<V2 | |
| B. | 若V1=V2,则二者混合后的溶液中pH>7 | |
| C. | 混合溶液中可能存在:c ( F-)>c (H+)>c (Na+)>c( OH-) | |
| D. | 二者恰好反应完时,则所得溶液中c(F-)=c (Na+) |
| A. | C2H4O2 | B. | C3H6O3 | C. | C4H6O4 | D. | C6H12O6 |
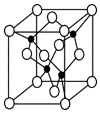 X、Y、Z、U、W 是原子序数依次增大的前四周期元素.其中 Y 的原子核外有 7 种运动状态不同的 电子;X、Z 中未成对电子数均为 2;U 是第三周期元素形成的简单离子中半径最小的元素;W 的内层电 子全充满,最外层只有 1 个电子.请回答下列问题:
X、Y、Z、U、W 是原子序数依次增大的前四周期元素.其中 Y 的原子核外有 7 种运动状态不同的 电子;X、Z 中未成对电子数均为 2;U 是第三周期元素形成的简单离子中半径最小的元素;W 的内层电 子全充满,最外层只有 1 个电子.请回答下列问题: .
.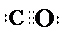 .
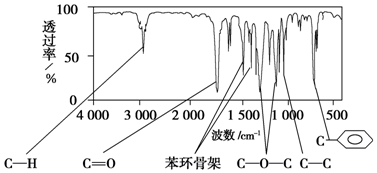
.
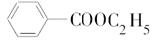 .
.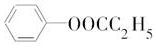 .
.