题目内容
3.二氧化铈(CeO2)是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质).某课题组以此粉末为原料,设计如图工艺流程对资源进行回收,得到纯净的CeO2和硫酸亚铁铵晶体.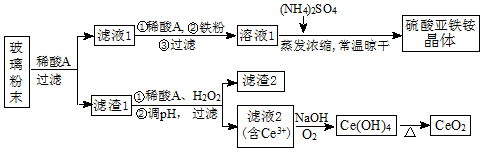
已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液.
(1)稀酸A的分子式是H2SO4;滤液1中加入铁粉的目的是把Fe3+还原为Fe2+.
(2)设计实验证明滤液1中含有Fe2+:用试管取少量酸性高锰酸溶液(或溴水),向试管中滴加过量滤液1若紫红(红棕)色褪色则滤液1中含有Fe2+[或取少许滤液1,滴加铁氰化钾溶液,有蓝色沉淀生成则证明滤液1中有Fe2+].
(3)由滤渣1生成Ce3+的化学方程式为2CeO2+H2O2+3H2SO4=Ce2(SO4)3+O2↑+4H2O.
(4)由滤液2生成Ce(OH)4的离子方程式为4Ce3++O2+12OH-+2H2O═4Ce(OH)4↓.
(5)硫酸铁铵晶体[Fe2(SO4)3•2(NH4)2SO4•3H2O]广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是存在水解反应Fe3++3H2O?Fe(OH)3+3H+,酸性废水中的H+抑制了Fe3+的水解(或水解平衡逆向移动),使其不能生成有吸附作用的Fe(OH)3胶体.
(6)取上述流程中得到的Ce(OH)4产品0.531g,加硫酸溶解后,用浓度为0.l000mol•L-1FeSO4标准溶液滴定至终点时(铈被还原为Ce3+ ),消耗25.00mL标准溶液.该产品中Ce(OH)4的纯度的表达式为:$\frac{0.1×25×1{0}^{-3}×208}{0.531}×100%$(或0.98、98%)(不必计算出结果).
分析 反应过程为:废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)中加入稀硫酸,FeO转化为FeSO4、Fe2O3转化Fe2(SO4)3存在于滤液1中,滤渣1为CeO2和SiO2;
滤液1中加入稀硫酸和铁粉,被Fe2(SO4)3还原为FeSO4,溶液1为FeSO4溶液,加入硫酸铵混合蒸发浓缩、常温晾干后得到硫酸亚铁铵晶体;
滤渣1中加入稀硫酸和H2O2,CeO2转化为Ce3+存在于滤液2中,反应为2CeO2+H2O2+3H2SO4=Ce2(SO4)3+O2↑+4H2O,滤渣2为SiO2;滤液2加入碱并通入氧气将Ce从+3氧化为+4后Ce3+转化为沉淀Ce(OH)4,反应为:4Ce 3++O2+12OH-+2H2O═4Ce(OH)4↓,加入分解Ce(OH)4得到产品CeO2;据此分析作答.
解答 解:(1)已知:CeO2不溶于稀硫酸,废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)中也不SiO2溶于酸,加入稀硫酸可将CeO2和SiO2与Fe2O3、FeO分离,滤液1中加入铁粉的目的是把Fe3+还原为Fe2+;
故答案为:H2SO4; 把Fe3+还原为Fe2+;
(2)亚铁离子有还原性能使酸性高锰酸钾褪色,也与铁氰化钾生成蓝色沉淀,故证明滤液1中含有Fe2+方法为:用试管取少量酸性高锰酸溶液(或溴水),向试管中滴加过量滤液1若紫红(红棕)色褪色则滤液1中含有Fe2+[或取少许滤液1,滴加铁氰化钾溶液,有蓝色沉淀生成则证明滤液1中有Fe2+];
故答案为:用试管取少量酸性高锰酸溶液(或溴水),向试管中滴加过量滤液1若紫红(红棕)色褪色则滤液1中含有Fe2+[或取少许滤液1,滴加铁氰化钾溶液,有蓝色沉淀生成则证明滤液1中有Fe2+];
(3)滤渣1为CeO2和SiO2,加入稀硫酸和H2O2,CeO2转化为Ce3+,则过氧化氢中氧元素化合价升高生成氧气,离子方程式为:2CeO2+H2O2+3H2SO4=Ce2(SO4)3+O2↑+4H2O;
故答案为:2CeO2+H2O2+3H2SO4=Ce2(SO4)3+O2↑+4H2O;
(4)滤液2为含有Ce 3+的溶液,加入碱并通入氧气将Ce从+3氧化为+4后Ce3+转化为沉淀Ce(OH)4,离子方程式为:4Ce 3++O2+12OH-+2H2O═4Ce(OH)4↓;
故答案为:4Ce 3++O2+12OH-+2H2O═4Ce(OH)4↓;
(5)硫酸铁铵晶体[Fe2(SO4)3•2(NH4)2SO4•3H2O]溶于水后,由于存在水解反应Fe3++3H2O?Fe(OH)3+3H+,酸性废水中的H+抑制了Fe3+的水解(或水解平衡逆向移动),使其不能生成有吸附作用的Fe(OH)3胶体;
故答案为:存在水解反应Fe3++3H2O?Fe(OH)3+3H+,酸性废水中的H+抑制了Fe3+的水解(或水解平衡逆向移动),使其不能生成有吸附作用的Fe(OH)3胶体;
(6)用0.1000mol/LFeSO4溶液滴定至终点,铈被还原成Ce3+,则Fe2+被氧化为Fe3+,则
Ce(OH)4~Ce3+~FeSO4
所以n(Ce(OH)4)=n(FeSO4)=0.1×25×10-3mol,m(Ce(OH)4)=0.1×25×10-3×208g,该产品中Ce(OH)4的纯度的表达式为$\frac{0.1×25×1{0}^{-3}×208}{0.531}×100%$=98%;
故答案为:$\frac{0.1×25×1{0}^{-3}×208}{0.531}×100%$(或0.98、98%).
点评 本题考查了物质的制备,涉及对工艺流程的理解、氧化还原反应、水解平衡的应用、物质纯度的计算等,理解工艺流程原理是解题的关键,是对学生综合能力的考查,需要学生具备扎实的基础与灵活运用能力,题目难度中等.

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案| A. | 用分液漏斗分离乙醇和乙酸乙酯的混合物 | |
| B. | 新制氯水或浓硝酸存放在带橡皮塞的棕色玻璃瓶中 | |
| C. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 | |
| D. | 加热蒸发NaCl溶液时应用玻璃棒不断搅拌 |
(1)选用如图所示的装置(可以重复选用)进行实验,装置依次连接的合理顺序为ABDCEDF.
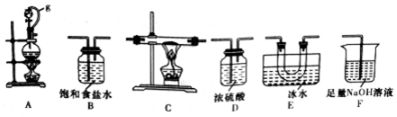
(2)图中g管的作用是保持气压平衡,便于分液漏斗中的液体流入蒸馏烧瓶,装置E的作用是冷凝并收集BCl3.
(3)开始实验时,先点燃A(填“A”或“B”)处的酒精灯.
(4)请写出BCl3遇水变质的化学方程式BCl3+3H2O=H3BO3+3HCl.
(5)硼酸是一元弱酸,其钠盐化学式为Na,则硼酸在水中电离方程式是H3BO3+H2O?[B(OH)4]-+H+.
(6)实验完成后,某同学向F (溶液中含有0.05mol/LNaC1 0、0.05mol/LNaCl、0.1mol/L NaOH)中滴加品红溶液,发现溶液褪色.现设计实验探究溶液褪色的原因,请将表中数据补充完整,完成实验方案.
| 实验序号 | 0.1mol/LNaClO溶液/mL | 0.1mol/LNaCl溶液/mL | 0.2mol/LNaOH溶液/mL | H2O/mL | 品红溶液 | 现象 |
| ① | 4.0 | 0 | 0 | x | 3滴 | 较快褪色 |
| ② | 0 | 4.0 | 4.0 | 0 | 3滴 | 不褪色 |
| ③ | 4.0 | 0 | 4.0 | 0 | 3滴 | 缓慢褪色 |
| A. | 植物油久置会出现油脂的酸败现象,是因为油脂发生了水解 | |
| B. | 有机玻璃、合成橡胶、涤纶都是由加聚反应制得的 | |
| C. | 糖类、油脂、蛋白质的水解产物都是非电解质 | |
| D. | 将已成熟的水果放入未成熟的水果中并密封,可加速水果成熟 |
(2)如图2所示,每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化.每个小黑点代表一种氢化物,其中a点代表的是SiH4.
(3)化合物(CH3)3N与盐酸反应生成【(CH3)3 NH】+,该过程新生成的化学键为b.(填序号)
a.离子键 b.配位键 c.氢键 d.非极性共价键
若化合物(CH3)3N能溶于水,试解析其原因化合物(CH3)3N为极性分子且可与水分子间形成氢键
(4)CO2在高温高压下所形成的晶体其晶胞如图3所示.该晶体的熔点比SiO2晶体高(选填“高”或“低”),该晶体中碳原子轨道的杂化类型为sp3.
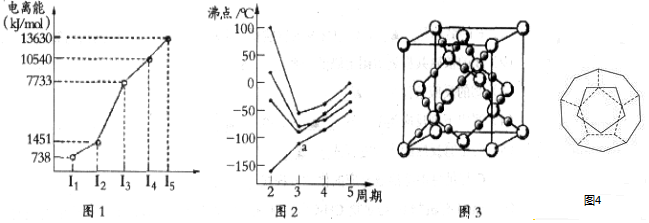
(5)如图4为20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成如图.C20分子中每个碳原子只跟相邻的3个碳原子形成化学键;
则:C20分子共有12个正五边形,共有30条棱边.
(6)Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律.试推断Ni2+的水合离子为有(填“有”或“无”)色离子,依据是Ni2+的3d轨道上有未成对电子.
| 离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
| 颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
| A. | 氯化钠 | B. | 氯气 | C. | 小苏打 | D. | 明矾 |