题目内容
16.某有机物A的分子式为C9H10O2,其核磁共振氢谱有5个峰,面积之比为1:2:2:2:3,红外光谱如图: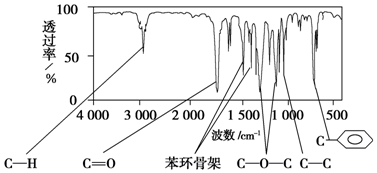
已知,A分子中只含一个苯环,且苯环上只有一个取代基,A与NaOH溶液共热的两种生成物均可用于食品工业(常见防腐剂和饮品),试填空.
(1)A的结构简式为
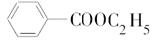 .
.(2)A的分子结构中只含一个甲基的依据是bc(填序号).
a.A的相对分子质量 b.A的分子式
c.A的核磁共振氢谱图 d.分子的红外光谱图
(3)A的芳香类同分异构体有多种,其中符合下列条件:①分子结构中只含一个官能团;②分子结构中含有一个甲基;③苯环上只有一个取代基,则A的芳香类同分异构体共有5种(不包括A本身),其中水解产物能使FeCl3溶液变紫色的结构简式为
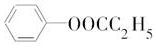 .
.
分析 (1)某有机物A的分子式为C9H10O2,A分子中只含一个苯环,且苯环上只有一个取代基,则苯环上的H的类型有3种,氢原子数目之比为1:2:2,其核磁共振氢谱有5个峰,面积之比为1:2:2:2:3,则另外的2个峰2:3来自侧链;A与NaOH溶液共热的两种生成物均可用于食品工业(常见防腐剂和饮品),结合A的红外光谱可知A分子中含有酯基,据此可判断A的结构;
(2)通过A的分子式和核磁共振氢谱可判断H的类型,从而确定含有甲基,而相对分子质量和红外光谱无法确定是否含有甲基;
(3)A的芳香类同分异构体有多种,其中符合下列条件:①分子结构中只含一个官能团,可能为羧基或酯基;②分子结构中含有一个甲基;③苯环上只有一个取代基,侧链为-OOCH2CH2CH3,或-CH2OOCCH3,或-COOCH2CH3,或-CH(CH3)OOCH,或-CH(CH3)COOH;水解产物能使FeCl3溶液变紫色,说明分子中含有酚羟基,据此判断满足体积的有机物的结构简式.
解答 解:(1)机物A的分子式为C9H10O2,A分子中只含一个苯环,且苯环上只有一个取代基,则苯环上的H的类型有3种,氢原子数目之比为1:2:2,其核磁共振氢谱有5个峰,面积之比为1:2:2:2:3,则另外的2个峰2:3来自侧链;A与NaOH溶液共热的两种生成物均可用于食品工业(常见防腐剂和饮品),结合A的红外光谱可知A分子中含有酯基,则A为苯甲酸乙酯,其结构简式为: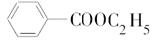 ,
,
故答案为: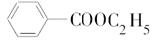 ;
;
(2)通过A的分子式C9H10O2及核磁共振氢谱有5个峰,面积之比为1:2:2:2:3可确定A分子中含有1个甲基,而A的相对分子质量、红外光谱都无法确定是否含有甲基,故bc正确,
故答案为:bc;
(3)A的芳香类同分异构体有多种,其中符合下列条件:①分子结构中只含一个官能团,可能为羧基或酯基;②分子结构中含有一个甲基;③苯环上只有一个取代基,侧链为-OOCH2CH2CH3,或-CH2OOCCH3,或-COOCH2CH3,或-CH(CH3)OOCH,或-CH(CH3)COOH,共有5种;
其中水解产物能使FeCl3溶液变紫色,说明有机物分子水解产物中含有酚羟基,其结构简式为: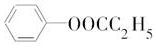 ,
,
故答案为:5;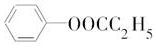 .
.
点评 本题考查有机物结构与性质,题目难度中等,正确推断A的结构为解答关键,注意熟练掌握常见有机物组成、结构与性质,试题有利于提高学生的分析、理解能力及逻辑推理能力.

| A. | 晶体硅是良好的半导体材料 | |
| B. | 铁、铝合金的熔点高于铁的熔点,硬度小 | |
| C. | 氨常用作制冷剂利用了氨的化学性质 | |
| D. | 漂白粉、明矾都可用于污水的净化,其原理是相同的 |
①臭氧的体积分数越大的空气越有利于人体健康
②煤燃烧时加入适量的石灰石,可减少废气中SO2的量
③PH在5.6~7.0之间的降水通常称为酸雨
④汽车尾气中含有氮氧化物、碳氧化物、含铅化合物等,严重污染大气.
| A. | ①③ | B. | ①④ | C. | ③④ | D. | ②④ |
| A. | CH2=CH2 | B. | CH≡C-CH3 | C. | CH2=CH-CH=CH2 | D. | CH3-CH=CH2 |
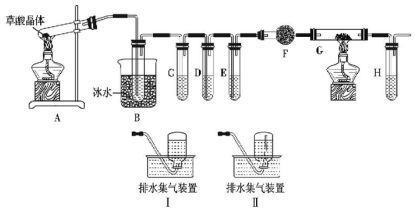
(1)选用如图所示的装置(可以重复选用)进行实验,装置依次连接的合理顺序为ABDCEDF.
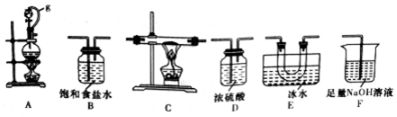
(2)图中g管的作用是保持气压平衡,便于分液漏斗中的液体流入蒸馏烧瓶,装置E的作用是冷凝并收集BCl3.
(3)开始实验时,先点燃A(填“A”或“B”)处的酒精灯.
(4)请写出BCl3遇水变质的化学方程式BCl3+3H2O=H3BO3+3HCl.
(5)硼酸是一元弱酸,其钠盐化学式为Na,则硼酸在水中电离方程式是H3BO3+H2O?[B(OH)4]-+H+.
(6)实验完成后,某同学向F (溶液中含有0.05mol/LNaC1 0、0.05mol/LNaCl、0.1mol/L NaOH)中滴加品红溶液,发现溶液褪色.现设计实验探究溶液褪色的原因,请将表中数据补充完整,完成实验方案.
| 实验序号 | 0.1mol/LNaClO溶液/mL | 0.1mol/LNaCl溶液/mL | 0.2mol/LNaOH溶液/mL | H2O/mL | 品红溶液 | 现象 |
| ① | 4.0 | 0 | 0 | x | 3滴 | 较快褪色 |
| ② | 0 | 4.0 | 4.0 | 0 | 3滴 | 不褪色 |
| ③ | 4.0 | 0 | 4.0 | 0 | 3滴 | 缓慢褪色 |
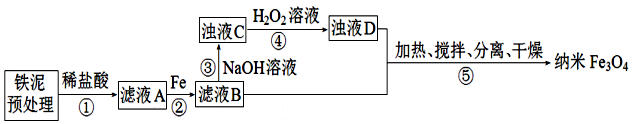
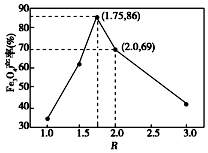
已知:步骤⑤中,相同条件下测得Fe3O4的产率与R(R=$\frac{n(\stackrel{+3}{Fe})}{n(\stackrel{+2}{Fe})}$)的关系如图所示.
(1)为提高步骤①的反应速率,可采取的措施是搅拌、适当升高温度.
(2)步骤②中,主要反应的离子方程式是2Fe3++Fe=3Fe2+.
(3)常温下Fe3+、Fe2+以氢氧化物形式完全沉淀时溶液的pH如图.该温度下Ksp[Fe(OH)3]=1.0×10-38
| 沉淀物 | Fe(OH)3 | Fe(OH)2 |
| 完全沉淀物PH | 3.0 | 8.3 |
步骤④中,反应完成后需再加热一段时间除去剩余H2O2目的是加热使其分解除去,防止其在步骤⑤中继续氧化+2价铁元素
(5)⑤反应的离子方程式为2FeOOH+Fe2++2OH-$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+2H2O;步骤⑤中的“分离”包含的步骤有过滤、洗涤.
(6)设浊液D中FeOOH的物质的量为a,滤液B中的铁元素的物质的量为b.为使Fe3O4的产率最高,则$\frac{a}{b}$=0.636.(填数值,小数点后保留3位)
| A. | 催化剂V2O5不改变该反应的逆反应速率 | |
| B. | 不论以何种方式使反应体系的压强增大,化学反应速率一定增大 | |
| C. | 该反应是放热反应,降低温度将缩短反应到达平衡的时间 | |
| D. | 当该反应到达平衡时,SO2、O2、SO3都存在于反应体系中 |
| A. | 2H2O?H3O++OH- | B. | H2S?H++HS- | C. | NaHS=Na++HS- | D. | HCO3-=H++CO32- |