题目内容
18.有甲、乙、丙三种物质:
(1)乙中含有的官能团的名称为氯原子和羟基.
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):

其中反应Ⅰ的反应类型是取代反应,反应Ⅱ的条件是氢氧化钠水溶液、加热,
反应Ⅲ的化学方程式为
 (不需注明反应条件).
(不需注明反应条件).(3)由甲出发合成丙的路线之一如下

①下列物质不能与B反应的是bc(填字母).
a.金属钠 b.FeCl3 c.碳酸钠溶液 d.HBr
②丙的结构简式为
 .
.③D符合下列条件的所有同分异构体3种,任写其中一种能同时满足下列条件的同分异构体结构简式:
 、
、 、
、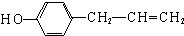 (任写一种).
(任写一种).a.苯环上的一氯代物有两种 b.遇FeCl3溶液发生显色反应 c.能与Br2/CCl4溶液反应.
分析 (1)乙中官能团是氯原子、羟基;
(2)甲和HCl发生加成反应生成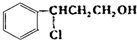 ,
,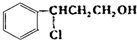 发生催化氧化反应生成Y,Y结构简式为
发生催化氧化反应生成Y,Y结构简式为 ,Y发生消去反应生成乙;
,Y发生消去反应生成乙;
(3)甲和溴水发生加成反应生成A,A的结构简式为: ,
, 和氢氧化钠的水溶液发生取代反应生成B,B的结构简式为:
和氢氧化钠的水溶液发生取代反应生成B,B的结构简式为: ,B被氧化生成C,则C的结构简式为:
,B被氧化生成C,则C的结构简式为: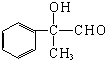 ,丙能使溴褪色,说明丙中含有碳碳双键,C发生消去反应生成丙,则丙的结构简式为:
,丙能使溴褪色,说明丙中含有碳碳双键,C发生消去反应生成丙,则丙的结构简式为: ,B发生消去反应生成D,D的结构简式为:
,B发生消去反应生成D,D的结构简式为: .
.
解答 解:(1)甲、乙中含氧官能团的名称分别为醇羟基、醛基,故答案为:醇羟基;醛基;
(2)甲和HCl发生加成反应生成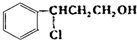 ,
,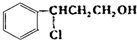 发生催化氧化反应生成Y,Y结构简式为
发生催化氧化反应生成Y,Y结构简式为 ,Y发生消去反应生成乙;
,Y发生消去反应生成乙;
I的反应类型是取代反应;II的反应类型是消去反应,条件是NaOH的水溶液、加热,Ⅲ为碳碳双键与HCl的加成反应,该反应为 ;
;
故答案为:取代反应;氢氧化钠水溶液、加热; ;
;
(3)甲和溴水发生加成反应生成A,A的结构简式为: ,
, 和氢氧化钠的水溶液发生取代反应生成B,B的结构简式为:
和氢氧化钠的水溶液发生取代反应生成B,B的结构简式为: ,B被氧化生成C,则C的结构简式为:
,B被氧化生成C,则C的结构简式为: ,丙能使溴褪色,说明丙中含有碳碳双键,C发生消去反应生成丙,则丙的结构简式为:
,丙能使溴褪色,说明丙中含有碳碳双键,C发生消去反应生成丙,则丙的结构简式为: ,B发生消去反应生成D,D的结构简式为:
,B发生消去反应生成D,D的结构简式为: ;
;
①B为 ,可与钠、HBr发生反应,与氯化铁、碳酸钠不反应,
,可与钠、HBr发生反应,与氯化铁、碳酸钠不反应,
故答案为:bc;
②由以上分析可知丙为 ,故答案为:
,故答案为: ;
;
③D的结构简式为: ,D的结构简式符合下列条件:
,D的结构简式符合下列条件:
a.苯环上的一氯代物有两种说明苯环上含有两类氢原子;
b.遇FeCl3溶液发生显色反应说明含有酚羟基;
c.能与Br2/CCl4发生加成反应说明含有碳碳不饱和键,
则符合条件的D的同分异构体有: 、
、 、
、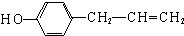 ,所以有3种同分异构体,
,所以有3种同分异构体,
故答案为:3; 、
、 、
、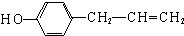 (任写一种).
(任写一种).
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,明确有机物官能团结构和性质关系是解本题关键,注意结合反应条件进行推断,题目难度中等.

 硝基苯是重要的精细化工原料,是医药和染料的中间体,还可做有机溶剂.制备硝基苯的过程如下:
硝基苯是重要的精细化工原料,是医药和染料的中间体,还可做有机溶剂.制备硝基苯的过程如下:①配制混酸:组装如图反应装置.取100 mL烧杯,用20 mL浓硫酸与浓硝酸18 mL配制混和酸,加入漏斗中.把18 mL苯加入三颈烧瓶中.
②向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀.
③在50-60℃下发生反应,直至反应结束.
④除去混和酸后,粗产品依次用蒸馏水和10%Na2CO3溶液洗涤,最后再用蒸馏水洗涤得到粗产品.
已知(1)
 +HNO3(浓)$→_{98%浓H_{2}SO_{4}}^{50-60℃}$
+HNO3(浓)$→_{98%浓H_{2}SO_{4}}^{50-60℃}$ +H2O
+H2O 
(2)可能用到的有关数据列表如下
| 物质 | 熔点/℃ | 沸点/℃ | 密度(20℃)/g•cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 1,3-二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | 83 | 1.4 | 易溶于水 | |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |
(1)配置混酸应先在烧杯中先加入浓硝酸.
(2)恒压滴液漏斗的优点是可以保持漏斗内压强与发生器内压强相等,使漏斗内液体能顺利流下.
(3)实验装置中长玻璃管可用冷凝管(球形冷凝管或直行冷凝管均可)代替(填仪器名称).
(4)反应结束后产品在液体的下层(填“上”或者“下”),分离混酸和产品的操作方法为分液.
(5)用10%Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净?取最后一次洗涤液,向溶液中加入氯化钙,无沉淀生成,说明已洗净.
(6)为了得到更纯净的硝基苯,还须先向液体中加入氯化钙除去水,然后蒸馏,最终得到17.5g硝基苯,则硝基苯的产率为70%(保留两位有效数字).若加热后,发现未加沸石,应采取的操作是停止加热,待冷却后加入.
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 所有物质之间均存在化学键 | |
| C. | 由非金属元素可以组成离子化合物 | |
| D. | 不同元素组成的多原子分子里的化学键一定为极性键 |
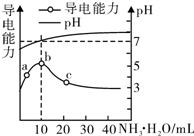
| A. | a~b点导电能力增强说明HR为弱酸 | |
| B. | b点溶液pH=7说明NH4R没有水解 | |
| C. | c点溶液存在c( NH4+)>c( R-)、c(OH-)>c(H+) | |
| D. | b~e任意点溶液均有c(H+)×c(OH-)=Kw=l.0×l0-14 |
钠碱循环法脱硫技术.
(1)此法是利用Na2SO3溶液可脱除烟气中的SO2.Na2SO3可由NaOH溶液吸收SO2制得,该反应的离子方程式:SO2+2OH-=SO32-+H2O.
(2)NaOH溶液吸收SO2的过程中,pH随(SO32-):n(HSO3-)变化关系如表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| PH | 8.2 | 7.2 | 6.2 |
②当溶液呈中性时,离子浓度关系正确的是(选填字母):bc.
a.c(Na+)═c(SO32-)+c(HSO32-)+c(H2SO3)
b.c(Na+)>c(HSOe-)>c(SOe2-)>c(H+)═c(OH-)
c.c(Na+)═2c(SOe2-)+c(HSOe-)
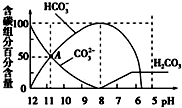
| A. | 0.1 mol/L Na2CO3溶液中c(Na+)+c(H+)═2c(CO32-)+c(HCO3-)+c(OH-) | |
| B. | 当加入20 mL盐酸时,混合溶液的pH约为8 | |
| C. | 常温下CO2饱和溶液的pH约为5.6 | |
| D. | 在A点:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
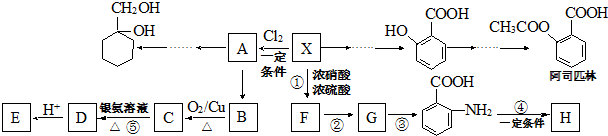
 (苯胺,易被氧化)
(苯胺,易被氧化)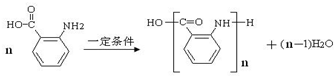 .
.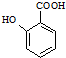 的同系物M比其本身相对分子质量大14,M的同分异构体中能同时满足以下条件:①芳香族化合物,②能发生水解反应,③与FeCl3溶液能够发生显色反应;共有19(不考虑立体异构)种.
的同系物M比其本身相对分子质量大14,M的同分异构体中能同时满足以下条件:①芳香族化合物,②能发生水解反应,③与FeCl3溶液能够发生显色反应;共有19(不考虑立体异构)种.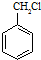 和其他无机物合成
和其他无机物合成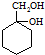 最合理的方案.
最合理的方案.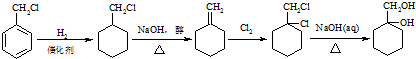 .
.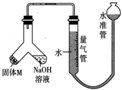 某课外兴趣小组为探究某种铝合金(合金元素为Mg、Al)是否符合国家质量标准(国家规定其中铝含量不能低于78%),设计如图所示装置进行实验.
某课外兴趣小组为探究某种铝合金(合金元素为Mg、Al)是否符合国家质量标准(国家规定其中铝含量不能低于78%),设计如图所示装置进行实验.