题目内容
NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、常温常压下,44 g C3H8中含有的碳碳单键数为3NA |
| B、1mol羟基中电子数为10NA |
| C、室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
| D、标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.1个C3H8中含有2个碳碳单键;
B.1个羟基中含有9个电子;
C.乙烯和丁烯的最简式为CH2,只需计算21.0gCH2中碳原子数;
D.标准状况甲醇不是气体;
B.1个羟基中含有9个电子;
C.乙烯和丁烯的最简式为CH2,只需计算21.0gCH2中碳原子数;
D.标准状况甲醇不是气体;
解答:
解:A.常温常压下,44gC3H8的物质的量为1mol,含有的碳碳单键数为2NA,故A错误;
B.1个羟基中含有9个电子,1mol羟基中含有9mol电子,故B正确;
C.乙烯和丁烯的最简式为CH2,只需计算21.0gCH2中碳原子数=
×NA=1.5NA,标准状况下,22.4LNO和11.2LO2混合后气体的分子总数为1.5NA ,故C正确;
D.标准状况甲醇不是气体,22.4L甲醇物质的量不是1mol,故D错误;
故选C.
B.1个羟基中含有9个电子,1mol羟基中含有9mol电子,故B正确;
C.乙烯和丁烯的最简式为CH2,只需计算21.0gCH2中碳原子数=
| 21g |
| 14g/mol |
D.标准状况甲醇不是气体,22.4L甲醇物质的量不是1mol,故D错误;
故选C.
点评:本题考查了阿伏伽德罗常数的分析应用概念理解,微粒数计算,气体摩尔体积的条件应用,物质性质的分析判断是解题关键.题目难度中等.

练习册系列答案
相关题目
设NA为阿伏加德罗常数,下列说法不正确的是( )
| A、标准状况下22.4L Cl2和H2混合气体原子数为2NA |
| B、1mol Na2O2和足量的水完全反应,转移的电子数为NA |
| C、1mol金刚石中含共价键数目为4NA |
| D、电解食盐水若产生2g氢气,则转移的电子数目为2NA |
对于可逆反应:2NH3(g)?N2(g)+3H2(g);正反应为吸热反应,当温度升高时,下列说法一定正确的是( )
| A、v(正)增大,v(逆)减小 |
| B、v(正)>v(逆) |
| C、v(正)、v(逆)都增大 |
| D、v(正)<v(逆) |
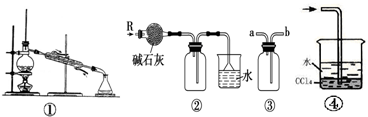 如图各装置不能达到实验目的是( )
如图各装置不能达到实验目的是( )| A、装置①可制取少量蒸馏水 |
| B、装置②可用于干燥、收集氨气,并吸收多余的氨气 |
| C、装置③可用于排空气法收集NO气体 |
| D、装置④中下层物质若为四氯化碳,则可用于吸收氯化氢 |
用如图所示实验装置进行相应实验,能达到实验目的是( ) 

| A、装置①所示的气流方向可用于收集H2、NH3等 |
| B、按装置②可证明非金属性Cl>C>Si |
| C、装置③向左推动针筒活塞可检验该装置的气密性 |
| D、装置④可用于除去Cl2中含有的少量HCl气体 |
将下列各组物质按酸、碱、盐分类顺次排列.其中正确的是( )
| A、硫酸,纯碱,醋酸钠 |
| B、硝酸,烧碱,纯碱 |
| C、盐酸,乙醇,醋酸钠 |
| D、盐酸,熟石灰,苛性钠 |
 某反应的反应过程中能量变化如图所示.下列有关叙述不正确的是( )
某反应的反应过程中能量变化如图所示.下列有关叙述不正确的是( )| A、该反应的△H>0 |
| B、E1表示正反应的活化能 |
| C、E2表示逆反应的活化能 |
| D、使用催化剂降低正反应的活化能,不能降低逆反应的活化能 |