题目内容
18.某可逆反应正向反应过程中能量变化如图所示,下列说法不正确的是( )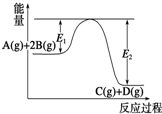
| A. | 该反应为放热反应 | |
| B. | 当反应达到平衡时,降低温度,A的转化率增大 | |
| C. | 压强增大,平衡向正反应方向移动 | |
| D. | 加入催化剂,反应速率增大,E1减小,E2减小,反应热减小 |
分析 A.当反应物的能量高于生成物的能量,反应是放热,反之是吸热;
B.降低温度平衡向放热方向移动;
C.增大压强,平衡向气体体积减小的方向移动;
D.催化剂不会改变反应的焓变.
解答 解:A.由图可知,反应物A(g)和2B(g)的总能量大于生成物C(g)和D(g)的总能量,为放热反应,故A正确;
B.正方向为放热反应,则降低温度平衡向放热方向移动,即正向移动,则A的转化率增大,故B正确;
C.增大压强,平衡向气体体积减小的方向移动,对于该反应而言,平衡正向移动,故C正确;
D.加入催化剂,降低反应的活化能,则E1减小,E2减小,反应速率增大,由于反应物与生成物的总能量差不变,即△H不变,故D错误;
故选D.
点评 本题涉及物质的能量和反应的吸放热之间的关系、催化剂的特点以及温度对化学平衡移动的影响等方面的知识,综合性较强,难度不大.

练习册系列答案
相关题目
8.燃料电极是一种高效、环境友好的发电装置,某氢氧燃料电池的构造示意图如下,该电池工作时,下列说法正确的是( )

| A. | a电极是该电池的正极 | B. | O2在b电极上发生氧化反应 | ||
| C. | 电解质溶液中OH-向正极移动 | D. | 该装置实现了化学能到电能的转化 |
9.下列关于热化学反应的描述中正确的是( )
| A. | 吸热反应不一定需要加热才能发生 | |
| B. | CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)═2CO(g)+O2(g)△H=2×283.0 kJ/mol | |
| C. | HCl和NaOH反应的中加热△H=-57.3 kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol | |
| D. | 1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
6.NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,44 g C3H8中含有的共价键数为11 NA | |
| B. | 0.1 mol醛基中的电子数为1.5NA | |
| C. | 室温下,28.0 g乙烯和一氧化碳的混合气体中含有的碳原子数目为1.5NA | |
| D. | 标准状况下,22.4 L乙醇中含有的氧原子数为1.0NA |
13.决定化学反应速率的主要因素是( )
| A. | 参加反应的物质本身的性质 | B. | 催化剂 | ||
| C. | 温度 | D. | 反应物的浓度或压强 |
3.下列不能使溴水完全褪色的是( )
| A. | 碳酸钠 | B. | 氢氧化钾溶液 | C. | 二氧化硫 | D. | KI溶液 |
10.下列反应中没有表明乙酸酸性比碳酸酸性强的是( )
| A. | 2CH3COOH+BaCO3→(CH3COO)2Ba+CO2↑+H2O | |
| B. | CH3COOH+KHCO3→CH3COOK+CO2↑+H2O | |
| C. | 2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O | |
| D. | CH3COOH+Na2CO3→CH3COONa+NaHCO3 |

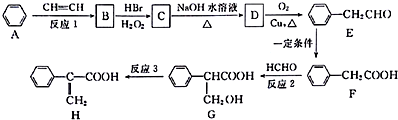
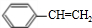 .
.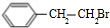 ;②D-E的化学方程式是2
;②D-E的化学方程式是2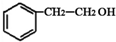 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2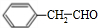 +2H2O;
+2H2O;