题目内容
8.燃料电极是一种高效、环境友好的发电装置,某氢氧燃料电池的构造示意图如下,该电池工作时,下列说法正确的是( )
| A. | a电极是该电池的正极 | B. | O2在b电极上发生氧化反应 | ||
| C. | 电解质溶液中OH-向正极移动 | D. | 该装置实现了化学能到电能的转化 |
分析 一个电极反应为:O2+2H2O+4e-═4OH-,该电极上氧气得电子发生还原反应,所以为正极,则通入氢气的电极是负极,将电池反应式减去正极反应式就是负极反应式,放电时,电解质溶液中阴离子向负极移动,据此分析解答.
解答 解:A、通入燃料氢气的电极是负极,通氧气的电极是正极,所以a是负极,故A错误;
B、通入燃料氢气的电极a是负极,通氧气的电极b是正极,O2在b电极上发生还原反应,故B错误;
C、电解质溶液中OH-向负极移动,故C错误;
D、燃料电池的工作原理属于原电池原理,是化学能转化为电能的装置,故D正确;
故选D.
点评 本题考查化学电源新型电池,为高频考点,明确正确判断正负极是解本题关键,难点是电极反应式的书写,注意结合电解质溶液酸碱性书写.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案
相关题目
19.已烯雌酚是一种激素类药物,结构如下:
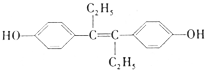
下列有关叙述中不正确的是( )

下列有关叙述中不正确的是( )
| A. | 可以用有机溶剂萃取 | |
| B. | 可与NaOH或NaHCO3溶液发生反应 | |
| C. | 1mol该有机物可以与5molBr2发生反应 | |
| D. | 该有机物分子中,可能有8个碳原子共平面 |
16.下列物质中,既含共价键又含离子键的是( )
| A. | NaCl | B. | O2 | C. | NaOH | D. | CO2 |
3.下列事实描述不正确的是( )
| A. | 高温煅烧石灰石的反应中,反应物总能量高于生成物总能量 | |
| B. | 中和反应中,反应物总能量高于生成物总能量 | |
| C. | 铝粉和盐酸反应时,溶液温度通常会上升 | |
| D. | 氢氧化钡晶体和氯化铵晶体的反应是吸热反应 |
13.某研究小组设计了如下实验,探究常温下催化剂对过氧化氢分解反应的影响.
(1)实验Ⅰ的作用是对照实验,证明实验Ⅱ和Ⅲ中的速率加快与溶液浓度无关.
(2)实验Ⅲ反应的化学方程式为2H2O2$\frac{\underline{\;三氯化铁\;}}{\;}$2H2O+O2↑.
(3)根据实验Ⅰ~Ⅲ中现象的不同,可以得出的结论是:
①使用合适的催化剂,可提高双氧水分解的反应速率:
②不同催化剂的催化效率不同.
(4)在一定温度下,10mL0.40mol/LH2O2溶液发生催化分解.不同时刻测得生成O2的体积(已折算为标准差状况)如下表所示:
0~6min,以H2O2的浓度变化表示的反应速率为v(H2O2)=0.033mol/(L•min).(计算结果精确到0.001)
| 序号 | 实验操作示意图 | 实验现象 |
| Ⅰ | 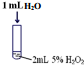 | 有极少量气泡产生 |
| Ⅱ | 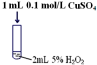 | 产生气泡速率略有加快 |
| Ⅲ | 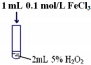 | 产生气泡速率明显加快 |
(2)实验Ⅲ反应的化学方程式为2H2O2$\frac{\underline{\;三氯化铁\;}}{\;}$2H2O+O2↑.
(3)根据实验Ⅰ~Ⅲ中现象的不同,可以得出的结论是:
①使用合适的催化剂,可提高双氧水分解的反应速率:
②不同催化剂的催化效率不同.
(4)在一定温度下,10mL0.40mol/LH2O2溶液发生催化分解.不同时刻测得生成O2的体积(已折算为标准差状况)如下表所示:
| t/min | 0 | 2 | 3 | 6 | 8 | 10 |
| v(O2)mL | 0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
20.下列有关实验装置正确的是( )
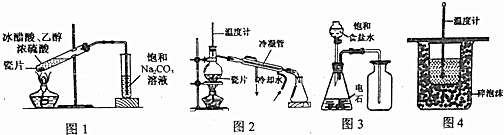

| A. | 用图1装置制取少量乙酸乙酯 | B. | 用图2装置分离苯和溴苯 | ||
| C. | 用图3装置制取并收集乙炔气体 | D. | 用图4装置测定中和热 |
18.某可逆反应正向反应过程中能量变化如图所示,下列说法不正确的是( )
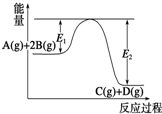

| A. | 该反应为放热反应 | |
| B. | 当反应达到平衡时,降低温度,A的转化率增大 | |
| C. | 压强增大,平衡向正反应方向移动 | |
| D. | 加入催化剂,反应速率增大,E1减小,E2减小,反应热减小 |
 .
. .
.