题目内容
用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、标准状况下,22.4LCCl4含有NA个分子 |
| B、0.1molAlCl3完全转化为胶体,生成胶体粒子的数目为0.l NA个 |
| C、常温常压下46gNO2和N2O4的混合气体含有3NA个原子 |
| D、0.1molCl2与足量冷的NaOH溶液反应,转移电子数为0.2 NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、标况下,是CCl4是液态;
B、一个Al(OH)3胶粒是多个Al(OH)3的集合体;
C、根据NO2和N2O4的最简式均为NO2来计算;
D、Cl2与NaOH的反应为歧化反应来分析.
B、一个Al(OH)3胶粒是多个Al(OH)3的集合体;
C、根据NO2和N2O4的最简式均为NO2来计算;
D、Cl2与NaOH的反应为歧化反应来分析.
解答:
解:A、标况下,是CCl4是液态,故A错误;
B、一个Al(OH)3胶粒是多个Al(OH)3的集合体,故生成胶体粒子的数目少于0.l NA个,故B错误;
C、NO2和N2O4的最简式均为NO2,故46g混合气体中NO2的物质的量n=
=
=1mol,而1molNO2中含3mol原子,故含有的原子个数为3NA个,故C正确;
D、Cl2与NaOH的反应为歧化反应:Cl2+2NaOH=NaCl+NaClO+H2O,此反应中1molCl2转移1mol电子,故0.1mol氯气转移0.1mol电子,故D错误.
故选C.
B、一个Al(OH)3胶粒是多个Al(OH)3的集合体,故生成胶体粒子的数目少于0.l NA个,故B错误;
C、NO2和N2O4的最简式均为NO2,故46g混合气体中NO2的物质的量n=
| m |
| M |
| 46g |
| 46g/mol |
D、Cl2与NaOH的反应为歧化反应:Cl2+2NaOH=NaCl+NaClO+H2O,此反应中1molCl2转移1mol电子,故0.1mol氯气转移0.1mol电子,故D错误.
故选C.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
下列说法在一定条件下可以实现的是( )
①酸性氧化物与碱发生反应;
②弱酸与盐溶液反应可以生成强酸;
③没有水生成,也没有沉淀和气体生成的复分解反应;
④两种酸溶液充分反应后的溶液体系为中性;
⑤有两种氧化物反应的产物有气体.
①酸性氧化物与碱发生反应;
②弱酸与盐溶液反应可以生成强酸;
③没有水生成,也没有沉淀和气体生成的复分解反应;
④两种酸溶液充分反应后的溶液体系为中性;
⑤有两种氧化物反应的产物有气体.
| A、①②③④⑤ | B、②④⑤ |
| C、①②③⑤ | D、③④⑤ |
将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)?2G(g).忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
下列判断不正确的是( )
压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
| A、b>f |
| B、K(1000℃)>K(810℃) |
| C、915℃、2.0MPa时E的转化率为60% |
| D、该反应的△S>0 |
向ZnSO4溶液中加入Na2S溶液时,得到白色沉淀,然后向白色沉淀上滴加CuSO4溶液,发现沉淀变为黑色,则下列说法不正确的是( )
| A、利用该原理可实现一种沉淀转化为更难溶的沉淀 |
| B、该过程破坏了ZnS的溶解平衡 |
| C、白色沉淀为ZnS,而黑色沉淀为CuS |
| D、上述现象说明ZnS的Ksp小于CuS的Ksp |
已知下列数据
Fe(s)+
O2(g)=FeO(s)△H1=-272kJ/mol
2Al(s)+
O2(g)=Al2O3(s)△H2=-1675kJ/mol
则2Al(s)+3FeO(s)=Al2O3(s)+3Fe(s)的△H3的是( )
Fe(s)+
| 1 |
| 2 |
2Al(s)+
| 3 |
| 2 |
则2Al(s)+3FeO(s)=Al2O3(s)+3Fe(s)的△H3的是( )
| A、+859kJ/mol |
| B、-859kJ/mol |
| C、-1403kJ/mol |
| D、+1403kJ/mol |
恒温、恒压下,1molA和amolB在一个容积可变的容器中发生如下反应:A(g)+2B(g)?2C(g). 一段时间后达到平衡,生成bmolC.则下列说法中正确的是( )
| A、当v正(A)═2v逆(C)时,可断定反应已达平衡 |
| B、起始时刻和达平衡后容器中的压强比为 1:1 |
| C、物质A、B的转化率之比为1:2 |
| D、若起始时放入2molA和2amolB,则达平衡时生成2bmolC |
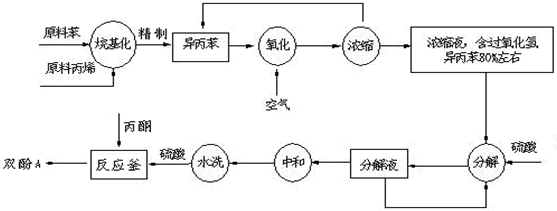
 (2)在氧化操作中,需要严格控制温度,防止温度过高.其原因是:①防止反应过于剧烈②
(2)在氧化操作中,需要严格控制温度,防止温度过高.其原因是:①防止反应过于剧烈② 如图是实验室制乙烯的发生装置和乙烯性质实验装置,反应原理为:
如图是实验室制乙烯的发生装置和乙烯性质实验装置,反应原理为: