题目内容
双酚A,也称BPA,用来生产防碎塑料.每年,全世界生产2700万吨含有PBA的塑料.但BPA也能导致内分泌 失调,威胁着胎儿和儿童的健康.欧盟认为含双酚A奶瓶 会诱发性早熟,从2011年3月2日起,禁止含生产化学物质双酚A(BPA)的婴儿奶瓶.采用苯和丙烯为原料,经过氧化、分解生成丙酮、苯酚,再使之反应生成双酚A工艺过程如下:
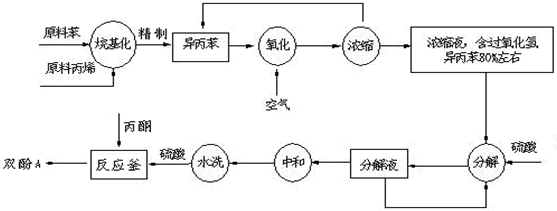
已知过氧化氢异丙苯化学式为C6H5C3H6OOH,受热容易分解.
(1)氧化操作中进料前需先通一段时间氮气或水蒸气,才能进料.目的是
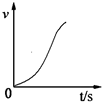 (2)在氧化操作中,需要严格控制温度,防止温度过高.其原因是:①防止反应过于剧烈② .一定温度下投料后发现反应速率如右图变化,其可能的原因是 .
(2)在氧化操作中,需要严格控制温度,防止温度过高.其原因是:①防止反应过于剧烈② .一定温度下投料后发现反应速率如右图变化,其可能的原因是 .
(3)分解操作中在常压下控制温度在70~80℃时,过氧化氢异丙苯分解方程式为 .浓缩操作必须严格控制条件,一般可采用 方法浓缩溶液
(4)制备双酚A反应釜中加入丙酮,其量等于或略大于流程中产生的过氧化氢异丙苯的量,目的是
该反应以硫酸为催化剂时,反应温度约40℃,反应在搅拌釜中进行.若反应时间过长,则产率明显降低.其原因可能是 .

已知过氧化氢异丙苯化学式为C6H5C3H6OOH,受热容易分解.
(1)氧化操作中进料前需先通一段时间氮气或水蒸气,才能进料.目的是
 (2)在氧化操作中,需要严格控制温度,防止温度过高.其原因是:①防止反应过于剧烈②
(2)在氧化操作中,需要严格控制温度,防止温度过高.其原因是:①防止反应过于剧烈②(3)分解操作中在常压下控制温度在70~80℃时,过氧化氢异丙苯分解方程式为
(4)制备双酚A反应釜中加入丙酮,其量等于或略大于流程中产生的过氧化氢异丙苯的量,目的是
该反应以硫酸为催化剂时,反应温度约40℃,反应在搅拌釜中进行.若反应时间过长,则产率明显降低.其原因可能是
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:(1)进料前需先通一段时间氮气或水蒸气,以便把空气排净;
(2)温度升高,反应速率加快,反应难于控制,过氧化氢异丙苯受热容易分解;
从图中看出反应速率加快,从影响反应速率的因素分析;
(3)过氧化氢异丙苯分解生成苯酚和丙酮;过氧化氢异丙苯受热容易分解,产物是有毒物质,浓缩时保证在密封设备进行,需要减压蒸发浓缩,生产效率高,操作条件好;
(4)增大一种反应物的浓度可以提高其他反应物的转化率;苯酚易被氧化.
(2)温度升高,反应速率加快,反应难于控制,过氧化氢异丙苯受热容易分解;
从图中看出反应速率加快,从影响反应速率的因素分析;
(3)过氧化氢异丙苯分解生成苯酚和丙酮;过氧化氢异丙苯受热容易分解,产物是有毒物质,浓缩时保证在密封设备进行,需要减压蒸发浓缩,生产效率高,操作条件好;
(4)增大一种反应物的浓度可以提高其他反应物的转化率;苯酚易被氧化.
解答:
解:(1)进料前需先通一段时间氮气或水蒸气,以便把空气排净,利于提高产物的纯度,故答案为:用氮气或水蒸气置换空气;
(2)温度升高,反应速率加快,反应难于控制,过氧化氢异丙苯受热容易分解;
从图中看出反应速率加快,加快反应速率的因素有增大压强、增大反应物浓度、升高温度和加催化剂,从反应过程是在一定温度下进行的反应,温度影响因素忽略,随反应进行,反应物浓度逐渐减小,压强对气体的影响较大,对固、液体的影响可以忽略,故可考虑催化剂的影响,即产物过氧化氢异丙苯对反应有催化作用;
故答案为:温度过高,反应产物过氧化氢异丙苯容易受热分解;产物过氧化氢异丙苯对反应有催化作用;
(3)过氧化氢异丙苯分解生成苯酚和丙酮,反应方程式为C6H5C3H6OOH
C6H5OH+CH3COCH3;分解产物有毒,需要在密封的设备中进行操作,可以使用减压蒸发浓缩,生产效率高,操作条件好;
故答案为:C6H5C3H6OOH
C6H5OH+CH3COCH3;减压蒸发浓缩;
(4)丙酮的量增大,可以使苯酚能够充分的反应,提高苯酚的转化率;苯酚易被氧化,暴露在空气中被氧气氧化为粉红色的醌,而使产率明显降低.
故答案为:使苯酚充分反应,提高其转化率;苯酚被空气中的氧气氧化.
(2)温度升高,反应速率加快,反应难于控制,过氧化氢异丙苯受热容易分解;
从图中看出反应速率加快,加快反应速率的因素有增大压强、增大反应物浓度、升高温度和加催化剂,从反应过程是在一定温度下进行的反应,温度影响因素忽略,随反应进行,反应物浓度逐渐减小,压强对气体的影响较大,对固、液体的影响可以忽略,故可考虑催化剂的影响,即产物过氧化氢异丙苯对反应有催化作用;
故答案为:温度过高,反应产物过氧化氢异丙苯容易受热分解;产物过氧化氢异丙苯对反应有催化作用;
(3)过氧化氢异丙苯分解生成苯酚和丙酮,反应方程式为C6H5C3H6OOH
| 硫酸 |
| 70-80℃ |
故答案为:C6H5C3H6OOH
| 硫酸 |
| 70-80℃ |
(4)丙酮的量增大,可以使苯酚能够充分的反应,提高苯酚的转化率;苯酚易被氧化,暴露在空气中被氧气氧化为粉红色的醌,而使产率明显降低.
故答案为:使苯酚充分反应,提高其转化率;苯酚被空气中的氧气氧化.
点评:本题考查了双酚A的制备过程,注意操作过程中的根据物质的性质选择合理的制备方法,解答时注意题给信息的选取使用.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
设阿伏加德罗常数为6.02×1023mol-1,关于1molH2O的叙述正确的是( )
| A、含有1molH2 |
| B、含有6.02×1023个水分子 |
| C、质量为18g/mol |
| D、在标准状况下的体积为22.4L |
如图是某物质发生化学反应的示意图,其中“ ”表示碳原子,“
”表示碳原子,“ ”表示氧原子,“
”表示氧原子,“ ”表示氢原子,则生成物甲的化学式为
”表示氢原子,则生成物甲的化学式为 ( )
( )
 ”表示碳原子,“
”表示碳原子,“ ”表示氧原子,“
”表示氧原子,“ ”表示氢原子,则生成物甲的化学式为
”表示氢原子,则生成物甲的化学式为 ( )
( )| A、H2 |
| B、CO2 |
| C、H2O |
| D、CO |
用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、标准状况下,22.4LCCl4含有NA个分子 |
| B、0.1molAlCl3完全转化为胶体,生成胶体粒子的数目为0.l NA个 |
| C、常温常压下46gNO2和N2O4的混合气体含有3NA个原子 |
| D、0.1molCl2与足量冷的NaOH溶液反应,转移电子数为0.2 NA |
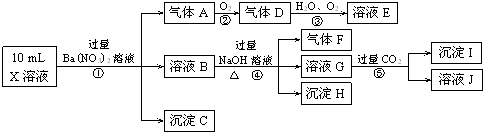
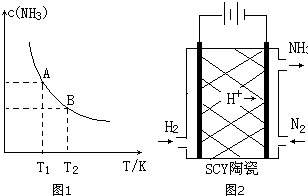 (1)在一定条件下,将1.00molN2(g)与3.00molH2(g)混合于一个10.0L密闭容器中,在不同温度下达到平衡时NH3(g)的平衡浓度如图所示.其中温度为T1时平衡混合气体中氨气的体积分数为25.0%.
(1)在一定条件下,将1.00molN2(g)与3.00molH2(g)混合于一个10.0L密闭容器中,在不同温度下达到平衡时NH3(g)的平衡浓度如图所示.其中温度为T1时平衡混合气体中氨气的体积分数为25.0%.